Propriedades das soluções
970 likes | 1.35k Views
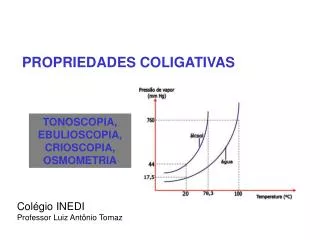
QUÍMICA I. Propriedades das soluções. Prof. Marcelo R. Alexandre. O processo de dissolução. Uma solução é uma mistura homogênea de soluto (presente em menor quantidade) e solvente (presente em maior quantidade). Os solutos e solvente são componentes da solução. O processo de dissolução.

Propriedades das soluções
E N D
Presentation Transcript
QUÍMICA I Propriedades das soluções Prof. Marcelo R. Alexandre
O processo de dissolução • Uma solução é uma mistura homogênea de soluto (presente em menor quantidade) e solvente (presente em maior quantidade). • Os solutos e solvente são componentes da solução.
O processo de dissolução • Considere o NaCl (soluto) dissolvendo-se em água (solvente): • as ligações de H da água têm que ser quebradas, • o NaCl se dissocia em Na+ e Cl-, • formam-se forças íon-dipolo: Na+…-OH2 e Cl- …+H2O. • Dizemos que os íons são solvatados pela água. • Se água é o solvente, dizemos que os íons são hidratados.
O processo de dissolução • Mudanças de energia e formação de solução • Há três fases de energia na formação de uma solução: • a separação das moléculas do soluto (H1), • a separação das moléculas do solvente (H2) ea formação das interações soluto-solvente (H3). • Definimos a variação de entalpia no processo de dissolução como • Hdissol = H1 + H2 + H3 • O Hsoln pode tanto ser positivo como negativo, dependendo das forças intermoleculares.
O processo de dissolução • Formação de solução, • espontaneidade e desordem • Um processo espontâneo ocorre sem intervenção externa. • Quando a energia do sistema diminui (por exemplo, deixar um livro cair e permitir que ele caia para uma energia potencial mais baixa), o processo é espontâneo. • Alguns processos espontâneos não envolvem a variação do sistema para um estado de energia mais baixa (por exemplo, uma reação endotérmica).
O processo de dissolução • Formação de solução, • espontâneidade e desordem • Se o processo leva a um maior estado de desordem, então o processo é espontâneo. • Exemplo: um mistura de CCl4 e C6H14 é menos ordenada do que os dois líquidos separados. Conseqüentemente, eles se misturam espontaneamente, apesar do Hdissol ser muito próximo de zero. • Há soluções que se formam a partir de processos físicos e outras por processos químicos.
O processo de dissolução Formação de solução, espontaneidade e desordem
O processo de dissolução • Formação de solução e reações químicas • Exemplo: uma mistura de CCl4 e C6H14 é menos ordenada. • Considere: • Ni(s) + 2HCl(aq) NiCl2(aq) + H2(g) • Observe que a forma química da substância sendo dissolvida se alterou (Ni NiCl2). • Quando toda a água é removida da solução, não se encontra o Ni, apenas NiCl2·6H2O(s). Conseqüentemente, a dissolução do Ni em HCl é um processo químico.
O processo de dissolução • Formação de solução e reações químicas • Exemplo: • NaCl(s) + H2O (l) Na+(aq) + Cl-(aq). • Quando a água é removida da solução, encontra-se NaCl. Conseqüentemente, a dissolução do NaCl é um processo físico.
Soluções saturadas e solubilidade • Dissolva: soluto + solvente solução. • Cristalização: solução soluto + solvente. • Saturação: a cristalização e a dissolução estão em equilíbrio. • Solubilidade: é a quantidade de soluto necessária para formar uma solução saturada. • Supersaturada: é uma solução formada quando dissolve-se mais soluto do que em uma solução saturada.
Fatores que afetam a solubilidade • Interações soluto-solvente • Os líquidos polares tendem a se disssolver em solventes polares. • Líquidos miscíveis: misturam-se em quaisquer proporções. • Líquidos imiscíveis: não se misturam. • As forças intermoleculares são importantes: água e etanol são miscíveis porque as ligações de hidrogênio quebradas em ambos os líquidos puros são reestabelecidas na mistura. • O número de átomos de carbono em uma cadeia afeta a solubilidade: quanto mais átomos de C, menos solúvel em água.
Fatores que afetam a solubilidade • Interações soluto-solvente • O número de grupos -OH dentro de uma molécula aumenta a solubilidade em água. • Generalização: “semelhante dissolve semelhante”. • Quanto mais ligações polares na molécula, mais facilmente ela se dissolve em um solvente polar. • Quanto menos polar for a molécula, mais dificilmente ela se dissolve em um solvente polar e melhor ela se dissolve em um solvente apolar.
Fatores que afetam a solubilidade Interação soluto-solvente
Fatores que afetam a solubilidade Interações soluto-solvente
Fatores que afetam a solubilidade • Interações soluto-solvente • Efeitos da pressão • A solubilidade de um gás em um líquido é uma função da pressão do gás.
Fatores que afetam a solubilidade • Efeitos da pressão
Fatores que afetam a solubilidade • Efeitos da pressão • Quanto maior a pressão, mais próximas as moléculas de gás estarão do solvente e maior a chance da molécula de gás atingir a superfície e entrar na solução. • Conseqüentemente, quanto maior for a pressão, maior a solubilidade. • Quanto menor a pressão, menor a quantidade de moléculas de gás próximas ao solvente e menor a solubilidade. • Se Sg é a solubilidade de um gás, k é uma constante e Pg é a pressão parcial de um gás, então, a Lei de Henry nos fornece:
Fatores que afetam a solubilidade • Efeitos da pressão • As bebidas carbonadas são engarrafadas com uma pressão parcial de CO2 > 1 atm. • Ao abrirmos a garrafa, a pressão parcial de CO2 diminui e a solubilidade do CO2 também diminui. • Conseqüentemente, bolhas de CO2 escapam da solução.
Fatores que afetam a solubilidade • Efeitos de temperatura • A experiência nos mostra que o açúcar se dissolve melhor em água quente do que em água fria. • Geralmente, à medida que a temperatura aumenta, a solubilidade dos sólidos aumenta. • Algumas vezes, a solubilidade diminui quando a temperatura aumenta (por exemplo Ce2(SO4)3).
Fatores que afetam a solubilidade
Fatores que afetam a solubilidade • Efeitos de temperatura • A experiência nos mostra que as bebidas carbonadas ficam insípidas ao serem aquecidas. • Conseqüentemente, os gases se tornam menos solúveis à medida que a temperatura aumenta. • A poluição térmica: se os lagos se aquecem muito, o CO2 e o O2 tornam-se menos solúveis e ficam indisponíveis para as plantas ou animais.
Fatores que afetam a solubilidade
Formas de expressar a concentração • Porcentagem de massa, ppm e ppb • Todos os métodos envolvem medir a quantidade de soluto em função da quantidade de solvente (ou da solução). • Geralmente, as quantidades ou medidas são massas, quantidade de matéria ou litros. • Qualitativamente, as soluções são diluídas ou concentradas. • Definições:
Formas de expressar a concentração • Porcentagem de massa, ppm e ppb • Partes por milhão (ppm) podem ser expressas como 1 mg de soluto por quilograma de solução. • Se a densidade da solução é 1g mL-1, então 1 ppm = 1 mg de soluto por litro de solução. • Partes por bilhão (ppb) são 1 g de soluto por quilograma de solução.
Formas de expressar a concentração
Formas de expressar a concentração
Formas de expressar a concentração • Ex. Qual a concentração em quantidade de matéria de uma solução preparada pela dissolução de 10 g de NaNO3 em 500 mL de água? • C = n/V(L), onde n= m/MM • MM(NaNO3) = 23+14+(16x3) = 85 g/mol • n = 10g/85g/mol = 0,117 mol • C = 0,117/0,5 = 0,235 mol/L
Formas de expressar a concentração Ex. 50,0 g de NaCl foram dissolvidos em 250,0 mL de água. Considerando que a solução resultante tenha densidade igual a 1g/mL, expresse a concentração dessa solução em porcentagem de massa e ppm. %NaCl = (massa do componente/massa solução)x100 = 50g/300gx100 = 16,6% ppm = (massa do componente/massa solução)x1000000 = (50g/300g)x1000000 = 166666,67 ppm
Líquidos • As propriedades físicas das substâncias segundo a teoria cinética molecular : • Os gases são altamente compressíveis, assumem a forma e o volume do recipiente: As moléculas de gás estão separadas e não interagem muito entre si. • Os sólidos são incompressíveis e têm forma e volume definidos: As moléculas de sólidos estão mais próximas. As moléculas estão unidas de forma tão rígida que não conseguem deslizar facilmente umas sobre as outras.
Líquidos • Os líquidos são quase incompressíveis, assumem a forma, mas não o volume do recipiente: As moléculas de líquidos são mantidas mais próximas do que as moléculas de gases, mas não de maneira tão rígida de tal forma que as moléculas não possam deslizar umas sobre as outras.
Uma comparação entre líquidos e sólidos
Uma comparação entre líquidos e sólidos
Forças intermoleculares • A ligação covalente que mantém uma molécula unida é uma força intramolecular. • A atração entre moléculas é uma força intermolecular. • Forças intermoleculares são muito mais fracas do que as forças intramoleculares (por exemplo, 16 kJ mol-1versus 431 kJ mol-1 para o HCl). • Quando uma substância funde ou entra em ebulição, forças intermoleculares são quebradas (não as ligações covalentes).
Forças intermoleculares Forças íon-dipolo A interação entre um íon e um dipolo (por exemplo, água). A mais forte de todas as forças intermoleculares.
Forças intermoleculares • Forças dipolo-dipolo • As forças dipolo-dipolo existem entre moléculas polares neutras. • As moléculas polares necessitam ficar muito unidas. • Mais fracas do que as forças íon-dipolo. • Há uma mistura de forças dipolo-dipolo atrativas e repulsivas quando as moléculas se viram. • Se duas moléculas têm aproximadamente a mesma massa e o mesmo tamanho, as forças dipolo-dipolo aumentam com o aumento da polaridade.
Forças intermoleculares Forças dipolo-dipolo
Forças intermoleculares Forças dipolo-dipolo
Forças intermoleculares Forças de dispersão de London A mais fraça de todas as forças intermoleculares. É possível que duas moléculas adjacentes neutras se afetem. O núcleo de uma molécula (ou átomo) atrai os elétrons da molécula adjacente (ou átomo). Por um instante, as nuvens eletrônicas ficam distorcidas. Nesse instante, forma-se um dipolo (denominado dipolo instantâneo).
Forças intermoleculares Forças de dispersão de London Um dipolo instantâneo pode induzir outro dipolo instantâneo em uma molécula (ou átomo) adjacente. As forças entre dipolos instantâneos são chamadas forças de dispersão de London.
Forças intermoleculares Forças de dispersão de London Polarizabilidade é a facilidade com que a distribuição de cargas em uma molécula pode ser distorcida por um campo elétrico externo. Quanto maior é a molécula (quanto maior o número de elétrons) mais polarizável ela é. As forças de dispersão de London aumentam à medida que a massa molecular aumenta. Existem forças de dispersão de London entre todas as moléculas. As forças de dispersão de London dependem da forma da molécula.
Forças intermoleculares Forças de dispersão de London Quanto maior for a área de superfície disponível para contato, maiores são as forças de dispersão. As forças de dispersão de London entre moléculas esféricas são menores do que entre outros tipos de moléculas.
Forças intermoleculares Ligação de hidrogênio Caso especial de forças dipolo-dipolo. A partir de experimentos: os pontos de ebulição de compostos com ligações H-F, H-O e H-N são muito altos. Forças intermoleculares são fortes.
Forças intermoleculares • Ligação de hidrogênio • A ligação de H necessita do H ligado a um elemento eletronegativo (mais importante para compostos de F, O e N). • Os elétrons na H-X (X = elemento eletronegativo) encontram-se muito mais próximos do X do que do H. • O H tem apenas um elétron, dessa forma, na ligação H-X, o H + apresenta um próton quase descoberto. • Conseqüentemente, as ligações de H são fortes.
Forças intermoleculares Ligação de hidrogênio
Forças intermoleculares Ligação de hidrogênio