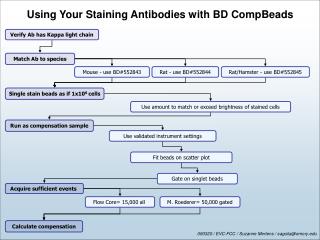
Section 1-11 염색 (Staining )
Section 1-11 염색 (Staining ). Stain. 염색의 필요성 생체나 고정상태의 세포는 구성성분이나 세포간 물질이 투명한 상태이며 각 성분들 간의 굴절률의 차이가 없으므로 검경 시 각 세포 구성 성분의 구별이 어렵기 때문에 염료 (dye) 를 사용하여 세포의 구성 성분을 가시화 시키는 일인 염색 (stain) 이 필요

Section 1-11 염색 (Staining )
E N D
Presentation Transcript
Section 1-11 염색 (Staining)
Stain • 염색의필요성 • 생체나 고정상태의 세포는 구성성분이나 세포간 물질이 투명한 상태이며 각 성분들 간의 굴절률의 차이가 없으므로 검경 시 각 세포 구성 성분의 구별이 어렵기 때문에 염료(dye)를 사용하여 세포의 구성 성분을 가시화 시키는 일인 염색(stain)이 필요 • Staining(염색)은 microscopic image에서 contrast (대비)를 증가시키는데 이용되는 보조 기술
Dye (염료) • 염료의 화학적 구성 • 벤젠(benzene) • Benzene 고리는 C6H6의 분자식으로 이루어진 방향족 유기 화합물이며, 다른 기(radical)와 치환반응을 하여 새 화합물을 생성 • benzene 분자에서 2개의 수소원자가 2개의 산소 원자로 치환되면 벤젠 고리 내 원자결합 (이중결합)의 재배열이 일어나 quinone 이라는 새로운 화합물 (quinoid compound)이 된다.
Dye (염료) • 염료의 화학적 구성 • 발색단 (chromophores) • 색을 내는 염료에는 이중결합을 하고 있으며, 방향족 유기화합물인 불포화 결합을 가지는 특정 원자단 • 발색단만 가지고 있는 화합물로 조직을 염색하면 일시적으로 염색이 된 것처럼 보이나 수세에 의해 곧 제거되기 때문에 발색단을 갖고 있다고 해도 모두 염료는 아니다. • 발색단의 종류 • ethylene 기(>C=C<), ketone (carbonyl) 기(>C=O), thiocarbonyl 기(>C=S), azo 기 (-N=N-), nitro 기 (-N=O), oxy-azo 기(-N=N-), quinone ring
Dye (염료) • 염료의 화학적 구성 • 색원체(chromogen) • 염료에 발색단이 많을수록 염료의 색은 진해지고, 발색단을 가지고 있는 방향족 유기화합물은 염료와 색소의 모체가 되므로 이를 색원체(chromogen)라 하며 그 자체로 조직성분에 착색이 가능 • 착색된 색원체는 저항성이 없어 수세를 하면 쉽게 제거된다.
Dye (염료) • 염료의 화학적 구성 • 조색단(auxochrome) • 색원체가 발색단에 의해 색을 나타내기는 하지만 염료가 되기 위해 조직과 친화력이 있는 제 2의 기를 필요로 하는데 이를 조색단이라 한다. • 조색단 자체는 색을 내지 않으며 다만 염료에 전해 능력을 부여하여 수용액에서 해리되어 색소가 조직에 잘 결합할 수 있게 한다. • 조색단의 종류 • amino 기(-NH2), hydroxyl 기(-OH), carboxyl 기(-COOH), sulfon산 기(-SO3H), 치환 amino 기(-N(R2))
Dye (염료) • 염료의 화학적 구성 • 염료 • 색을 나타내는 발색단과 조직성분과 결합능력을 갖는 조색단을 갖고 있는 유기화합물 • 염료 = 벤젠 + 발색단 + 조색단
Dye (염료) • 염료의 화학적 구성 • Leuco compounds (백색염기) • 대부분의 발색단은 분해되어 수소와 결합하여 단일결합으로 변하는 환원과정으로 인해 발색단이 파괴되어 색을 상실하게 되는데 이를 leucobase (백색염기)라 한다. • PAS 염색에 이용되는 Schiff reagent 가 대표적 예이다.
Dye (염료) • 염료의 화학적 구성 • 매염제 (mordants) • 염료와 조직 사이를 연결하여 염색이 가능하도록 조력하는 물질 (조직과 염색액 사이에 요철형) • 매염제는 먼저 염료와 결합하여 “lake (dye + mordant)”라 부르는 화합물을 형성하며 자체로는 색이 매우 약하여 염색으로서의 가치는 없지만 이런 상태의 화합물은 조직에 강하게 부착 • 일반염색에 사용되는 hematoxylin 용액은 alum (NH4, K)이 매염제로 사용되고, 미생물 염색 중 Gram 염색은 iodine을 매염제로 사용 • 조직화학에서 일반적으로 사용되는 매염제는 chromium, aluminium, iron, sulfate 염
Dye (염료) • 염료의 화학적 구성 • 염색 강화제 (accentuators, 염색 보강제 ) • 매염제와 같이 어떤 분명한 화학적 결합을 하는 것이 아니고, 선택성을 증가 시키거나 염료의 염색능력을 증가하여 현색시키는 물질 • 함께 사용하는 염색의 염색능을 높이는 역할을 하지만 염료와 lake를 만들지 못하며, 또 조직과도 화학적으로 결합하지 않는다. • methylene blue 용액에 포함되는 patassium hydroxide이나 carbol fuchsin에 들어가는 phenol 등
염료의분류 • 천연염료 (natural dyes) • Hematoxylin • Mexico의 Campeche 지방에서 자라는 logwood tree의 나무껍질에서 추출되는 연한 갈색 염료 • 염색할 때에는 염료 자체가 염색능력이 없고 자연산화나 화학적인 산화에 의해 hematein으로 전환되어야 염료로서의 기능인 염색능력을 갖게 되고 조직과의 친화력이 약하므로 염색 시 매염제와 결합시켜 사용 • 염색액을 제조 시 hematein으로 전환시켜 주어야 하며 염색용액 제조시 염색능력을 갖게 하는 과정을 숙성(ripening) 또는 산화시킨다고 한다. • 주로 핵염색에 이용
염료의분류 • 천연염료 (natural dyes) • Hematoxylin
염료의분류 • 천연염료 (natural dyes) • Indigo • 가장 오래된 염료로서 '염료의 제왕‘이라 하며, 남옥(indogofera)속의 식물로부터 얻어지는 푸른색 염료 • 근래에는 인공적으로 합성이 가능 • 생물학적으로 원형질과 광견병 환자의 신경세포 Negri 소체(Negri body)의 염색에 이용 • Cocchineal과 그 유도체 (Carmine) • 중남미 선인장에서 번식하는 연지벌레암컷의 체부를 건조시켜 추출된 cocchineal을 alum으로 처리하여 만든 양홍염료 • 당원, 점액질 등의 염색에 이용
염료의분류 • 천연염료 (natural dyes) • Orcein • 지의류(이끼식물) 식물인 Lecanora tinctoria와 Rocella tinctoria 속에 존재하는 lecanoric acid를 추출 처리 • 탄력섬유와 성염색질 소체 (sex chromatin body)의 증명과 B형 간염의 virus 봉입체(HBs Ag)를 증명할 때 사용 • Saffron • Crocus(Saffron속 붓꽃과의 일종)꽃에서 추출된 노란색의 천연염료 • alcohol 용해성이 있으며 세포질 및 원형질 염색에 이용
염료의분류 • 인공합성염료 (artifical dyes, synthetic dyes) • 산성염료 (acid dyes, anionic dyes) • 유색인 염기의 염(보통 sodium 염)으로 염료가 수용액에 해리되어 염료분자의 발색단과 조색단이 염료분자의 음이온 쪽에 위치 • Na+- (Chromogen + Auxochrome) - • alcohol보다 물에 녹기 쉽고 세포질과 같은 염기성을 띠는 세포 성분의 염색에 적합 • eosin Y, light green, erythrosine, picric acid, acid fuchsin 등 • OH, COOH, NO2 및 SO2OH 등의 원자기를 가지고, carboxylic acid 나 sulfurous acid의 sodium 염의 형을 가지고 있다.
염료의분류 • 인공합성염료 (artifical dyes, synthetic dyes) • 염기성 염료 (basic dyes, cationic dyes) • 유색인 염기의 염(보통 chloride, sulfate, acetate 염)으로 염료가 수용액에 해리되어 발색단과 조색단이 염료분자의 양이온 쪽에 위치 • (Chromogen + Auxochrome) + -Cl- • alcohol에 쉽게 녹고 수분에는 잘 녹지 않으며, NH2, NHCH3, N(CH3)2 및 NH 등의 원자기를 가진다. • 핵염색에 많이 이용 • basic fuchsin, methyl blue, methyl green, thionine, toluidine blue 등
염료의분류 • 인공합성염료 (artifical dyes, synthetic dyes) • 중성염료 (neutral dyes) • 한 염료분자 내에 두 종류의 발색단 (산성염료와 염기성염료)을 가지고 있어서 두 종류의 다른 색을 나타내는 유색염료 • 중성염색법을 최초로 개발한 사람은 러시아의 Romanowsky이며, 염료는 polychrome methylene blue와 eosin이 혼합된 형태로 혈구염색에 널리 사용 • 혈액학에서 사용되는 Wright 염색이나 Giemsa 염색, neutral red와 light green 혼합용액 등이 대표적인 중성염색법
염료의분류 • 인공합성염료 (artifical dyes, synthetic dyes) • 양성염료 (amphoteric dye, 혼합염색) • 염료분자가 양(+)으로 하전될 수 있는 기와 음으로 하전될 수 있는 기를 가진 염료 • 용액의 pH 상태에 따라 양이온성 염료 (염기성 염료) 또는 음이온성 염료 (산성염료)로 기능할 수 있는 염료 • carmine을 수순 정제한 carminic acid는 등전점이 약 pH 4.5인 양성염료로서, 용매가 알칼리인 경우 음(-)으로 하전되며, 산성인 경우 양(+)으로 하전
염료의분류 • Colour index Number (CIN) • Direct Fast Scarlet 4BS • 관칭 형용사 색상명 기호 • 염료의 명칭, 구조, 성질, 기타에 관하여 S.D.C (The Society of Dyers & Colourists. England)와 A.T.C.C (The American of Textile Chemists & Colourists. U.S.A)에서 공동 출판하고 있는 염료색인 (colour index)을 이용 • 동일한 염료는 회사명 (염료명)이 다르더라도 일련번호로 통일되어 있으며 C.I Name 혹은 C.I Number라고 한다.
염료의분류 • Colour index Number
염색의원리 • 물리적 염색작용 • 염료의 분산도와 농도 및 조직의 구성밀도 (pore size)가 중요 • 지방염색에 사용되는 수단염료(예> sudan Ⅲ)와 같은 무극성염료(indifferent dye)는 물리적인 과정 특히 그 분산력에 의해 지방 속으로 녹아 들어가는 것
염색의원리 • 물리적 염색작용 • 용해성 반응(solubility, absortion) • 조직 성분에 녹는 염료를 통상 용해성 염료 (lysochrome)라 부르며 그 대부분은 지용성 성질을 갖고 있어서 조직 내의 지질 증명시 빈번하게 사용 • 지방염색에서 염료인 oil red O 처럼 용매로 쓰이는 propylene glycol은 염료가 녹아 있는 상태에서 지방질을 접촉하면 용매에 녹을수 있는 한계보다 더 확산되어 용해되는 성질이 있고 이 과정에서 염색액 내의 색소가 용매보다 지방에 잘 녹아 색소가 이행되어 발색되는 성질을 이용
염색의원리 • 물리적 염색작용 • 흡착성 반응(absorption) • 큰 물질이 조그마한 일부분을 유인하여 끌어 붙이는 것으로, 염료의 일부분이 세포에 침전된 어떠한 물질(조직)에 침투되거나, 세포의 성분으로 화합되는 상태 • hematoxylin 용액은 alum이나 aluminium sulfate를 가하여 양(+)으로 대전한 염기성 색소로서 강하게 음(-)으로 대전한 핵이나 연골기질을 염색 • 용매의 수소 ion 농도(pH)에 따라 조직의 대전성이 변화하며, 염색성도 변화
염색의원리 • 물리적 염색작용 • 이염색성 반응, 변색성 염색(metachromasia) • 조직구성분 중 어떤 물질은 특정 염료와 결합할 때 원래 염료가 지닌 고유의 색과는 다르게 발색되어 그 주변에 염색된 다른 성분들과 구별되는 경우 • 조직의 점액(mucin) 성분은 toluidine blue 염료에 적색으로 염색되고 나머지 구성성분은 염료 자신의 색인 청색으로 염색 • 이런 특성의 염료를 변색성 또는 이염색성 염료라 하고, 변색성 염료의 색을 변화시키는 성분을 변색성물질또는 향색소라 한다.
염색의원리 • 물리적 염색작용 • 이염색성 반응, 변색성 염색(metachromasia) • 이염색성 조직성분 • 점액(sulfated mucopolysaccharide), 유전분, 연골(cartilage), 비만세포(mast cell) 과립, 핵산 복합체, hyaluronic acid • 이염색성 염료 • methylene blue, thionin, toluidin blue, bismark brown, safranin, crystal violet, methyl violet, azure • 이염색성 반응은 불안정하여 탈수제로 처리하면 잘 없어지므로 수용성 봉입제를 이용 • 염료가 조직에 친화력으로 인한 굴절률의 차가 발생하여 변색
염색의원리 • 화학적 염색작용 • 염료가 조직성분과 결합하기 위해서는 가장 흔한 결합방식으로 이온결합 (정전기적 결합), van der waals forces, 수소결합, 공유결합 (covalent bonding)이 관여 • 이온결합에 의한 염색 • 염료가 조직성분과 결합하여 불용성의 염(salt)을 형성 • 염료는 염색액 내에서 양이온 또는 음이온으로 이온화되어 단백질 및 기타 성분들과 결합하여 유색의 화합물을 형성 • 염기성 염료는 일정한 pH 범위내에서 양(+)으로, 산성염료는 음(-)으로 하전 • 양성염료는 염료의 등전점 이하의 pH에서는 양(+)으로 이상의 pH 에서는 음 (-)으로 하전
염색의원리 • 금속염의 주입법 (metalic impregnation) • 조직의 구성 성분과 세포 주위에 다량의 금속염(metal salt)이 침투되었을 경우, 염료가 가진 조염기성과 결합하여 불용성의 염을 만들고, 색조를 얻는 것 • 도은법에 의한 reticulum 염색은 ammonical silver 착염의 염색용액을 만들어 금속염에 도은(silvering)하여 조색하는 방법
염색 반응에 영향을 주는 요인 • 염색액의 이온강도 • 염색액 이온강도가 높을수록 특정 조직성분의 염색 강도는 증가 • 염료 및 염색액의 농도와 절편의 두께 • 염색액의 농도가 높을수록 염색반응이 강하나 염료가 결합할 수 있는 binding site의 수와 이미 결합된 염료분자의 수에 의해 제한 • 염색의 온도 • 온도의 상승은 염색용액의 확산력을 높이며, 단백질 구조 사이를 이완시켜 염료의 침투율을 증가
염색 반응에 영향을 주는 요인 • 조직화학성분과 염료가 반응하는 외부환경의 pH (염색액의 pH) • pH에 따라 조직화학성분과 염료의 이온화 경향에 영향이 있으며, 염색액의 pH는 염색결과에 큰 영향을 미친다. • 조직화학성분의 이온화의 양 • 조직의 고정 정도 • 고정액에 의한 단백질 구조의 변화는 화학적으로 염료가 조직에 염료 친화성이 있게 할 뿐만 아니라 조직성분의 투과성을 변화시켜 염료의 침투율을 증가 또는 감소시키기도 한다.
Application of staining • 생체염색(vital stain) • 살아있는 동물이나 세포에 시행하는 염색형식 • 탐식세포의 식작용 (phagocytosis)과 같은 세포의 기능을 확인하거나 세포질 내 특정 성분을 염색하는데 사용 • 이미 고정된 조질절편은 사용할 수 없다.
Application of staining • 생체염색(vital stain) • 종류 • 생체내 염색(intravital staining) • 생물체 내로 특수 염료를 주입한 다음 염색된 조직편을 절제한 후 표본을 제작하여 염색하는 방법 • 생체에는 무독성이며 주사용 멸균증류수에 용해된 교질상태의 용액 • trypan blue 및 trypan red 수용액과 india ink를 사용
Application of staining • 생체염색(vital stain) • 종류 • 초생체 염색(supravital staining) • 살아있는 세포를 분리하여 염색액 속에 넣어 염색하는 방법 • 염료의 조건은 모든 세포 및 조직에 침투할 수 있고, 세포내에 침투하여 세포를 죽이지 않고 원형질로 확산되어 세포내에 존재하는 특정 세포 포함물 (cell inclusions)에 착색되어야 할 뿐 아니라 세포의 주위나 세포들 사이에서 특이한 세포를 보다 뚜렷이 구별할 수 있는 강한 염착능을 보유 • methylene blue, Janus green B,neutral red
Application of staining to fixed tissue • 단순염색 (simple stain) • 염료를 단순히 물이나 alcohol에 용해시킨 염색액으로 조직성분의 염료에 대한 친화력의 차이를 이용한 가장 기본적인 염색법 • 동결박절법을 이용하여 표본을 제작할 때, 염기성 염료인 methylene blue를 단지 증류수에 용해하여 만든 0.2% 수용액으로 절편한 조직을 염색하여 핵은 청색으로, 염기성 염료에 친화력이 약한 세포질과 세포간의 물질 등은 옅은 색으로 나타나는 염색법
Application of staining to fixed tissue • 직접염색(direct staining) • 매염제(mordant)를 이용하지 않고 직접 조직의 특정성분을 염색 • 조직의 밀도가 염료의 흡수를 조절하는 중요한 요인 • congo red, sirius red 등
Application of staining to fixed tissue • 매염제 (mordants)를 이용한 염색 • 간접염색(indirect staining) • 염료와 매염제가 결합함으로써 염료의 색이 더 짙은 화합물, 즉 lake를 만들어 조직과 결합하면 조직-매염제-염료 복합체를 형성 • 매염 염료는 hematein, celestine blue B(mordant blue 14), alizaline red S(mordant red 13) 등
Application of staining to fixed tissue • 금속 침투법 • 금속염(salts of heavy metals)을 이용하는 염색 • 주로 질산은(AgNO3)을 많이 이용하는데, 질산은을 증류수에 용해하면 유리되는 은이온(silver ion, Ag+)을 염색과정에 이용 • 은이온을 이용하는 금속 침투법을 도은법(silver impregnation) • 도은법의 종류 • 호은성 반응(argyrophilic reaction) • 은환원성 반응(argentaffin reaction) • 유도성 은환원성 반응(induced argentaffin reaction)
Application of staining to fixed tissue • 금속 침투법 • 호은성 반응(argyrophilic reaction) • 암모니아성 은을 직접 환원시킬 수 없지만, 외부에서 developer를 첨가해 주면 환원이 되어 색상이 나타나게 하는 방법 • 세망섬유나 Helicobacter pylori검출 시 사용
Application of staining to fixed tissue • 금속 침투법 • 은환원성 반응(argentaffin reaction) • 조직 내에 어떤 성분은 은이온과 결합하면서 동시에 은이온을 환원시킬 수 있는 능력이 있어 발색을 하는 developer를 첨가할 필요가 없다. • 멜라닌과 같은 타이로신 유도체 등을 검출
Application of staining to fixed tissue • 금속 침투법 • 유도성 은환원성 반응(induced argentaffin reaction) • 조직성분을 인위적으로 은이온을 환원시킬 수 있는 상태로 전환시킨 다음 (산화를 하여 aldehyde 기를 유리) 은이온을 반응시키는 방법 • 진균이나 기저막의 검출에 사용되는 도은법
Application of staining to fixed tissue • 혼합염색 • 하나의 용액에 여러 종류의 염료를 혼합한 염색용액으로 조직을 염색 • 조직성분의 염료에 대한 친화력의 정도에 따라 각각 다른 색으로 구분되어 염색되는 형식 • van Gieson 염색용액이 대표적 • 하나의 염색용액에 산성염료인 picric acid와 acid fuchsin을 혼합하여 각각 근섬유와 아교섬유를 노란색과 적색으로 구분
Progression processing • 진행성 염색 (progressive staining) • 조직의 여러 구성성분을 정해진 순서에 따라 차례로 염색하고, 과염색된 부분을 수세로 제거하여 미세구조를 잘 관찰할 수 있도록 감별해 주는 염색 • 여러 시점에서 현미경으로 관찰해가면서 염색 정도를 판정하여 적당한 수준에서 그 과정을 정지시켜 수세하는 방법 • Mayer's hematoxylin 핵염색, Gill’s hematoxylin 핵염색
Progression processing • 진행성 염색 (progressive staining)
Progression processing • 퇴행성 염색 (regressive staining) • 섬세하고 예민한 염색결과를 필요로 할 때 사용하는 염색 형식 • 먼저 염색을 원하는 부분 뿐만 아니라 기타 다른 부분(원하지 않는 부분)까지도 과염색 (overstaining) 시킨 후에 과염된 염료를 감별(탈색)과정을 거쳐 불필요한 부분을 탈색 • 탈색(감별)이 지나치면 목적하는 부분까지도 과탈색되는 경향이 있으므로 반드시 현미경하에서 조절해가면서 수행하여야 좋은 결과를 얻을 수 있으며 특정 성분만을 정밀하게 염색해 낼 수 있다. • Harris' hematoxylin 핵염색
Progression processing • 퇴행성 염색 (regressive staining)
Progression processing • 감별(탈색 : differentiation, decoloration) • 퇴행성 염색방법을 사용하여 어떤 성분을 염색하려면 먼저 증명하고자 하는 물질 뿐만 아니라 모든 조직성분에 염색강도를 조절하여 염료를 완전히 포화시켜 염색한 후에 과잉의 염료를 제거(원하지 않는 부분에 염색된 염료를 제거)하여야 하는데 이 과정을 감별(탈색 혹은 분별)이라 한다. • 감별제로는 산성 용액, 염기성 용액, 고농도의 매염제가 포함된 용액, 완충액과 산화제 등
Progression processing • 감별(탈색 : differentiation, decoloration) • 산성용액, 염기성 용액 • 염기성 염료는 약산성 물질로 감별 • alum hematoxylin으로 염색한 것을 acid alcohol(1% HCl / 70% alcohol)로 감별 • 산성염료는 약염기 물질로 감별 • eosin이 과염된 것을 0.1% ~ 0.5% ammonia / 70% alcohol 용액으로 감별 • 산성 혹은 염기성 탈색제에는 물 대신 alcohol을 용매로 사용하고 있는데, 그 이유는 조직 염색에 사용되는 다수의 염료가 alcohol 보다는 물에 더 잘 용해되기 때문
Progression processing • 감별(탈색 : differentiation, decoloration) • 산성용액, 염기성 용액 • pH와 등전점 • 조직염색에서 산성염료, 염기성 염료의 분류는 등전점으로 분류하며, 단백질의 등전점 보다 pH가 낮으면 산성염료이다. • 핵의 등전점은 pH 1.5~2.0 이며 핵 염색제 hematoxylin은 pH 2.2~2.9로 염기성 염료 • 세포질의 등전점은 pH 5.5~6.0 이며 세포질 염색제 eosin은 pH 4.5 내외이므로 산성염료
Progression processing • 감별(탈색 : differentiation, decoloration) • 매염제 • 이온경쟁을 이용한 방법으로, 고농도의 매염제는 조직 주위에 과량의 매염제가 존재하면, 조직과 결합한 dye-mordant (염료-매염제)복합체를 파괴하여 염료가 과량의 매염제쪽으로 나오므로 조직에서 빠져 감별 • 탄력섬유의 증명에 이용되는 Verhoeff's elastic fiber 염색에서, hematoxylin의 매염제인 ferric chloride가 함유된 염색액을 사용
Progression processing • 감별(탈색 : differentiation, decoloration) • 완충액 • pH 6.0~6.5 인산완충액은 혈액도말표본에 사용하는 wright‘s 염색의 탈색제로 이용 • 인산완충액의 pH는 methylene blue와 eosin의 최대 염색범위의 pH에 대하여 중간에 위치하게 되어 methylene blue에 대해서는 산성 탈색제로, eosin에 대해서는 염기성 탈색제로 작용 • 산화제 • 산성 alcohol 용액의 pH를 이용하는 것과 ferricyanide, bisulfate, permanganate 등과 같은 산화제를 이용