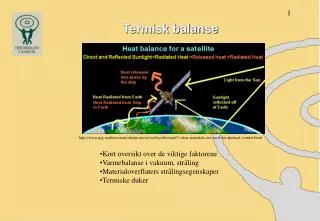
Termisk Energi
Termisk Energi . Energi SI-enhed: joule Findes ved brug af formlen E=P/t - Energisætningen: ”Den samlede mængde energi er konstant i et isoleret system” . Formler For Energi . Effekt: SI enheden er Watt

Termisk Energi
E N D
Presentation Transcript
Termisk Energi Energi SI-enhed: joule Findes ved brug af formlen E=P/t - Energisætningen: ”Den samlede mængde energi er konstant i et isoleret system”
Formler For Energi • Effekt: • SI enheden er Watt • Kan findes ved brug af samme formlen som for energi E=P/t, men bliver omskrevet til P=E*t • Varmefylde: - Den mængde energi der skal til at varme 1 kg af stoffet 1 grad - Formel: J/kg*°C - Den energi der tilføjes: E=c*m*∆
Opvarmning Et stofs temperatur afgør hvor meget molekylerne i stoffet bevæger sig det absolutter nulpunkt er 273,15°C, ved den temperatur står molekylerne helt stille. Stoffer kan have tre forskellige tilstandsformer afhængig af temperaturen: Fast: Stoffets molekylerne i en fast gitterstruktur. Molekylerne bevæger sig lidt frem og tilbage. Flydende: Stoffets molekyler bevæger sig frit rundt mellem hinanden men bliver stadig holdt sammen af kræfter. Gasform: Molekylerne bevæger sig helt frit rundt mellem hinanden med langt større kraft end ved flydende.
Formler ved opvarmning • Ved opvarmning af et stof bruges formlen • E=c*m*∆t, • Ved formlen kan man udregne hvor meget energi der bliver brugt ved at gange stoffets varmefylde(c) med massen(m) og tilvæksten i temperaturen(∆t) ex. • E=4186J/g°C*180g*20°C; E=15069600 joule • Varmefylde: 4186 (vand) J/1g*1°C • Massen: vi har taget 180 gram vand • Tilvækst i temperatur: vandets temp. øges med 20°C
Faseovergang - Når et stof fra en tilstand til en anden kaldes det faseovergang fx. fra fast til flydende. - Ved faseovergang kan formlen for opvarmning (E=c*m*∆t) ikke bruges: hvis vores stof er is (vand i fast form) så er temperaturen uforandret indtil alt isen er smeltet til vand (se dias nr. 6). - I stedet for bruges formel: Ls=∆E/m eller Lf=∆E/m (Smeltevarmen (Ls)= tilvækst i energi (J)/massen (g) ) Den tilførte energi (Ls) pr. masse for at smelte/fordampe et stof (ex. fra is til vand) kalder vi: smeltevarme=Lseller fordampningsvarme=Lf
Graf over temperaturstigning og faseovergange (fast-flydende-gas). x-aksen: Den brugte energi (joule) til opvarmning af vandet y-aksen: Temperaturen i °C Opvarmning af vand