Elektrolyse von Wasser
340 likes | 1.47k Views
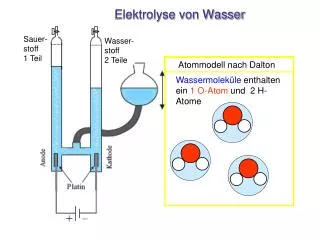
Elektrolyse von Wasser. Sauer- stoff 1 Teil. Wasser-stoff 2 Teile. Teilchenmodell. Atommodell nach Dalton. Wassermoleküle enthalten ein 1 O-Atom und 2 H-Atome. Wasserteilchen. Nichtmetall + Nichtmetall → Molekularverbindung

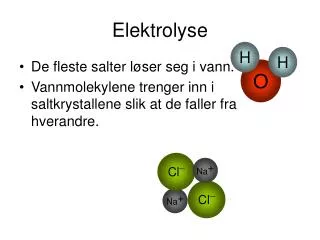
Elektrolyse von Wasser
E N D
Presentation Transcript
Elektrolyse von Wasser Sauer-stoff1 Teil Wasser-stoff2 Teile Teilchenmodell Atommodell nach Dalton Wassermoleküle enthaltenein 1 O-Atom und 2 H-Atome Wasserteilchen
Nichtmetall + Nichtmetall → Molekularverbindung Metall + Nichtmetall → Salz (Metall + Metall → Legierung)
Gold-Atome(Gitterstruktur) Sauerstoff-MoleküleO2 Alkohol-Moleküle(C2H6O) Helium-AtomeHe Ammoniak-Moleküle(NH3) Verbindungen Elemente Salze Molekularverbindungen Wasser-Moleküle(H2O) EisensulfidFeS (Gitter) Natriumchlorid (Kochsalz)NaCl (Gitter)
Gib an, ob es sich um Salze oder um Molekularverbindungen handelt: C2H6O NaCl CuSO4 CH3COCH3MV Salz Salz MV Alkohol Natriumchlorid Kupfersulfat Aceton Kochsalz Nagellackentferner CaCO3 NH3 CaSO4 CH4 NaHCO3 Salz MV Salz MV Salz Kalk Ammoniak Gips Methan Backpulver Erdgas MV: Molekularverbindung
Modell zur Atommassenbestimmung am leichtesten am schwersten
Edukte Produkte + 2 H2 NH3 3 N2 + Kontrolle 2 N 2 N 6 H 6 H 2 N, 6 H, 2 N, 6 H
Edukte Produkte + 6 Cl2 N2 HCl 3 + 2 NH3 + + Kontrolle 2 N 2 N 6 H 6 H 6 Cl 6 Cl 2 N, 6 H, 6 Cl 2 N, 6 H, 6 Cl
Edukte Produkte + 2 CH4 O2 CO2 H2O 2 + + + Kontrolle 1 C 1 C 4 H 4 H 4 O 2 O 2 O 1 C, 4 H, 4 O 1 C, 4 H, 4 O
Edukte Produkte + 2 CH4 O2 CO2 H2O 2 + + + • Verbrennung von organischen Verbindungen mit C, H und O • Reaktion mit Sauerstoff (O2) • Produkte Kohlenstoffdioxid (CO2) und Wasser (H2O) Benzin (C8H18)Alkohol (C2H6O)Haushaltzucker (C12H22O11)Fett (C18H36O2)
Salze • 1. 2 Fe + 3 Cl2 2 FeCl3 • 2. 2 Mg + O2 2 MgO • 3. 4 Al + 3 O2 2 Al2O3 • 4. 2 Al + 6 HCl 2 AlCl3 + 3 H2 • 5. Cu2S + 2 Cu2O 6 Cu + SO2 • 6. 2 WC + 5 O2 2 WO3 + 2 CO2 • 7. 2 NaN3 2 Na + 3 N2 • P4 + 5 O22 P2O5 Reaktionsgleichungen
9. CH4 + 2 O2 CO2 + 2 H2O 10. C6H12O6 + 6 O2 6 CO2 + 6 H2O 11. NH3 + 3 F2 NF3 + 3 HF 12. I2O5 + 5 CO I2 + 5 CO2 13. 3 Fe + 4 H2O Fe3O4 + 4 H2 14. B2O3 + 3 C + 3 Cl2 2 BCl3 + 3 CO 15. B2H6 + 6 H2O 2 H3BO3 + 6 H2 16. 3 NO2 + H2O 2 HNO3 + NO Reaktionsgleichungen
Berechnung der Anzahl Teilchen N: Anzahl Teilchenm: Gesamtmasse (auf der Waage bestimmen)mT: Masse eines Teilchens (im PSE nachschauen) Umrechnungsfaktor u → g 1 u = 1.66 ∙10–24 g (Tabelle physikalische Konstanten)
Das Zählen von Teilchen in der Chemie 1 mol enthält 6.02∙1023 Teilchen (Atome, Moleküle) 1 Dutzend enthält 12 Teilchen (Eier) Avogadro-Konstante: NA = 6.02∙1023 / mol (Tabelle physikalische Konstanten)
Treibhauseffekt durch fossile Brennstoffe C8H18 + 12½ O2 8 CO2 + 9 H2O Infrarotlangwellig H2O CO2 CO2 CO2 Ultraviolettkurzwellig