SPETTROSCOPIA
SPETTROSCOPIA. Materiale tratto da: Progetto Lauree Scientifiche 2009 Dipartimento di Fisica Università degli studi Perugia.

SPETTROSCOPIA
E N D
Presentation Transcript
SPETTROSCOPIA Materiale tratto da: Progetto Lauree Scientifiche 2009 Dipartimento di Fisica Università degli studi Perugia
La misura e lo studio di uno spettro è chiamato spettroscopia. In origine uno spettro era la gamma di colori che si osserva quando della luce bianca viene dispersa per mezzo di un prisma. Con la scoperta della natura ondulatoria della luce, il termine spettro venne riferito all'intensità della luce in funzione della lunghezza d'onda o della frequenza. Oggi il termine spettro è stato generalizzato ulteriormente, ed è riferito a un flusso o un'intensità di radiazione elettromagnetica o particelle (atomi, molecole o altro) in funzione della loro energia, lunghezza d'onda, frequenza o massa. Uno strumento che permette di misurare uno spettro viene chiamato spettrometro, spettrografo o spettrofotometro. Quest'ultimo termine si riferisce ad uno strumento per la misura dello spettro elettromagnetico. fonte wikipedia
IL DUALISMO ONDA-PARTICELLA Alcuni fenomeni fisici possono essere spiegati assumendo che la luce sia costituita da onde. Altri fenomeni vengono spiegati accettando che la luce sia costituita da particelle discrete (i FOTONI), ciascuna dotata di una energia E legata alla frequenza della radiazione dalla relazione di Einstein del 1905: E = hn Costante di Planck Nel 1924 Louis de Broglie ipotizzò che TUTTA la materia avesse proprietà ondulatorie: ad un corpo con quantità di moto p veniva infatti associata un'onda di lunghezza d'onda λ. Tre anni dopo i fisici Davisson e Germer confermarono le previsioni della formula di De Broglie del 1924: l = h/p
LA LUCE La luce visibile è formata dalle onde elettromagnetiche, vibrazioni di campi magnetici ed elettrici che si propagano nello spazio. Le onde elettromagnetiche viaggiano alla velocità della luce: 300.000.000 metri al secondo, 1.080.000.000 chilometri l'ora! Ogni onda elettromagnetica ha una frequenza (n) definita ed una lunghezza d'onda (l) associata a questa frequenza; queste due grandezze sono legate dalla relazione di De Broglie: l = c/n Velocità della luce ~ 3×108 m/s (una costante)
LA LUCE p. 401 Con il termine radiazione s’intende normalmente ogni forma di energia che si propaga mediante onde o particelle in moto (luce, suono, raggi cosmici, radioattività, ecc.). Le radiazioni utilizzate in spettroscopia per perturbare la materia, e quindi ottenere informazioni sull'analita di interesse, sono prevalentemente onde elettromagnetiche. La radiazione elettromagnetica èuna forma di energia trasmessa attraverso lo spazio ad enorme velocità. Molte delle proprietà delle radiazioni elettromagnetiche sono convenientemente descritte trattando le radiazioni come onde sinusoidali caratterizzate da lunghezza d'onda, , frequenza, , velocità, c, e ampiezza, A. Diversamente da altri fenomeni ondulatori (per es. le onde sonore), la radiazione elettro-magnetica non richiede alcun mezzo di supporto per propagarsi nello spazio, pertanto si propaga velocemente anche nel vuoto. 6
LA LUCE In realtà…. Il modello ondulatorio falliscenel rendere conto di fenomeni associati con l'assorbimento e l'emissione di energia radiante. Per questi processi, la radiazione elettromagnetica deve essere trattata come una corrente di particelle discrete o pacchetti d'onda chiamati fotoni o quanti. L'energia di un fotone è proporzionale alla frequenza della radiazione. Questi due aspetti della radiazione, la natura ondulatoria e quella corpuscolare sono complementari. 7
LA LUCE L'ampiezza A dell'onda sinusoidale è definita come la lunghezza del vettore elettrico al massimo dell'onda. Il tempo richiesto per il passaggio di massimi (o minimi) successivi attraverso un punto fisso nello spazio è chiamato periodo p della radiazione. La frequenza è il numero di oscillazioni del campo per secondo ed è uguale ad 1/p. È importante tenere presente che la frequenza è determinata dalla sorgente e rimane costante indipendentemente dal mezzo attraversato dalla radiazione. Di contro, la velocità di propagazione, vi del fronte d'onda attraverso un mezzo è dipendente sia dal mezzo che dalla frequenza; il pedice i è impiegato per indicare questa dipendenza dalla frequenza. La lunghezza d'onda i è la distanza lineare fra massimi o minimi successivi di un'onda. Il prodotto della frequenza in onde per secondo per la lunghezza d'onda in centimetri dà la velocità vi di propagazione in centimetri per secondo vi = .i La velocità con la quale le radiazioni elettromagnetiche si propagano nel vuoto, c, è indipendente dalla lunghezza d'onda ed è massima: c = 2,99792 1010 cm/s. La velocità nell'aria differisce solo leggermente da c (è circa lo 0,03% in meno). Nel vuoto o nell'aria la velocità della luce è convenientemente arrotondata a 3.00 1010 cm/s = 3,00 108 m/s . 8
LA LUCE In un mezzo contenente materia, la radiazione si propaga ad una velocità minore di c perché il campo elettromagnetico della radiazione, interagendo con gli elettroni degli atomi o molecole del mezzo, si propaga meno rapidamente. Dal momento che la frequenza della radiazione è invariante ed è fissata dalla sorgente, la lunghezza d'onda della radiazione deve diminuire nel passare dal vuoto ad un mezzo contenente materia vi = .i Il numero d'onda, è definito come il numero di onde per centimetro, ed è uguale a 1/. Per definizione, ha le unità di cm-1. La potenza, P,è l'energia di radiazione che raggiunge una data area per secondo. L'intensità, I, è la potenza per unità di angolo solido. Sebbene non sia strettamente corretto, potenza e intensità sono frequentemente usate indifferentemente. Le proprietà particellari possono essere riassunte nella relazione Ad ogni fotone può quindi essere associata l’energia E. 9
Riportiamo qui un esempio di spettro continuo nel visibile (luce) spettro di emissione discreto dell'idrogeno atomico eccitato da scarica elettrica spettro solare di assorbimentodiscreto con varie righe da vari atomi Per questa ragione gli spettri di assorbimento e di emissione atomici sono “a righe”: in un atomo ci possono essere più salti energetici, ma ad ogni salto è associata una precisa radiazione, con una precisa frequenza (e lunghezza d’onda)
Le molecole sono costituite da più atomi e da più elettroni, e quindi rappresentano dei sistemi più complicati: anche le molecole possono assorbire radiazione elettromagnetica, e possono passare a stati eccitati (fare dei salti energetici). E1 E1 hn E0 E0 molecola* molecola = elettrone generico Ecco un esempio del processo di assorbimento per una molecola generica: hn Molecola Molecola* Anche per le molecole, affinchè avvenga una transizione energetica, occorre utilizzare radiazione con una precisa frequenza (n)
CENNI STORICI • MODELLO DI THOMSON: • - spiega la stabilità dell’atomo • - si rivela inadeguato dopo l’esperimento di Rutherford. • MODELLO DI RUTHERFORD: • - giustifica le osservazioni dell’esperimento di Rutherford • - non spiega la stabilità dell’atomo • Entrambi i modelli sono quindi inadeguati. • SPETTRI DI EMISSIONE A RIGHE: • - vengono emessi da gas ionizzati, e non sono continui; nessuno dei due modelli atomici esistenti all’inizio del Novecento riesce a spiegarli.
L’INNOVAZIONE DI BOHR Bohr propoSe un nuovo modello, esso si basa su alcuni postulati: 1°) All’elettrone sono consentite solamente alcune orbite, nelle quali esso non perde energia. L’energia associata a ciascuna orbita è data dalla formula: È così possibile capire che i livelli più interni (quelli con n basso), in uno stesso atomo, sono quelli a energia minore.
2°) Ogni elettrone può acquisire energia, e “saltare” ad un livello ad energia maggiore, quindi più esterno, per poi tornare spontaneamente nella propria orbita, cedendo la stessa quantità di energia assorbita (sotto forma di radiazione elettromagnetica, quindi di luce, che può essere osservata). L’energia da fornire all’elettrone per promuoverlo ad un livello superiore è data dalla formula: per passare, per esempio, dal 1° al 2° livello.
L’elettrone eccitato tende a tornare allo stato fondamentale, liberando l’energia sotto forma di onde elettromagnetiche di lunghezza: L’emissione di onde elettromagnetiche può quindi avvenire solo a determinate lunghezze d’onda
SELEZIONE DELLA LUNGHEZZA D’ONDA Gli spettrofotometri sono equipaggiati con uno o più dispositivi per selezionare una stretta banda, assorbita o emessa dall'analita (banda passante). Una banda passante stretta aumenta la probabilità che lo strumento risponda linearmente alla concentrazione di analita. I due tipi principali di selettori di lunghezza d'onda sono i monocromatori ed i filtri. I monocromatori hanno il vantaggio che la lunghezza d'onda in uscita può essere variata continuamente in un intervallo spettrale considerevole. I filtri offrono il vantaggio di semplicità, robustezza e basso costo. I monocromatori dei moderni spettrofotometri sono prismi e, principalmente, reticoli.
PRISMA Un prisma è un oggetto in grado di disperdere la luce bianca nelle sue componenti monocromatiche Con il “cerchio di Newton” è possibile “miscelare” le componenti monocromatiche ed ottenere la loro somma, il bianco rotazione
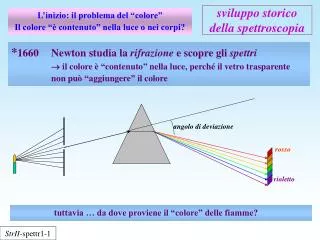
PRISMA L’indice di rifrazionedi un mezzo dipende dal colore della luce, cioè dalla sua lunghezza d’onda. La deviazione di un raggio luminoso in seguito a rifrazione è diversa per ciascuna delle singole componenti monocromatiche che lo costituiscono. Indice di rifrazione n funzione decrescente di Dispersione(cromatismo per rifrazione) = separazione della luce nelle sue componenti monocromatiche A e B costanti caratteristiche della sostanza rifrangente • La deviazione cresce andando dal rosso al viola
PRISMA Gli angoli i ed r tra i raggi e la normale sono definiti di incidenza e di rifrazione. Dato che n2 dipende dalla lunghezza d’onda, nella rifrazione la luce bianca incidente si separa nelle sue componenti colorate. La radiazione rossa è la meno deviata, la violetta è la più deviata. 26
SPETTROGRAFO A PRISMA Idrogeno Ferro l
RETICOLO Diffrazione da una fenditura
RETICOLO Diffrazione da una fenditura
RETICOLO Doppia fenditura http://hyperphysics.phy-astr.gsu.edu/hbase/phyopt/grating.html
EQUAZIONE DEL RETICOLO Lunghezza d’onda Angolo di diffrazione ml=d sinq Ordine Costante del reticolo
Ordine 0 -1 0 1