补充内容二 热分析技术 Thermal Analysis
补充内容二 热分析技术 Thermal Analysis. 1. 一 概述. 1 、热分析的起源. 1887 年,法(德)国人第一次用 热电偶测温的方法研究粘土矿物 在升温过程中的热性质的变化。 1891 年,英国人使用示差热电偶和参比物,记录样品与参照物间存在的温度差,大大提高了测定灵敏度,发明了 差热分析( DTA ) 技术的原始模型。 1915 年,日本人在分析天平的基础上研制出热天平,开创了 热重分析 (TG) 技术。 1940-1960 年,热分析向自动化、定量化、微型化方向发展。

补充内容二 热分析技术 Thermal Analysis
E N D
Presentation Transcript
一 概述 1、热分析的起源 • 1887年,法(德)国人第一次用热电偶测温的方法研究粘土矿物在升温过程中的热性质的变化。 • 1891年,英国人使用示差热电偶和参比物,记录样品与参照物间存在的温度差,大大提高了测定灵敏度,发明了差热分析(DTA)技术的原始模型。 • 1915年,日本人在分析天平的基础上研制出热天平,开创了热重分析(TG)技术。 • 1940-1960年,热分析向自动化、定量化、微型化方向发展。 • 1964年,美国人在DTA技术的基础上发明了示差扫描量热法(DSC), Perkin-Elmer公司率先研制了DSC-1型示差扫描量热仪。
2、定义 国际热分析协会(International Confederation for Thermal Analysis---ICTA) 曾于1977年对热分析技术下了如下定义: 热分析是在程序控制温度下测量物质的物理性质与温度关系的一类技术。 指物质的质量、温度、热量、尺寸、机械特征、声学特征、光学特征、电学特征及磁学特征的任何一种 指线性升温、线性降温、恒温等 指试样本身,也可指试样的反应产物 热分析法的核心就是研究物质在受热或冷却时产生的物理和化学的变迁速率、温度以及所涉及的能量和质量变化。 3
3、特点: 1.温度的变化是受程序控制的; 2.能很简便地测定因温度变化而引起材料物性改变的方法。 4、应用 测量和分析材料在温度变化过程中的物理变化(晶型转变、相态变化和吸附等)和化学变化(脱水、分解、氧化和还原等)。 4
5、分类 9类17种 国际热分析协会确认的热分析技术 (ICTA) 热分析的四大支柱 5
最常用的三种热分析法 1热重分析法TG (Thermo-gravimetry) (微商热重分析法 DTG (Derivative Thermogravimetry ) 2 差热分析法 DTA(Differential Thermal Analysis) 3示差扫描量热分析法DSC (Differential Scanning Calorimetry) 6
二、热重法 (Thermo-gravimetry,TG) 1.定义 在程序控温下,测量物质的质量与温度或时间的关系的方法,通常是测量试样的质量变化与温度的关系。 控温方法:升温法、恒温法 升温法:动态法 • 在程序升温下,测定物质质量变化与温度的关系。 恒温法:静态法 • 在恒温条件下,试样质量变化随时间变化的函数关系 7
2.仪器 基本结构由精密天平、加热炉及温控单元组成。 STA 449C热分析仪
3. 基本原理 天平 高温炉 温控单元 热电偶 基本原理:待测物置于耐高温容器中,此容器被置于一具有可程式控制温度的高温炉中,上端被悬挂在一个具有高灵敏度及精确度的天平上。在加热或冷却的过程中,由于待测物会因为反应导致重量的变化,这个因温度变化造成的重量变化可以由天平测量获得。 9
4. 热重分析曲线 • TG曲线: • DTG曲线: 一次微分
4.1、热重曲线(TG曲线): 质量变化对温度的关系曲线 纵坐标:重量---由上到下质量减少 横坐标:温度或时间---从左到右增加 • 热重曲线中,水平部分表示重量恒定,曲线斜率发生变化的部分表示重量的变化 • 根据热重曲线上各步失重量可以简便地计算出各步的失重分数,从而判断试样的热分解机理和各步的分解产物。 • 还可看出热稳定性温度区,反应区,反应所产生的中间体和最终产物。
例:固体热分解反应:A(固)→B(固)+C(气)的典型热重曲线如图所示例:固体热分解反应:A(固)→B(固)+C(气)的典型热重曲线如图所示 失重百分数为: (W0-W1)/W0×100% W0 W1
4.2、微商热重曲线(DTG曲线): 试样质量变化率与温度或时间的关系曲线。 纵坐标:dW/dt(或dW/dT)---从上到下减少 横坐标:温度或时间---自左至右增加 15
DTG • DTG曲线的峰顶d2W/dt2 = 0,即失重速率的最大值,它与TG曲线的拐点相对应。 • DTG曲线上的峰的数目和TG曲线的台阶数相等 • DTG曲线上的峰面积与失重量成正比。 TG
5.影响热重曲线的因素 1.实验条件的影响: ⑴ 样品盘的影响 ⑵ 挥发物冷凝的影响 ⑶ 升温速率的影响 ⑷ 气氛的影响 2.样品的影响: ⑴ 样品用量的影响 ⑵ 样品粒度的影响 加热屏板解决 升温速率越大,热滞后越严重,导致起始温度和终止温度偏高 CO2气氛、空气或N2气氛,物质的反应温度会有较大变化 最好的办法是根据天平的灵敏度,尽可能使用少量试样。用量大:吸放热引起的温度偏差大,且不利于热扩散和热传递。 粒度小的比粒度大的试样热分解温度低,反应区间窄。 17
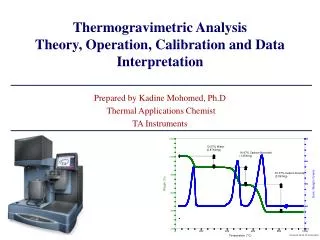
CuSO4·5H2O的TG曲线 6. 热重分析应用举例 CuSO4·5H2O的热分解行为研究 实验条件为试样质量为:10.8 mg, 升温速率为10 ℃/min, 采用静态空气,在铝坩埚中进行 曲线AB段为一平台,表示试样在室温至45℃间无失重。故mo=10.8 mg。 曲线BC为第一台阶,失重为mo-m1=1.55 mg,求得质量损失率为: 曲线CD 段又是一平台,相应质量为m1; 曲线DE 为第二台阶,质量损失为1.6 mg,求得质量损失率:
曲线EF段也是一平台,相应质量为m2; 曲线FG 为第三台阶,质量损失为0.8 mg,可求得质量损失率 可以推导出CuSO4·5H2O 的脱水方程如下:
验证: 根据方程,可计算出CuSO4·5H2O 的理论质量损失率。计算结果表明第一次理论质量损失率为 第二次理论质量损失率也是14.4%;第三次质量损失率为7.2%;固体剩余质量理论计算值为63.9%,总失水量为36.1%。理论计算的质量损失率和TG 测得值基本一致。 14.4% 14.4% 7.2%
三 差热分析(Differential Thermal Analysis,DTA) 1、概念 是在程序控制温度下测量物质与参比物之间温度差与环境温度关系的一种技术。 2、基本原理 背景知识:试样发生任何物理或化学变化,都会释放或吸收的热量使试样温度发生变化。 如相转变、熔化、结晶、升华等 氧化还原反应、断裂与分解反应、脱氢反应、晶格破坏时以及其他化学反应等 21
把被测试样和参比物置放在同样的热条件下进行加热或冷却,记录试样在某一特定温度下发生物理化学反应引起热效应的变化,得到差热曲线,即DTA曲线。把被测试样和参比物置放在同样的热条件下进行加热或冷却,记录试样在某一特定温度下发生物理化学反应引起热效应的变化,得到差热曲线,即DTA曲线。 参比物应是惰性材料,即在测定的温度范围内,不产生任何热效应(放热、吸热)的材料,如:α-A12O3、α-石英、硅油等。 22
T 向下表示吸热过程向上表示放热过程 + A 3DTA曲线 纵坐标:温差(T) 横坐标:温度T(或时间t) 0 - 差热仪炉子供给的热流为Q 试样无热效应时: QS QR TS = TR ΔT = 0 试样吸热效应时:(Q-g)S QRTS<TR ΔT<0 峰向下 试样放热效应时:(Q+g)S QR TS>TR ΔT>0 峰向上 基线—— T近于零(图中的AB、DE段); 峰——BCD; 峰宽—— B’D’; 峰高—— CF; 峰面积——BCDB; 外推起始点(出峰点)一峰前沿最大斜率点与基线延长线的交点(G) 23
T + 0 - 若试样不发生热效应,在理想情况下,试样温度和参比物温度相等,T=0,差示热电偶无信号输出,记录仪上记录温差的笔仅划一条直线(即基线)。 T/oC 24
4、差热分析仪的组成 加热炉 温差检测器 温度程序控制仪 信号放大器 记录仪 气氛控制设备 25
热电偶 热电偶是差热分析的关键元件 • 铜-康铜(长期350℃ /短期500 ℃ )、 • 铁-康铜(600/800 ℃ ) • 镍铬-镍铝(1000/1300℃ )、 • 铂-铂铑(1300/1600 ℃ )、 铱-铱铑(1800/>2000 ℃)
测量池 热电偶 样品 参比物 电热丝 金属 经典测量池 易受试样、参比物的密度、导热系数、比热容、热扩散的影响
程序温控装置: 使炉温按给定的程序方式(升温、降温、恒温、循环)以一定速度变化 升温速度:1~100K/min,常用:1~20K/min • 微伏放大器: 灵敏、稳定;< 10 uV 用以放大温差电势差,热信号须经放大后再送入记录仪中记录 • 记录仪:多笔记录仪 • 气氛控制系统:Ar;N2
5. DTA曲线提供的信息 峰的数目:表示物质发生物理、化学变化的次数 峰的方向:表明体系发生热效应的正负性 峰面积:说明热效应的大小 注意:两种或多种不相互反应的物质的混合物,其差热曲线为各自差热曲线的叠加。 30
定性分析 差热分析中产生吸热、放热的物理化学反应
6、差热分析曲线的影响因素 影响差热分析的主要因素有三个方面: (一)实验条件的影响 1.升温速率 2.气氛-不同性质的气氛如氧化气氛,还原气氛或惰性气氛对DTA 测定有较大影响。 3. 参比物用量、比重、粒度、比热及热传导性等都应与试样尽可能一致,否则可能出现基线偏移、甚至造成缓慢变化的假峰。 常用的参比物: α- Al2O3 不同升温速率对高岭土脱水反应DTA曲线的影响
(二)试样 1 试样的用量:试样用量多,热效应大,峰顶温度滞后,容易掩盖邻近小峰谷。以少为原则,通常10~30 mg。 2. 样品粒度:较大的颗粒峰形较宽,分辨率下降。一般以200目为宜。 3. 样品的装填:装填不均会引起导热及温度的差异,出现无法解析的小峰。 (三)仪器因素 仪器中加热方式、炉子形状、尺寸的影响 样品支持器(均温块体的结构和材质) 热电偶的位置,热电偶的类型、尺寸的影响
6、差热分析的应用 (1)推测材料的分解过程 例1.从热分析曲线推测NH4VO3的分解过程 在所示温度范围内发生了两次热分解反应,并且都为吸热反应。 两次热分解反应对应的热失重量分别为14%和22%,并由此推测两次热分解反应的产物中都有气相的逸出从而使重量减轻。 34
NH4VO3的分子量为117: 第一次热失重的失去重量为14%,对应的分子量约为16.4,相当于NH3的分子量,即失去氨气后剩余HVO3; 第二次热失重反应后累计失去的重量为22%,减去第一次热反应所失去的量还有8%,即等于分子量9.4,相当于H2O的一半。这样,完整的热分解反应方程式为: -NH3 -1/2 H2O NH4VO3--------HVO3--------------V2O5 35
(2)材料的鉴别与成分分析 • 应用差热分析对材料进行鉴别主要是根据物质的相变(包括熔融、升华和晶型转变等)和化学反应(包括脱水、分解和氧化还原等)所产生的特征吸热或放热峰。 • 有些材料常具有比较复杂的DTA曲线,虽然不能对DTA曲线上所有的峰作出解释,但是它们象“指纹”一样表征着材料的特性。 36
(3)材料相态结构的变化 • 检测非晶态的分相最直接的方法是通过电镜观察,但电镜分析比较复杂,从制样到分析需要的周期比较长,而用DTA不仅制样简单,而且方便快速。 39
(3) 凝胶材料的烧结进程研究 DTA TG 41
四、示差扫描量热法 (DSC,(Differential Scaning Calarmeutry) • DTA面临的问题 定性分析,灵敏度不高 1、DSC定义是在程序控制温度下,保持试样与参比物之间温度始终相同,测量输给试样和参比物的能量差随温度或时间变化的一种技术。 优势:试样和参比间无温差、无热传递,使热损失小,检测信号大。灵敏度和精度大有提高,可进行定量分析。
2、测量方法分类及其工作原理 热流式示差扫描量热法 功率补偿式示差扫描量热法 在给予样品和参比品相同的功率下,测定样品和参比品两端的温差T,然后根据热流方程,将T(温差)换算成Q(热量差)作为信号的输出。 在样品和参比品始终保持相同温度的条件下,测定满足此条件样品和参比品两端所需的能量差,并直接作为信号Q(热量差)输出。 差示扫描量热法可以直接测量样品在发生物理或化学变化时的热效应。
3、典型的DSC曲线 以热流率(dH/dt)为纵坐标、以时间(t)或温度(T)为横坐标,即dH/dt-t(或T)曲线。 峰或谷包围的面积:代表热量的变化
4、DSC与DTA的区别 样品和参比物各自独力加热 产生温差用功率补偿,保持同温 分析曲线与DTA相同,但更准确 示差量热计代替加热炉
CuSO4·5H2O的DSC和DTA曲线比较 DTA DSC DSC与DTA曲线相同,但更准确
5、示差扫描量热分析法的影响因素 (一)实验条件的影响 ⑴升温速率 程序升温速率主要影响DSC曲线的峰温和峰形。 ⑵气体性质 (二)试样特性的影响 ⑴试样用量 ⑵试样粒度 ⑶试样的几何形状
试样 标样 基线 6、示差扫描量热分析的应用 (二)样品比热的测定 H = mcT (一)样品焓变的测定 • 目前测定比热容大部分用DSC。具体作法是: • 用DSC仪先放两个空坩埚用一定的升温速率作一条基线; • 再用同样条件,在试样坩埚中放蓝宝石标准样,作一条DSC曲线; • 把蓝宝石取出来在同一个坩埚中放入称量好的未知试样,用同样的操作条件再作一条DSC曲线,把这三条线画到一起,如图。利用上式可计算比热。
(三)纯度测定 根据熔点或凝固点下降来确定杂质总含量的,基本原理是以Van’t Hoff(凡特何夫)方程式为依据: Tm为杂质样品的熔点(K); T0为纯样品的熔点(K); R为气体常数; ΔHf为样品熔融热; x2为杂质摩尔数; 图纯度对苯甲酸熔融峰的影响