Modelos atómicos
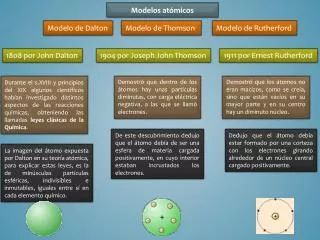
Modelos atómicos. Modelo de Dalton. Modelo d e Thomson. Modelo de Rutherford. 1808 por John Dalton. 1904 por Joseph John Thomson. 1911 por Ernest Rutherford.

Modelos atómicos
E N D
Presentation Transcript
Modelos atómicos Modelo de Dalton Modelo de Thomson Modelo de Rutherford 1808 por John Dalton 1904 por Joseph John Thomson 1911 porErnest Rutherford Demostró que dentro de los átomos hay unas partículas diminutas, con carga eléctrica negativa, a las que se llamó electrones. Demostró que los átomos no eran macizos, como se creía, sino que están vacíos en su mayor parte y en su centro hay un diminuto núcleo. Durante el s.XVIII y principios del XIX algunos científicos habían investigado distintos aspectos de las reacciones químicas, obteniendo las llamadas leyes clásicas de la Química. De este descubrimiento dedujo que el átomo debía de ser una esfera de materia cargada positivamente, en cuyo interior estaban incrustados los electrones. Dedujo que el átomo debía estar formado por una corteza con los electrones girando alrededor de un núcleo central cargado positivamente. La imagen del átomo expuesta por Dalton en su teoría atómica, para explicar estas leyes, es la de minúsculas partículas esféricas, indivisibles e inmutables, iguales entre sí en cada elemento químico.
Modelos atómicos Modelo de Dalton Modelo de Thomson Modelo de Rutherford La materia está formada por minúsculas partículas indivisibles llamadas átomos. Hay distintas clases de átomos que se distinguen por su masa y sus propiedades. Todos los átomos de un elemento poseen las mismas propiedades químicas. Los átomos de elementos distintos tienen propiedades diferentes. Los compuestos se forman al combinarse los átomos de dos o más elementos en proporciones fijas y sencillas. De modo que en un compuesto los de átomos de cada tipo están en una relación de números enteros o fracciones sencillas. En las reacciones químicas, los átomos se intercambian de una a otra sustancia, pero ningún átomo de un elemento desaparece ni se transforma en un átomo de otro elemento. La identificación por J.J. Thomson de unas partículas subatómicas cargadas negativamente, los electrones, a través del estudio de los rayos catódicos, y su posterior caracterización, le llevaron a proponer un modelo de átomo que explicara dichos resultados experimentales. Se trata del modelo conocido informalmente como el pudín de ciruelas, según el cual los electrones eran como 'ciruelas' negativas incrustadas en un 'pudín' de materia positiva. Rutherford estableció el llamado modelo atómico de Rutherford o núclear. El átomo está formado por dos partes: núcleo y corteza. El núcleo es la parte central, de tamaño muy pequeño, donde se encuentra toda la carga positiva y, prácticamente, toda la masa del átomo. Esta carga positiva del núcleo, en la experiencia de la lámina de oro, es la responsable de la desviación de las partículas alfa (también con carga positiva). La corteza es casi un espacio vacío. Aquí se encuentran los electrones con masa muy pequeña y carga negativa. Como en un diminuto sistema solar, los electrones giran alrededor del núcleo, igual que los planetas alrededor del Sol. Los electrones están ligados al núcleo por la atracción eléctrica entre cargas de signo contrario.
Modelos atómicos Modelo de Bohr Modelo de Sommerfeld Modelo de Schrödinger 1913 por Niels Bohr 1913 porArnoldSommerfeld 1924 porErwin Schrödinger Sommerfeld había encontrado que en ciertos átomos las velocidades de los electrones alcanzaban una fracción apreciable de la velocidad de la luz. Sommerfeld estudió la cuestión para electrones relativistas. El modelo de Bohr funcionaba muy bien para el átomo de hidrógeno. En los espectros realizados para otros átomos se observaba que electrones de un mismo nivel energético tenían energías ligeramente diferentes. Espectros atómicos discontinuos originados por la radiación emitida por los átomos excitados de los elementos en estado gaseoso. Los electrones giran en órbitas circulares alrededor del núcleo, ocupando la órbita de menor energía posible, o la órbita más cercana posible al núcleo. Predice líneas de emisión espectrales, de átomos neutros yde átomos ionizados. El modelo también predice la modificación de los niveles energéticos cuando existe un campo magnético o eléctrico. En el modelo de Bohr los electrones sólo giraban en órbitas circulares. La excentricidad de la órbita dio lugar a un nuevo número cuántico: el número cuántico azimutal, que determina la forma de los orbitales.
Modelos atómicos Modelo de Bohr Modelo de Sommerfeld Modelo de Schrödinger Los electrones describen órbitas circulares en torno al núcleo del átomo sin radiar energía. No todas las órbitas para electrón están permitidas, tan solo se puede encontrar en órbitas cuyo radio cumpla que el momento angular del electrón sea un múltiplo entero de El electrón solo emite o absorbe energía en los saltos de una órbita permitida a otra. En dicho cambio emite o absorbe un fotón cuya energía es la diferencia de energía entre ambos niveles. Este fotón, según la ley de Planck tiene una energía calculable a partir de una ecuación. Los electrones se mueven alrededor del núcleo en órbitas circulares o elípticas. A partir del segundo nivel energético existen dos o más subniveles en el mismo nivel. El electrón es una corriente eléctrica minúscula. El modelo de Schrödinger en su formulación original no tiene en cuenta el espín de los electrones, esta deficiencia es corregida por el modelo de Schrödinger-Pauli. El modelo de Schrödinger ignora los efectos relativistas de los electrones rápidos, esta deficiencia es corregida por la ecuación de Dirac que además incorpora la descripción del espín electrónico. El modelo de Schrödinger si bien predice razonablemente bien los niveles energéticos, por sí mismo no explica porqué un electrón en un estado cuántico excitado decae hacia un nivel inferior si existe alguno libre. Esto fue explicado por primera vez por la electrodinámica cuántica y es un efecto de la energía del punto cero del vacío cuántico.