Ομοιοπολικός δεσμός – Κβαντομηχανική Θεώρηση – Θεωρία Δεσμού Σθένους – σ και π δεσμοί
Lio. Ομοιοπολικός δεσμός – Κβαντομηχανική Θεώρηση – Θεωρία Δεσμού Σθένους – σ και π δεσμοί. Λιόντος Ιωάννης - Χημικός. • Ομοιοπολικός δεσμός • Κβαντομηχανική Θεώρηση • Θεωρία Δεσμού Σθένους. Lio. Δημιουργήθηκε από τον Linus Pauling προσπαθώντας να δώσει εξήγηση

Ομοιοπολικός δεσμός – Κβαντομηχανική Θεώρηση – Θεωρία Δεσμού Σθένους – σ και π δεσμοί
E N D
Presentation Transcript
Lio Ομοιοπολικός δεσμός – Κβαντομηχανική Θεώρηση – Θεωρία Δεσμού Σθένους– σ και π δεσμοί Λιόντος Ιωάννης - Χημικός Ιαν 2010
• Ομοιοπολικός δεσμός • Κβαντομηχανική Θεώρηση• Θεωρία Δεσμού Σθένους Lio Δημιουργήθηκε από τον Linus Pauling προσπαθώντας να δώσει εξήγηση για το πότε, πως και γιατί σχηματίζεται ένας δεσμός. Η θεωρία δεσμού σθένους περιγράφει το σχηματισμό ομοιοπολικού δεσμού σαν το αποτέλεσμα της αλληλεπίδρασης ή επικάλυψης των ατομικών τροχιακών (Orbital’s overlap) των ατόμων που συμμετέχουν στο χημικό δεσμό. Ιαν 2010
Οι βασικές αρχές της θεωρίας δεσμού - σθένους Lio • Η ανάπτυξη ομοιοπολικού δεσμού ανάμεσα σε 2 άτομα, επιτυγχάνεται όταν ατομικά τροχιακά σθένους του ενός ατόμου επικαλύπτουν ατομικά τροχιακά σθένους του άλλου ατόμου. • Αν στο κάθε ατομικό τροχιακό που συμμετέχει στον μηχανισμό αυτό της επικάλυψης περιέχεται ένα μονήρες ηλεκτρόνιο, τότε ηλεκτρόνια με αντι-παράλληλο spin δημιουργούν κοινά ζεύγη ηλεκτρονίων που ανήκουν και στα 2 άτομα. Η έλξη του ζεύγους ηλεκτρονίων από τους πυρήνες και των 2 ατόμων οδηγεί στην ανάπτυξη του δεσμού ανάμεσά τους. • Όσο μεγαλύτερος είναι ο βαθμός επικάλυψης των ατομικών τροχιακών τόσο ισχυρότεροςείναι ο ομοιοπολικός δεσμός. Υπάρχουν 2 είδη δεσμών :ο σ- και ο π- δεσμός Ιαν 2010
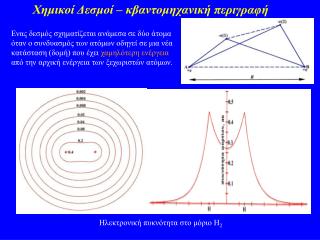
Ενέργεια του συστήματος Η – Η σε συνάρτηση με την απόσταση των πυρήνων των δύο ατόμων υδρογόνου Lio Μήκος δεσμού:είναι η απόσταση ανάμεσα στους δύο πυρήνες, στην οποία επιτυγχάνεται η ελάχιστη ενέργεια, άρα κι η μέγιστη σταθερότητα του μορίου Ιαν 2010
σ – δεσμός Lio 1. Δημιουργείται με μετωπική επικάλυψηs – s , s – p , p – p ατομικών τροχιακών κατά τον άξονα που συνδέει τους πυρήνες των 2 ατόμων. 2. Προκαλείται η μέγιστη δυνατή επικάλυψη, άρα και η μέγιστη ισχύς δεσμού. Είναι ισχυρότερος από τον π- δεσμό. 3. Η πυκνότητα του ηλεκτρονιακού νέφους είναι μέγιστη στον χώρο ανάμεσα στους 2 πυρήνες και το ηλεκτρονιακό νέφος έχει κυλινδρική συμμετρία. 4. Είναι ο πρώτος δεσμός που δημιουργείται ανάμεσα σε 2 άτομα (δηλαδή ανάμεσα σε 2 άτομα μπορεί να υπάρχει μόνο σ- δεσμός : Όλοι οι απλοί δεσμοί είναι σ- δεσμοί). 5. Επιτρέπεται η ελεύθερη περιστροφή γύρω από τον άξονά του. Ιαν 2010
σ- δεσμοί Lio σ – δεσμοί (s – p) και (p – p) σ – δεσμός (1s – 1s) στο μόριο του Η2 Ιαν 2010
σ – δεσμοί Lio Η δημιουργία του σ – δεσμού στο μόριο του H2 Μετωπική επικάλυψη 1s – 1s ατομικών τροχιακών. Η Η Η Η e e 1s 1s H2 : σ-δεσμός Ιαν 2010
Lio Θεμελιώδης ηλεκτρονιακή κατάσταση των 2 ατόμων H : 1H : 1s1 1H : 1s1 σ - δεσμός Ερμηνεία της μοριακής δόμησης του Η2 με βάση τη θεωρία δεσμού σθένους. Ιαν 2010
σ – δεσμοί Lio Η δημιουργία του σ – δεσμού Η – Ο Mετωπική επικάλυψη 1s – 2pατομικών τροχιακών Ο Η Η Ο e e 1s 2p Η – Ο : σ – δεσμός Ιαν 2010
Σχηματισμός σ- δεσμού στο HF Lio + Γίνεται μετωπική επικάλυψη του 1sατομικού τροχιακού του ατόμου του Hμε το 2pατομικό τροχιακό του ατόμου του F Οπότε δημιουργείται ένας σ - δεσμός Ιαν 2010
Θεμελιώδης ηλεκτρονιακή δομή των ατόμων του Η και του F Lio 1Η : 1s1 9F : 1s2, 2s2 2p5 σ - δεσμός Ερμηνεία της μοριακής δόμησης του HF με βάση τη θεωρία δεσμού σθένους. Ιαν 2010
σ – δεσμοί Lio Η δημιουργία του σ – δεσμού Ο – Ο(ο απλός δεσμός) Mετωπική επικάλυψη 2p – 2pατομικών τροχιακών Ο O O Ο e e 2p 2p Ο – Ο : σ – δεσμός Ιαν 2010
Θεμελιώδης ηλεκτρονιακή δομή των 2 ατόμων του F Lio 9F : 1s2, 2s2 2p5 9F : 1s2, 2s2 2p5 σ- δεσμός Ερμηνεία της μοριακής δόμησης του F2 με βάση τη θεωρία δεσμού σθένους Ιαν 2010
Lio Θεμελιώδης ηλεκτρονιακή δομή των ατόμων του Η και του S 1Η : 1s1 16S : 1s2, 2s2 2p8 ,3s23p4 Δύο σ- δεσμοί 3pψ (S) – 1s (H) και 3pz (S) – 1s (H) Ερμηνεία της μοριακής δόμησης του H2S με βάση τη θεωρία δεσμού σθένους. Ιαν 2010
σ-δεσμοί με επικάλυψη Lio s – s ατoμικών τροχιακών s – p ατoμικών τροχιακών Ιαν 2010
Lio σ-δεσμόςμε μετωπική επικάλυψη p – p ατομικών τροχιακών Ιαν 2010
π – δεσμός Lio 1. Δημιουργείται με πλευρική επικάλυψη μόνο p – p ατομικών τροχιακών (με παράλληλους άξονες). 2. Δεν επιτυγχάνεται η μέγιστη δυνατή επικάλυψη, άρα ο π- δεσμός είναι ασθενέστερος από τον σ- δεσμό. 3. Η πυκνότητα του ηλεκτρονιακού νέφους είναι μηδέν στον χώρο ανάμεσα στους 2 πυρήνες και μέγιστη εκατέρωθεν του άξονα που συνδέει τους 2 πυρήνες. 4. Δημιουργείται μόνο εφόσον προηγηθεί η δημιουργία του σ- δεσμού (π-δεσμοί υπάρχουν μόνο στον διπλό και στον τριπλό δεσμό) . 5. Δεν επιτρέπεται η ελεύθερη περιστροφή γύρω από τον άξονά του. Ιαν 2010
π – δεσμός Lio Η δημιουργία του π – δεσμού στο μόριο του Ο2 Πλευρική επικάλυψη 2p – 2p ατομικών τροχιακών. O O O – Ο : π – δεσμός 2p 2p Ιαν 2010
π- δεσμός Lio pψ pψ + Πλευρική επικάλυψη p – p ατομικών τροχιακών Δημιουργία π – δεσμού Ιαν 2010
Η επικάλυψη ενός p τροχιακού με ένα p τροχιακό, με παράλληλους άξονες, οδηγεί στο σχηματισμό ενός π δεσμού. Lio Ιαν 2010
Ηλεκτρονική πυκνότητα στους σ – και π – δεσμούς Lio σ - δεσμός π - δεσμός ηλεκτρονική πυκνότητα συμμετρικά κατανεμημένη κατά μήκος του άξονα του δεσμού ηλεκτρονική πυκνότητα συγκεντρωμένηεκατέρωθεν του άξονα του δεσμού Ιαν 2010
Η δημιουργία του διπλού δεσμού στο μόριο του Ο2 Lio p – τροχιακά Ο Ο π - δεσμός σ - δεσμός Δημιουργούνται :1 σ- δεσμός με μετωπική επικάλυψη 2pz – 2pz ατομικών τροχιακών1 π- δεσμός με πλευρική επικάλυψη 2px– 2pxατομικών τροχιακών Ιαν 2010
Η δημιουργία του τριπλού δεσμού στο μόριο του Ν2 Lio Δημιουργούνται :1 σ- δεσμός με μετωπική επικάλυψη 2pz – 2pz ατομικών τροχιακών2 π- δεσμοί με πλευρική επικάλυψη 2px– 2px και 2pψ – 2pψ Ιαν 2010
Τ έ λ ο ς Lio Λιόντος Ιωάννης - Χημικός Ιαν 2010