PROJETOS GENOMA E PROTEOMA HUMANOS
420 likes | 776 Views
PROJETOS GENOMA E PROTEOMA HUMANOS. Haline Reis de Oliveira 07/33091 Nathália de Vargas Haar 07/50751. Genética Básica. O que é genoma ?. “É o conjunto de todo material genético que define um ser vivo”. Como seqüenciar o DNA. Subdivisão em fragmentos menores.

PROJETOS GENOMA E PROTEOMA HUMANOS
E N D
Presentation Transcript
PROJETOS GENOMA E PROTEOMA HUMANOS Haline Reis de Oliveira 07/33091 Nathália de Vargas Haar 07/50751 Genética Básica
O que é genoma? “É o conjunto de todo material genético que define um ser vivo”
Como seqüenciar o DNA Subdivisão em fragmentos menores Amplificação- clonagem MÉTODO DE SANGER – técnica de seqüenciamento por terminação de cadeia
Projeto Genoma Humano Participantes: Alemanha, Austrália, Brasil, Canadá, China, Coréia, Dinamarca, Estados Unidos, França, Holanda, Israel, Itália, Japão, México, Reino Unido, Rússia, Suécia, União Européia e grandes centros de seqüenciamento Objetivos: • 3 bilhões de pares de bases • 100.000 genes • bancos de dados. • melhorar as ferramentas de análise de dados. • tecnologia para o setor privado • questões éticas, legais e sociais
PGH x Celera Departamento de Energia dos Estados Unidos Celera Genomics Corporation National Institute of Health (NIH) Investimento privado US$300 milhões Investimento governamental Robotização- menor custo US$ 3 bilhões Indústria farmacêutica Interesse acadêmico Royalties
Método Projeto Genoma Humano Seqüenciamento direcionado 4 5 2 1 6 3 2 4 6 1 1 3 5
Método Celera Shotgun 1 2 3 4 5 6 7 8 9 9 6 3 1 7 1 2 3 4 5 6 7 8 9 2 5 8 4
Marcos: 1990: início do projeto em um esforço conjunto do Depto de Energia e do Instituto Nacional de Saúde dos EUA. Junho de 2000: término do rascunho de todo o genoma humano. Abril de 2003: o seqüenciamento de todo o genoma humano é completado e o projeto é declarado finalizado dois anos antes da data prevista
O que o PGH nos informa? • O genoma humano contém cerca de 3 bilhões de pares de nucleotídios. • O tamanho médio médio de um gene é cerca de 3.000 pares de nucleotídios, mas a variação é muito grande; o maior gene humano é o da distrofina, com 2,4 milhões de pares de nucleotídios. • O número de genes no genoma humano está entre 20.000 e 25.000. • A seqüência de nucleotídios é muito semelhante (99,9%) entre todas as pessoas.
A função de 50% dos genes humanos descobertos é totalmente desconhecida. • Menos do que 2% do genoma humano codifica proteínas. • Seqüências repetitivas que não codificam proteínas (DNA lixo) constituem pelo menos 50% do genoma humano. • As seqüências repetitivas parecem não desempenhar nenhuma função direta, mas elas podem ter papel na dinâmica estrutural dos cromossomos. De tempos em tempos, essas seqüências possibilitam rearranjos do genoma, criando genes novos e modificando outros.
O genoma humano possui regiões onde se concentram genes e regiões muito pobres em genes • As regiões onde se concentram os genes possuem blocos ricos nas bases C e G, enquanto as regiões pobres em genes possuem blocos ricos nas bases A e T. • A região rica em genes parecem se concentrar aleatoriamente no genoma, separados por longas seqüências de DNA não-codificante. • O cromossomo 1 é o que contém o maior número de genes (2.968), e o cromossomo Y, o menor (231).
O que ainda não sabemos... • O número de genes, suas localizações exatas e suas funções • Como os genes são regulados • Detalhes da estrutura dos cromossomos e da organização dos genes • Os tipos de DNA não-codificante, sua quantidade, sua distribuição, se contêm algum tipo de informação e suas funções • Como as células coordenam a expressão dos genes, a síntese das proteínas e os eventos pós-tradução • A interação das proteínas nas complexas maquinarias celulares • Explicar a conservação evolutiva entre as espécies • O proteoma, ou seja, o conjunto total de proteínas e suas funções • A correlação entre as diferenças genéticas entre as pessoas com a saúde e com as doenças • Predizer a susceptibilidade a doenças com base na variação da seqüência gênica • Os genes envolvidos em traços complexos e doenças multigênicas • O controle genético do desenvolvimento
Projeto Genoma no Brasil Projeto Xylella - 1°patógeno de planta seqüenciado Projeto Genoma da cana-de-açúcar Bactéria Xilella fastidiosa Projeto Genoma da bactéria Xanthomonas citri Projeto Genoma do Câncer Humano Xanthomonas citri
Por muitos anos a genômica funcional propagou a noção de que não seria necessário estudar níveis de proteínas para obter-se dados de “up and down regulation”. Tudo o que era necessário seria a determinação dos níveis de mRNA Em 1997, Anderson apresentou um trabalho mostrando a primeira comparação da abundância de mRNA e proteínas correspondentes. A correlação foi de 0,43… Anderson &Seihamer (1997) Electrophoresis 18, 533-537 Esses resultados vem sendo confirmados por outros grupos. A proteômica, portanto, parece ser a ferramenta mais apropriada para entender-se o funcionamento dos genes, pois analisa o produto final do genoma
O que significa ? Proteoma significa o conjunto de proteínas expressas a partir de um determinado genoma. Separar e visualizar simultaneamente o máximo de proteínas possível do proteoma de uma amostra, permitindo que depois sejam identificadas e catalogadas Quais são seus objetivos? Como é a separação do proteoma? Atualmente, uma técnica chamada eletroforese bidimensional é o método mais eficiente de separação de proteínas. Hoje em dia, ela é considerada o “coração” da análise de proteomas pois esta talvez seja a etapa menos automatizada e que exija mais habilidade do pesquisador.
Eletroforese bidimensional É uma técnica na qual uma mistura de moléculas que possuam cargas elétricas (como é o caso das proteínas) são aplicadas em um tipo de gel e, em seguida, submetidas a um campo elétrico. Deste modo, as proteínas que tiverem carga negativa migrarão em direção ao pólo positivo e as de carga positiva migrarão para o negativo. Proteínas de cargas e tamanhos diferentes migrarão no gel com velocidades diferentes; quanto maior a carga e menor o tamanho, maior será sua velocidade. Após a eletroforese, o gel pode ser corado e cada tipo de proteína será visualizada como uma mancha colorida
Através desta técnica as proteínas são submetidas a dois processos consecutivos (dimensões) de separação baseados com duas propriedades diferentes das proteínas: 1)Focalização isoelétrica: as proteínas migram em um gel especial até atingirem uma posição estacionária onde possuem carga zero(ponto isoelétrico). Com carga zero, as proteínas não podem se mover e, então, diz-se que estão focalizadas. Como cada proteína tem seu ponto isoelétrico específico, o gel possuíra manchas em diferentes posições ao final da focalização, cada uma correspondendo a um tipo de proteína. Cada mancha não contém apenas uma molécula de proteína e sim milhões de moléculas do mesmo tipo de proteína.
2)Massa molecular : o gel da primeira dimensão é submetido a um segundo tipo de eletroforese de modo que as proteínas focalizadas sejam separadas pelo seu tamanho(massa molecular). As proteínas presentes o gel podem então ser coradas e visualizadas, permitindo que, ao final do processo, mais de 5000 manchas de proteínas possam ser observadas em um único gel bidimensional.
Aparelho utilizado na eletroforese bidimensional- focalização isoelétrica
O comportamento de diferentes proteínas durante a focalização
Eletroforese em gel bidimensional das proteínas de E. coli -mais de 2,000 proteínas podem ser visualizadas
Como ocorre a identificação das proteínas ? A seqüência de aminoácidos é o que dá a identidade da proteína. Para a análise de proteomas não é necessário sequenciar completamente cada proteína a fim de identificá-las. Um pedaço de seqüência juntamente com dados fornecidos pelo próprio gel bidimensional(massa molecular e ponto isoelétrico) são muitas vezes, suficientes para isso. A identificação da proteína é muito facilitada se sua seqüência completa for conhecida e já estiver depositada em bancos de dados de seqüências (já existem mais de um milhão de seqüências depositadas) , os quais podem ser acessados via internet.
Como pode-se obter a seqüência completa de uma proteína? • Sequenciando diretamente os aminoácidos da proteína • Sequenciando o DNA e, a partir daí, deduzindo a seqüência das proteínas utilizando o código genético, é muito mais rápido que o de proteínas, portanto a maior parte das sequencias de bancos de dados foi obtida desta forma.
Como identificar proteínas do proteoma? • Seqüenciador automático de proteínas:programas computacionais de busca fariam uma comparação da seqüência VLSPADKTD com a seqüência de todas as proteínas nos bancos de dados seqüência de aminoácidos V • Espectrometria de massa: o espectrômetro de massa agiria como se fosse um balança molecular. A metodologia utilizada é denominada de peptide mass fingerprinting ( impressão digital por massas de peptídeos) . - Quebra de proteínas em locais bem específicos, para formar peptídeos. A massa desses peptídeos são então determinadas no espectrômetro de massa com incrível precisão, elas formam uma espécie de impressão digital. Cada proteína é composta de peptídeos de massas moleculares definidas. - A seguir programas computacionais tomam as mais de um milhão de seqüências de proteínas depositadas nos bancos de dados e as quebram teoricamente com a protease. Então para cada proteína do banco de dados é obtido um conjunto de números que correspondem ás massas dos peptídeos produzidos teoricamente.
- Cada um desses conjuntos é comparado com os dados experimentais e, se a seqüência da proteína-problema estiver no banco de dados, ela é imediatamente identificada através dessa comparação. Com os dados de identificação de proteínas são preparados então os chamados mapas de proteoma. Apesar da enorme quantidade de trabalho proteômico, continuamos observando a ponta do iceberg. A grande maioria das proteínas proteínas raras (e preciosas) ainda estão escondidas. Todos estão identificando as mesmas proteínas (as mais abundantes)
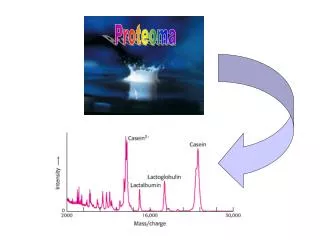
Afinal para que servem os mapas de proteomas? Permite que pesquisadores possam identificar mais facilmente as proteínas que foram afetadas em fenômenos biológicos envolvendo diferenças na expressão de proteínas, tais como efeito de fármacos, condições patológicas, diferenciação celular, comparação de variedades da mesma espécie e outros assuntos.
Mapa proteômico do fluido cérebro-espinhal –de um indivíduo sem patologia
Mapa proteômico do fluido cérebro-espinhal –de um indivíduo com patologia
Um Projeto Proteoma Humano? Um projeto Proteoma Humano ainda não existe oficialmente, entretanto os avanços que estão ocorrendo são inegáveis, empresas já começam a lançar equipamentos que automatizam quase totalmente a separação de proteínas por eletroforese bidimensional, mas dificuldades ainda existem. Por exemplo, como seria possível definir um proteoma humano, já que, para cada tipo de célula e para cada condição do organismo, o conjunto de dados seria diferente.
Proteoma no mundo • A Era pós-genômica que se inicia vem recebendo apoio de países como EUA, Dinamarca, Suíça, Suécia, França, Alemanha, Inglaterra, Japão e Austrália. Empresas como Large Scale Biology, Oxford Glycosciences e a Protana prestam consultorias para empresas farmacêuticas.
No Brasil... • Centro Brasileiro de Serviços e Pesquisas em Proteínas(CBSP) da UnB, que foram pioneiros na utilização de tecnologia proteômica desde 1995. Pesquisadores na UnB realizaram o primeiro sequenciamento completo dos aminoácidos uma proteína . • Hoje se estuda proteomas de neutrófilos humanos, de venenos de aranha e serpentes, além do proteoma do Trypanossoma cruzi. • Pesquisas na Unicamp envolvendo a análise de proteoma da Xilella fastidiosa, o mesmo microorganismo no qual se realizou o mapeamento completo do genoma no país.
Confirmação de diagnósticos Auxilio para escolha de tratamento apropriado Resultados positivos podem ser apresentados por pessoas que nunca desenvolverão a doença Geração de ansiedade desnecessária Riscos para produção de discriminação e estigmatização sociais Questão éticasTestes de DNA
Privacidade genética • Quem, como, quando, onde e por que os dados de DNA poderão ser utilizados e divulgados? No Brasil, o assunto ainda não entrou em pauta para discussão nas agendas do Governo Nacional ou no Congresso Federal. Nos EUA, não há nenhuma lei federal que regulamente o assunto, mas leis anteriores relacionadas a deficientes físicos e planos de saúde possam ser interpretadas para incluir discriminação genética.
Terapia gênica É uma nova abordagem para tratar, curar ou prevenir doenças através da interferência na atividade de um gene em um indivíduo. • Dificuldades... -dos 100000 genes estimados, a função de poucos é conhecida, e tentar terapia gênica sem ter o quadro geral das inter-relações de genes em uma doença pode dirigir o tratamento a apenas alguns dos genes implicados; -severas regulamentações na maioria dos países dificultam a realização de experimentos com seres humanos; -alto custo para desenvolvimento de tecnologia de terapia gênica ;
Patenteamento de genes • Como se protege o trabalho e o investimento de um pesquisador e uma empresa que trabalham nesse novo campo de análises genômicas e proteômicas? • É lícito patentear um genoma, um proteoma, um gene ou uma proteína? • Há limites éticos para tais práticas? A favor...os recursos das patentes são convertidos em novas pesquisas, duplicação desnecessária de esforços é evitada,a concessão de monopólio encoraja investimentos privado ou público, segredos são reduzidos e a informação fica mais disponível. Contra... O desenvolvimento de métodos diagnósticos seria impedido por terceiros devido aos custos na obtenção da licença e no pagamento dos royalties,empresas de biotecnologia que possuírem as patentes poderão controlar mercados monopolizados.
Farmacogenômica • Estuda o efeito da herança genética individual sobre a ação de drogas, combina conhecimentos farmacológicos e farmacêuticos tradicionais com os novos conhecimentos de genoma e proteoma. • Será responsável por terapias mais voltadas a constituição genética de cada paciente