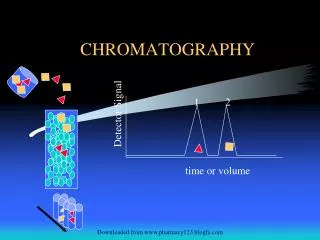
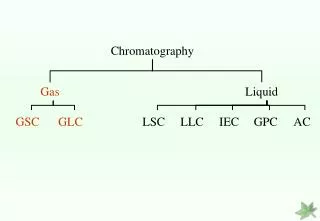
Chromatography
Chromatography. 1.1 Beginning 1.2 Separation Process 1.3 Plate Theory 1.4 Rate Theory 1.5 정성 분석 1.6 정량 분석. 1.1 Beginning. Chromatography 하나이상의 용질( Solute) 과 두 상( Phase) 간의 상호작용을 포함하는 Separation process 이동상( Mobile phase) 컬럼을 통과해서 지나가는 기체 또는 액체 고정상( Stationary phase)

Chromatography
E N D
Presentation Transcript
Chromatography 1.1 Beginning 1.2 Separation Process 1.3 Plate Theory 1.4 Rate Theory 1.5 정성 분석 1.6 정량 분석
1.1 Beginning • Chromatography • 하나이상의 용질(Solute) 과 두 상(Phase)간의 상호작용을 포함하는 Separation process • 이동상(Mobile phase) • 컬럼을 통과해서 지나가는 기체또는 액체 • 고정상(Stationary phase) • 이동하지 않는 고체 또는 액체 * The University of Akron의 분석화학 교재 참고함. 1. Chromatography
1.1 Beginning • Chromatography • Chromatography : color + to write • Tswett 이 1906년에 처음으로 기술함 • CaCO3로 채워진 튜브를 이용하여 식물 색소를 분리하는 방법을 고안함. • 식물 추출물을 넣고 유기용매로 컬럼을 통해 추출물을 씻어낸 후에 여러 색깔을 띤 띠를 만들어 냄. 1. Chromatography
1.1 Beginning • 분리과정 (Separation Process) • 시료 성분들이 고정상 위로 이동상에 의해 운반된다. • 각 성분들은 다음과 같은 고정상과의 다양한 상호작용에 의해 흐름을 방해 받는다. • Surface adsorption (표면 흡착 작용) • Relative solubility (상대적인 용해도) • Charge (전하) 1. Chromatography
1.1 Beginning • 분리 유형 (Types of Separation) • Frontal Analysis • 컬럼의 시작부분에 지속적으로 시료를 주입한다. • 각 성분들이 전개되는 과정을 관찰한다. • 성분들이 얼마나 흐름을 방해 받는 지에 대한 일반적인 관찰을 볼 수 있다. • 예 : 활성탄 여과 1. Chromatography
1.1 Beginning • Frontal Analysis • 이 방법은 상대적인 Retention time을 측정하기 위해 사용될 수 있다. • 하지만 분리를 위해 유용한 방법은 아니다. 1. Chromatography
1.1 Beginning • Displacement analysis (치환분석) • 물질이 더 많이 방해 받는 용질 과 치환되며 컬럼을 타고 내려간다. • 예 : Ion exchange / Water softener • 완전하게 분리할 수 없으며, 컬럼의 길이를 늘리는 것도 아무런 효과가 없다. 1. Chromatography
1.1 Beginning • Elution (용리) • 용질이 두 상 사이에서 분배한다.(equilibrium) • 분리는 상대적인 Retention에 기초한다. • 컬럼을 길게 하는 것은 분리도를 증가시킨다. • 여러 가지의 경쟁적인 친화력이 사용된다. • 예: GLC에서의 Vapor pressure(증기압) vs. 고정상에 대한 용질의 용해도 1. Chromatography
1.1 Beginning • Theory • 분리 과정을 설명하기 위한 두 가지 이론이 있다. • Plate theory • 1941 – Martin & Synge • 증류(distillation)와 역류 추출(counter current extraction)의 유추에 기초함 • Rate theory • 1956 – van Deemter • 분리의 동력학에 대한 설명 1. Chromatography
1.2 Plate Theory • Plate Theory • 크로마토그라피 컬럼을 평형상태에서의 Static System(움직임이 없는)으로 간주 • 각 성분은 이동상과 고정상 사이에서 평형 상태로 존재한다. 1. Chromatography
1.2 Plate Theory • Plate Theory • 이 평형상태에 기초한 분배계수(Partition coefficient) 가 정의된다. • K 는 농도에 독립적인 것으로 가정한다. 이것은 온도와 같은 Factor에 의해 바뀔 수 있다. • K 가 증가하면 용질이 컬럼을 통과하는데 더 많은 시간이 걸린다. 1. Chromatography
1.2 Plate Theory • Plate Theory • 분리에 있어서 다음과 같은 가정이 주어진다. • 컬럼의 길이는 고정되어 있다. • Flow는 일정하다. • 표준 시료들이 보여주는 것에 기초한 몇가지 용어가 정의 될 수 있다. • 첫번째 측정해야 할 것은 용질이 컬럼을 통과하는데에 걸리는 시간을 측정하는 것이다. 1. Chromatography
1.2 Plate Theory • Retention time & Volume • Retention Volume, VR–컬럼으로부터 최대의 용질을 추출하기 위해 필요한 이동상의 부피 • Retention Time, tR–일정한 Flow에서 최대 농도에 이르기까지 걸리는 시간 • VR = tR Ⅹ flow rate 1. Chromatography
1.2 Plate Theory • Plate Theory • 용질에 대한 평균 직선 속도는 다음과 같다. • v = L / tR • 이동상 에 대한 평균 직선 속도는 다음과 같다. • u = L / tR • 이것은 간단하게 상호작용이 없는 물질들이 컬럼을 통과하기 위해 필요한 시간이다. 1. Chromatography
1.2 Plate Theory • Plate Theory • v = u Ⅹ f • F는 용질이 이동상에서 소비하는 시간의 비율이다. • f = n soluteM / n solutes • (이동상의 용질의 수/ 고정상의 용질의 수) • 이동상과 고정상의 Volume(VM, VS)을 모두 알고 있기 때문에 이제 분배계수(partition coefficient) K를 구할 수 있다. 1. Chromatography
1.2 Plate Theory • Plate Theory • 첫째 줄 분모 두 번째 항 Cm 아니라 Cs 1. Chromatography
1.2 Plate Theory • Plate Theory • 이것은 어떤 성분이 용출되기 위해 필요한 Factor와 두 물질이 어떻게 분리될 수 있는 지를 보여준다. • 물질들은 고유한 K 값을 가지고 있다. • K가 증가함에 따라, 용출은 오래 걸린다. • 다른 항목들은 전반적인 분리에 영향을 미친다. 1. Chromatography
1.2 Plate Theory • Plate Theory • Vs를 늘리면 머무름이 증가한다. • VM을 늘리면 머무름이 감소한다. • U를 늘리면 분리의 속도를 증가시킨다. • 특정 컬럼 충진에 대한 직경과 길이를 달리하면 Vs와 VM은 변화된다. • U는 Flow rate를 달리하면 바뀐다. • 모든 항목들은 컬럼이 어떻게 만들어졌는지를 알면 알수 있다. 1. Chromatography
1.2 Plate Theory • Capacity Factor • 간단하게 시료를 주입하고 결과로부터 우리가 필요한 정보를 알고자 한다. • Capacity Factor • (컬럼 조건에 대해 일정함) • 이제 방정식을 확장할 수 있다. 1. Chromatography
1.2 Plate Theory • Capacity Factor • 이제 용출시간을 근거로 k 값을 결정하는 간단한 방법을 알게 되었다. 1. Chromatography
1.2 Plate Theory • Selectivity Factor – α • Chromatography의 목적은 두개 이상의 성분을 분리하는 것이다. • 각 성분은 고유한 k값을 가지므로, 두 성분이 분리될 지 어떨지를 말 할 수 있는 방법이 필요하다. • Selectivity Factor 1. Chromatography
1.2 Plate Theory • Selectivity Factor • 다음 식을 사용할 수 있다. • 용질들에 대한 용출시간에 근거하여 α 값을 결정할 수 있다. • 또는 α값에 근거하여 용질들이 분리되는지를 판단할 수 있다. 1. Chromatography
1.2 Plate Theory • Theoretical Plate (이론 단면) - N • 용매 추출에서 plate(단면)은 각각의 평형으로 표현된다. • 크로마토그라피 컬럼에서 실제로 이 단면을 볼 수 없다. 그래서 이 단면은 이론적이다. • 피크의 용출시간과 넓이를 근거로 하여 컬럼의 이론 단면의 수(이론단수)를 측정할 수 있다. • 두 가지 인자가 분리가 잘 될 것인지를 결정하는 데에 중요하다. 1. Chromatography
1.2 Plate Theory • N 계산하기 • 피크의 머무름시간과 넓이가 이론단수를 구하는데 사용된다. • 머무름 시간과 피크 넓이의 단위가 같다면 단위는 상관없다. 1. Chromatography
1.2 Plate Theory • N 계산하기 • 이론단수는 다음과 같이 구한다. • 피크는 Gaussian 모양을 따르고 통계적으로 처리될 수 있으므로 이러한 접근이 가능하다. • 필수적으로 2 sigma 범위를 취한다. 1. Chromatography
1.2 Plate Theory • N 계산하기 • 예제를 통해 머무름 시간은 같지만 이론단수의 수가 다른 물질을 볼 수 있다. 1. Chromatography
1.2 Plate Theory • N 계산하기 • 종종 피크의 넓이를 측정하기가 어려울 수가 있다. • 피크가 다른 성분과 함께 나올 수 있다. • 낮은 감도의 검출기는 피크의 시작과 끝을 잘못 지정하게 할 수 있다. • 다른 접근 방법을 시도할 수 있다. 1. Chromatography
1.2 Plate Theory • N 계산하기 • 중간 높이의 넓이를 측정할 수 있다. • 이는 검출기 감도의 문제를 배제 할 수 있다. 1. Chromatography
1.2 Plate Theory • N 계산하기 • 피크는 Gaussian 모양이므로 다음과 같은 수정된 식을 만들 수 있다. • 컬럼 길이가 고정된 경우에, 다음과 같은 용어를 정의 할 수 있다. • h (or HETP) • Hight equivalent to a theoretical plate • HETP = column length / N 1. Chromatography
1.2 Plate Theory • Resolution (분해능) • 컬럼이 얼마나 잘 성분을 머무르게 할 수 있는지를 아는 것은 좋다. 그러나 많은 eluent를 다루어야 한다. • Resolution, Rs • 근접한 두 피크가 얼마나 완전히 분리되었는 지에 대한 측정 1. Chromatography
1.2 Plate Theory • Resolution (분해능) 1. Chromatography
1.2 Plate Theory • Resolution (분해능) 1. Chromatography
1.2 Plate Theory • Resolution (분해능) 1. Chromatography
1.2 Plate Theory • 대략적인 Resolution 공식 1. Chromatography
1.2 Plate Theory • 대략적인 Resolution 공식 1. Chromatography
1.2 Plate Theory • 대략적인 Resolution 공식 1. Chromatography
1.2 Plate Theory • Example 1. Chromatography
1.2 Plate Theory • Example 1. Chromatography
1.2 Plate Theory • Example 1. Chromatography
1.2 Plate Theory • Example 1. Chromatography
1.3 Rate Theory • Rate Theory • Plate Theory 는 컬럼은 단면의 컬럼과 동일하다는 가정을 했다. • 이동상과 고정상 사이에서의 용질에 대한 평형 상태가 만들어 진다. • Plate Theory는 유용한 이론이며 크로마토그라피 성능에 대한 많은 정보를 추측할 수 있다. 1. Chromatography
1.3 Rate Theory • Rate Theory • Plate Theory 는 용질의 확산과 이동 경로라는 관점은 무시했다. • Rate Theory 는 이것들을 설명할 수 있으며 다음과 같은 정보를 얻어낼 수 있다. 1. Chromatography
1.3 Rate Theory • Rate Theory • Van Deemter가 유출 농도 함수로 귀착되는 등온에 대한 방정식을 만들었다. • 이 방적식도 Gaussian 분포에 기초한다. • 분리 과정에 대한 동력학을 설명하기 위한 시도이다. 1. Chromatography
1.3 Rate Theory • Van Deemter equation 1. Chromatography
1.3 Rate Theory • Van Deemter equation • 방정식은 다음의 세가지 항목으로 구성된다. • 충진 관련 항목 • 이동상 항목 • 고정상 항목 1. Chromatography
1.3 Rate Theory • Van Deemter equation • 여러 상수들을 그룹화 하여 단일 변수로 만들면 방정식은 다음과 같이 간단해 진다. • H = A + B/u + Cu • A : multipath or eddy diffusion • B : molecular diffusion (분자 확산) • C : resistance to mass transfer • A, B, C는 상수이지만 B와 C는 이동상의 속도에 의존적이다. 1. Chromatography
1.3 Rate Theory • Van Deemter equation • 방정식의 목표는 최적의 컬럼성능을 위한 Hmin 을 찾는 것이다. • H = A + B/u + Cu 1. Chromatography
1.3 Rate Theory • Van Deemter terms • 이 식을 사용하기 위해서 각각의 컬럼/용매 조합에 대한 H 값을 계산할 필요는 없다. • 각 항목이 미치는 효과에 대한 이해는 적절한 컬럼과 최적의 flow를 결정하는데 도움을 줄 수 있다. 1. Chromatography
1.3 Rate Theory • A term • 이 항목은 충진물의 크기와 배열의 영향을 설명한다. • 가능한 용질이 이동경로의 범위는 피크의 넓이로 귀착된다. 1. Chromatography
1.3 Rate Theory • A term • 한번 컬럼이 충진되고 나면, A 를 감소시키기 위해서는 아무런 방법도 없다. • 이 효과는 다음과 같은 것들에 의해 감소될 수 있다. • 균일한 크기의 충진 • 작은 직경을 사용한 충진 • 꽉 찬 충진 • Dead volume의 최소화 1. Chromatography