Ušlechtilé kovy
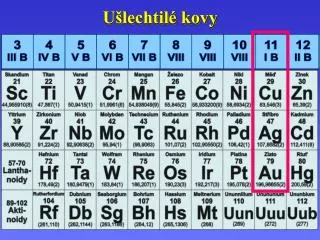
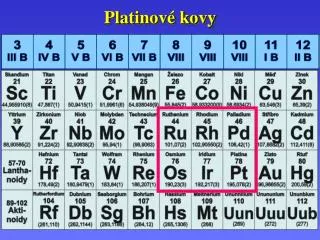
Ušlechtilé kovy. S kupina I . B. Měď, Stříbro, Zlato – ušlechtilé kovy. konfigurace Cu 4 s 1 3 d 10. M ě ď. Cu – Cu 2 S chalkosin, CuFeS 2 chalkopyrit Cu 2 O cuprit . . výroba Cu ~ S oxid + C Cu - sur ová Cu - sur ová elektrol ýz a. Oxidační čísla Cu ( I ) Cu ( II ) .

Ušlechtilé kovy
E N D
Presentation Transcript
SkupinaI.B Měď, Stříbro, Zlato –ušlechtilé kovy konfigurace Cu4s13d10
Měď Cu–Cu2Schalkosin,CuFeS2chalkopyrit Cu2Ocuprit . . výrobaCu ~ Soxid + CCu- surová Cu- surováelektrolýza Oxidační číslaCu(I)Cu(II) . Cu(I)Cu2O– červený(Fehling) CuCl, CuI, CuCN, Cu2S, Na3[Cu(CN)4], Cu(CO)Cl . . Cu(II)CuO,CuSO4·5H2O,NO3– Cu(CH3COO)2·2H2O . Cu(III)komplexy, telluridy . . Jahn-Telerův efekt[Cu(NH3)4]2+
Jahn - Tellerův efekt „Systémy se spinově a orbitálně degenerovanými stavy mají tendenci spontánně distortovat okolí centrálního atomu a sejmout tak tuto degeneraci.“ Oh D4h Cu2+3d9 6 el. dxy, dxz, dyz,3 el. dz2, dx2–y2 1,51,5 Oh–d4, d9 Td–d3, d4, d8, d9
Oxidy mědi CuO–tenorit Cu2O–kuprit
Cu 5– 5– III III Cu Te Te I Cu I 2– Cu Cu Komplexy mědi Komplex Cu2+ s biuretem
Cu Struktura plastocyaninu Komplexy mědi
Cu Cu • O • CuIICuII • O MĚĎ Dusík Uhlík Struktura deoxyhemocyaninu Komplexy mědi Cu – Cu~ 3,7 Å
Stříbro Ag–Ag2Sargenit,Ag3SbS3prousit AgAsS3pyrostilpnit . . výroba:hutnictví (Pb);Parkes chudé rudy:Ag2S+4CN–2[Ag(CN)2]– 2Ag++2OH–Ag2O+H2O . AgF·2H2O – dobře; AgCl, Br–, I– . AgCl+2NH4OH[Ag(NH3)2]Cl+2H2O AgNO3;Ag2SO4 . . Na2S2O3FotografieAgX[Ag(S2O3)2]3–
Stříbro Další oxidační čísla Ag(II)Ag++O3AgO++O2 AgO++Ag++2H+2Ag2++H2O . AgF2;AgO . . Ag(III)KAgF4
2+ 2+ II II Ag Ag (b) (a) 5– III Ag I I Komplexy stříbra
Zlato Au–Výroba: kyanidový způsob . 4Au+8CN–+H2O+O2 4[Au(CN)2]–+4OH– . 2[Au(CN)2]–+Zn2Au+[Zn(CN)4]2– . nestálýH[AuCl4] Au+(aq)Au3+(aq) + 2e–0=+ 1,401 V 2e– + 2Au+(aq)2Au0=+ 1,691 V 3Au+(aq)2Au + Au3+(aq)EMF=+ 0,290 V
SkupinaII.B Zinek, Kadmium, Rtuť konfigurace Zn4s23d10 Oxidační číslaZn2+,Cd2+,Hg2+[–Hg–Hg–]2+
SkupinaII.B Oxidy . ZnO –amfoterní ZnO+2HClZnCl2+H2O ZnO+NaOHNa2[Zn(OH)2] . . CdO, HgO– spíše bazické Tepelná stálost –klesáZnO>CdO>HgO . HgOHg+O2
Zinek a Kadmium Zn–ZnCO3 smithsonit . výroba:praženíZnCO3ZnO redukceZnO+CZn+CO . . ZnS–bílý,ZnSO4·5H2O [Zn(NH3)2]2+; [Zn(CN)4]2– Zn+2HClZnCl2+H2 . Zn+NaOHNa2[Zn(OH)4]+H2 (Na[Zn(OH)3H2O],Na[Zn(OH)3(H2O)3]) Cd–příměs Zn; CdS; CdSO4·8/3H2O
Sloučeniny zinku v biochemii karbonátová anhydráza
Karboxy- peptidáza A Sloučeniny zinku v biochemii
Rtuť Hg–HgS rumělka . HgS+O2Hg+SO2 Hg+FeHg+FeS . HgCl2–sublimát; Hg(NO3)2; [HgI4]2– Hg2Cl2–kalomel–málo rozpustný;Hg2(NO3)2 . . Hg–použití: teploměry,elektrolyzéry,fungicidy Hg(I)–Hg–Hg–nelze O2–,OH– Hg2X2;Hg2Cl2 kalomel; HgCl2+HgHg2Cl2 . . Hg(II)HgO;Hg2++2OH–HgOžlutý Hg(NO3)2HgO+2NO2+½O2 červený . dimethyl rtuť Hg(CH3)2
Chlor Rtuť NH3 Komplexy rtuti HgCl2+8NH3[Hg(NH3)2Cl2] (1) [Hg(NH3)2Cl2][Hg(NH2)Cl]+NH4Cl(2) 2[Hg(NH2)Cl]+H2O[Hg2NHCl(H2O)]+NH4Cl(3) [Hg(NH3)2Cl2]
N Hg Sloučeniny rtuti Uspořádání sítě Hg2N+v krystalové struktuře Millonovy báze[Hg2N(OH)(H2O)] 4NH3+2[HgI4]2–+H2O[Hg2NI(H2O)]+3NH4++7I–