Ch10 原子結構
Ch10 原子結構. §10-1 拉塞福的原子模型 §10-2 氫原子光譜 §10-3 波耳的氫原子模型 §10-4 夫然克 - 赫茲實驗 §10-5 中子的發現 §10-6 原子核的構造 §10-7 原子核的放射性與衰變 §10-8 原子核的分裂與核能 §10-9 核融合與核能. §10-1 拉塞福原子模型. 湯木生原子模型. 1904 年英國人 湯木生 ,在原子為電中性的基礎上,所提出的一種原子結構模型。 認為原子是半徑約 10 -10 公尺帶正電的實心球體,而帶負電的電子則散布其中。 電子在正電荷球中的位置呈平衡狀態。

Ch10 原子結構
E N D
Presentation Transcript
Ch10 原子結構 §10-1 拉塞福的原子模型 §10-2 氫原子光譜 §10-3 波耳的氫原子模型 §10-4 夫然克-赫茲實驗 §10-5 中子的發現 §10-6 原子核的構造 §10-7 原子核的放射性與衰變 §10-8 原子核的分裂與核能 §10-9 核融合與核能
§10-1 拉塞福原子模型 • 湯木生原子模型 • 1904年英國人湯木生,在原子為電中性的基礎上,所提出的一種原子結構模型。 • 認為原子是半徑約10-10公尺帶正電的實心球體,而帶負電的電子則散布其中。 • 電子在正電荷球中的位置呈平衡狀態。 • 又稱為西瓜模型。 湯木生的原子模型
拉塞福α粒子散射實驗 • 實驗裝置: • 以放射性元素鐳,放出的α粒子,撞擊薄金箔(厚度約為 10- 7米),從各角度觀測被散射的α粒子。
實驗結果: • 絕大部分α粒子筆直通過。 • 散射角大於 90o 的機率高達 1/8000,與湯木生模型計算的數值相差甚多。 • α粒子通過金箔後,金箔帶正電。 • 拉塞福的原子行星模型(於1911提出) • 原子的正電荷與大部分質量集中在原子內很小的區域,半徑大小約10-15m(1fm或1費米),此區域稱為原子核。 • 電子受原子核的靜電庫侖力作用繞原子核作圓周運動,電子存在的空間構成了原子的體積(半徑大小約10 -10m)。 • 原子核所帶的正電的量值等於原子內所有電子的電量總和,故原子可維持電中性。
拉塞福的理論計算結果: • 根據這個原子的行星模型,拉塞福假設α粒子和原子核間的作用力為兩個點電荷間的靜電排斥力,利用古典力學的運動定律計算出自某一散射角θ,測量到α粒子的散射機率 此結果與實驗數據完全吻合
拉塞福原子結構模型遭遇的困難: • 電子繞原子核的運動為加速度運動,因此會不斷的輻射出電磁波,而使電子的動能減少,最後墜落在原子核上,無法構成一穩定的原子。 • 波耳利用能階的概念解決拉塞福原子結構模型遭遇的困難。
例題:在拉塞福的α粒子散射實驗中,下列敘述何者正確?例題:在拉塞福的α粒子散射實驗中,下列敘述何者正確? (A) α粒子的力學能恆為正 (B) α粒子的角動量守恆 (C) α粒子的散射角恆小於 90o (D) α粒子的入射方向與力心的垂直距離越大,散射角越大 (E)由此一實驗之結果,證實了原子核的存在 [90.日大] 答案:ABE
例題:下列有關拉塞福α-粒子散設實驗之敘述有那些是正確的? (A)入射的α-粒子其動能約為 10 3電子伏特 (B)撞擊參數越大,α-粒子的偏折越大 (C)固定數目的入射α-粒子其動能越高,所測得之被散射α-粒子越多 (D)散射角大於 90o之α-粒子遠少於散射角小於 90o之α-粒子 (E)一種元素之各種同位素其拉塞福α-粒子散射角分布是相同的。 [75.日大] 答案:DE (A) α-粒子的動能為百萬電子伏特數量級
例題:在α質點對金屬箔片之拉塞福散射中下列敘述何者為正確的?例題:在α質點對金屬箔片之拉塞福散射中下列敘述何者為正確的? (A)被散射之α質點其軌跡為雙曲線 (B)在固定散射角處散射α質點的數目與α質點之入射速度 平方成反比 (C)每一α質點對原子核之最近距離一定大於其撞擊參數 (D)金屬箔片的原子序越大, α質點被散射的機會也越大 (E)散射角大於 60o者佔很小比例。 [70.日大] 答案:ACDE
例題:使用金靶做兩種散射實驗:其一用質子束衝擊,另一則用氘核束(質量數 2,原子序 1)。設此兩種粒子束的速率相同,則氘核可接近於金核的最短距離等於質子可接近最短距離之 ________ 倍。 [63.日大]
例題:設α粒子與金原子核所的電量分別為 +ze 與 +Ze,一質量為 m 的α粒子以初速度 v0射向一金原子核,由於受到靜電力的作用而產生散射。因為金原子核比α粒子重約 50倍,故在α粒子的散射過程,金原子核可視為固定不動。 α粒子的入射線與金原子核的垂直距離為 b(稱為撞擊參數),試求在α粒子的散射過程中與金原子核的最近距離。
§10-2 氫原子光譜 1. 夫朗和斐發明多狹縫的光柵稱為光譜儀,開啟了光譜學的研究。 2. 德國人克希何夫和本生發現每個元素在氣態時,都有其特定的明線光譜。 3. 埃司傳研究氣體放電的光譜中,找到了氫原子的可見光光譜。 4. 1885年瑞士人巴耳麥找到了氫光譜的可見光區域波長的經驗公式 其中 λ0 = 3645.6 埃,n 為大於或等於 3 的整數。
5. 1890年瑞典人芮得柏提議巴耳麥公式中波長改為倒數的形式。可得較簡潔的形式 其中 n 為大於或等於 3 的整數,R = 1.09677×10 7m-1稱為芮得柏常數。 6. 1908年瑞茲提出組合原理,由光譜中任兩條光譜線,其頻率的和或差,可找出另一條光譜線,故可將光譜線波長的關係式寫成 n 和 m 為正整數且 n > m
7. 瑞茲的公式預測了 m = 3 的氫原子光譜線,很快的此一線系於 1908年由德國人帕申所發現,稱為帕申系。 巴耳麥系的譜線自可見光範圍,帕申系的譜線則在紅外光的範圍
§10-3 波耳的氫原子模型 波耳為了解釋這些氫原子光譜,引進卜朗克和愛因斯坦的量子論,結合牛頓力學,提出波耳的原子模型。 • 波耳原子模型的基本假設: • 第一基本假設: • 電子僅能在某些特定的軌道上,繞原子核運動,這些軌道稱為穩定態。電子在穩定態上運動時,不會輻射電磁波,這些在穩定態的電子,其角動量 L必須滿足角動量量子化的條件: n 為一正整數
第二基本假設: 當電子從一能量為 Ei的穩定態軌道,躍遷到另一個較低能量Ef的穩定態軌道時,原子會輻射出頻率為ν的光子,所輻射出光子的能量等於兩穩定態的能量差,即 2. 波耳氫原子模型的理論計算: 電子繞原子核作圓周運動所需的向心力,由電子與原子核間的靜電力提供,依牛頓第二運動定律 m 為電子質量,k 為電力常數,r 為電子軌道半徑。
再由波耳第一基本假設,角動量量子化的條件 (1) ÷ (2) 2消去 v 得軌道半徑量子化條件 當電子在穩定態時,被允許的軌道半徑 r 是不連續的,電子的軌道半徑 r 正比於 n 2。 電子的總力學能 E 為
將軌道半徑量子化的條件代入上式,得能量量子化的條件將軌道半徑量子化的條件代入上式,得能量量子化的條件 n = 1 的能階稱為基態,n = 2 的能階稱為第一受激態, n = 3 的能階稱為第二受激態,依此類推。 3. 類氫原子的能階:原子序為 Z的單電子原子,能階為
4. 氫原子光譜: 當電子由高能階 En躍遷到低能階 Em時,由波耳的第二基本假設,原子所輻射出光子的頻率ν和波長λ分別為 芮得柏常數: 在波耳提出氫原子理論之前,僅有巴耳麥和帕申兩個光譜線系被發現,但波耳理論預測尚有 m = 1,4,5,....等的光譜線系,這些線系很快的陸續被發現。
(1922年) (1908年) (1885年) (1914年)
例題:在波耳的氫原子模型中,氦離子(He+)中的電子以圓形軌道繞行原子核。設此電子自基態躍遷至某一受激態,則下列電子的物理量中,躍遷後大於躍遷前的是:例題:在波耳的氫原子模型中,氦離子(He+)中的電子以圓形軌道繞行原子核。設此電子自基態躍遷至某一受激態,則下列電子的物理量中,躍遷後大於躍遷前的是: (A)位能 (B)動能 (C)物質波波長 (D)軌道運動之週期 (E)所受向心力之量值。 [88.日大] 解:量子數 n 變大,軌道半徑 r 變大,力學能增加。位能為力學能的兩倍,因此位能也增加。動能與力學能大小相等符號相反,因此動能減少。速率與軌道半徑開根號成反比,因此動量減小,物質波長變長。週期平方與軌道半徑三次方成正比,因此週期變大。 答案:ACD
例題:在波耳氫源子結構的理論當中,下列那一個物理量與量子數 n 的三次方成正比? (A)電子能量 (B)電子角動量 (C)電子速率 (D)電子軌道半徑 (E)電子軌道運動的週期。 [87.日大] 說明:軌道半徑與 n 的平方成正比,週期的平方與軌道半徑的三次方成正比正比,因此週期與 n 的三次方成正比。 答案:E
例題:波耳在氫原子結構的理論中,引入了量子數 n。在此理論中,下列各物理量與 n 的關係何者正確? (A)電子的軌道半徑與量子數 n 的平方成正比 (B)電子在軌道中的運動速率與量子數 n 成反比 (C)電子在軌道中的角動量與量子數 n 成反比 (D)電子的位能與量子數 n 的平方成正比 (E)當 n >> 1 時,電子在相鄰兩能階間的能量差約與 n 的立 方成反比。 [81.日大] 答案:ABE
例題:一氫原子之電子在量子數 n = 4 之受激態,它可能放射出之電磁波最高頻率為 ________ 赫。 [89.日大] 解:由量子數 n = 4 之受激態躍遷至 n = 1 之基態時,所放射的電磁波能量 E 最高
例題:若以 m → n 代表氫原子從能階 E m躍遷至能階 E n,並以 n = 1 代表基態,n = 2 代表第一受激態,…,則以能量13.00eV 之電子撞擊處於基態之原子後,受激發之氫原子可能發生之躍遷有那些? [73.日大] (A) 2 →1 (B) 3 →2 (C) 4 →1 (D) 4 →3 (E) 6 →4 。 答案:ABCD
例題:如一氫原子的電子從 n = 2 的穩定態躍遷至 n = 1 的穩定態時,所放出光子能量為 E。則一氦離子 He+ 的電子從 n = 3 的穩定態躍遷至 n = 2 的穩定態時,所放出光子的能量約為 ________ E。 [83.日大]
例題:已知氫原子的電子從量子數 n = 2 能階躍遷至 n = 1能階時,發射波長為 121.5nm 的電磁波;從 n = 4 能階躍遷至 n = 1 能階時,發射波長為 97.2 nm 的電磁波。試問電子從 n = 4 能階躍遷至 n =2 能階時,所發射電磁波的波長為 _______ nm。 [93.指定科考]
例題:已知要將氫原子基態的電子游離時,可用的最長波長的光為 913 埃的紫外光。那麼從各受激態至基態的來曼系光譜,其波長可用下式表示:
例題:已知將氦原子中兩個電子完全除去所需之總能量為 79電子伏特,則僅除去第一個電子時所需之能量為: (A)20.4eV (B)24.6eV (C)39.5eV (D)65.4eV 。 [70.日大] 解:除去第二個電子所需能量為 13.6 × 4 = 54.4 eV, 因此僅除去第一個電子的能量為 79 – 54.4 = 24.6 eV 答案:B
n = 2 n = 4 n = 3 n = 5 5. 波耳的第一基本假設與物質波: 根據德布羅依的物質波觀念,電子的物質波長 上式表示電子軌道的圓周長恰等於物質波長的整數倍,此為電子的物質波在軌道上行成駐波的條件。
例題:質量為 m 的帶電粒子,在相隔 d 的兩個固定壁間運動,因而產生輻射。此粒子由第一激發態回至基態時的輻射頻率為何? [70.夜大]
汞蒸氣 §10-4 夫然克-赫茲實驗 波耳所引入穩定態的觀念,不僅由氫原子光譜得到強力支持,1914年,夫然克-赫茲以電子碰撞汞原子的實驗,亦直接證實原子能階的存在。 • 1. 實驗裝置及原理: • C、G、P 極皆在低氣壓的管中,管內有汞蒸氣。 • 電子由陰極 C 發出至柵極 G ,經電壓 V 加速獲得動能
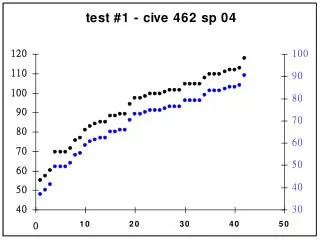
屏極 P 與柵極 G 之間有一小逆向電壓 Vr,使穿過柵極的電子減速,動能較小的電子將無法到達屏極 P。 • 安培計 A 測量單位時間到達屏極 P 的電子數。 • 2. 實驗結果: • 如右圖所示,當電壓 V 增至 4.9 伏特時,電流突然下降。 • V 增至 9.8 伏特時,電流再次下降。
3. 實驗結果的解釋: • 汞原子的第一受激態和基態之間的能階差為 4.9eV。 • 當電子被電場加速所得動能小於 4.9eV,無法激發汞原子,則電子與汞原子間作彈性碰撞。由於汞原子的質量遠大於電子,所以碰撞後電子動能幾乎不變,可以克服反向電壓而到達屏極,形成電流。 • 當電子被電場加速所得動能等於 4.9eV,恰可激發汞原子,則部分電子與汞原子間作非彈性碰撞。碰撞後電子動能損失,無法克服逆向電壓到達屏極,故電流減少。 • 當電壓增至或超過 9.8V,則電子有兩次機會將汞原子從基態激發至第一受激態,故也會造成電流驟降。因此電壓每間隔 4.9V,會有一次電流驟降。
例題: 汞原子之能階中第一受激態比基態高出 4.9 電子伏特,第二受激態比基態高出 6.7 電子伏特。若以動能為 6.2電子伏特之電子束射入處於基態之汞原子區域,則穿過此區域之電子其能量可能為: (A)0.5eV (B)1.3eV (C)4.9eV (D)6.2eV。 [70.日大] 答案:BD
§10-5 中子的發現 • 1. 中子發現的歷史: • 1930年,德國人波特和貝克利用釙所放射的α粒子撞擊鈹,產生一種穿透力很強的中性射線,猜想可能為γ射線。 • 1932年,居禮夫婦的女兒伊琳與女婿朱里歐,將α粒子撞擊鈹,產生的中性射線照射石臘板,發現會放射出動能高達 5.7MeV的質子,經計算此中性射線能量需高達 52MeV。 • 英國人查兌克認為由原子核放出的光子或粒子,一般能量僅有幾 MeV,不可能達 52MeV,因此認為原子核所放出的射線不是γ射線,而是中子。1932年,查兌克將α粒子撞擊鈹,產生的中性射線照射氣體原子,測量氣體離子動能,求出中子的質量約等於質子的質量。
2. 實驗裝置: α粒子從釙放射源射出後撞擊鈹,產生的中性射線照射氫原子與氮原子氣體,測量氫原子與氮原子被撞擊後的最大速度,利用彈性碰撞的動能守恆與動量守恆,求出中子的質量。
3. 實驗原理與結果: 中子質量 mn以速率 vn分別與氫離子(質量 mH)及氮離子(質量 mH)作正向彈性碰撞,由動量守恆及動能守恆可得 即中子的質量約等於質子的質量。 中子被證明是一個單一粒子。
質量數 元素符號 原子序 §10-6 原子核的構造 1. 原子核的組成: 1932年海森堡提出原子核結構的新模型: 原子核由 Z 個質子與 A - Z 個中子所構成, Z 稱為原子序,A 稱為質量數。符號上記為 2. 同位素: 質子數相同而質量數或中子數不同的元素稱為同位素。 同位素以相同的元素符號表示,在週期表佔據相同的位置,因其價電子情形相同,故化學性質相同,但物理性質不一定相同。
3. 原子量: • (1) 原子的質量單位: • 取碳同位素 12C 的一個中性原子質量定為 12u, 即 1u = 1.66056 ×10 - 27kg。 • 電子質量 me = 9.109 × 10 - 31kg = 0.000549u • 質子質量 mp = 1.6726 × 10 - 27kg = 1836me • 電子質量 mn = 1.6750 × 10 - 27kg = 1839me (2) 平均原子量: 該元素所有同位素的原子量乘上所占百分比之加總,為週期表上該元素原子量。 例如氯的平均原子量:35Cl(含量為 75.4%)和 37Cl(含量為 24.6%),因此 Cl 的原子量為 35u × 0.754 + 37u × 0.246 = 35.5 u
4. 原子核的大小和形狀 • 多數原子核的形狀接近球形,其半徑 R = R0A1/ 3 ,其中 A 為質量數,R0 = 1.2 fm(費米) • 原子核的體積與所含的質量數成正比,又質子及中子質量相近,故原子核的密度接近定值。ρ= 2.3 × 1017kg/m3,約為水的 2.3 × 1013倍。 • 5.核力: • 核子(質子、中子)間存在一遠較靜電排斥力為強的吸引力(稱為核力),使質子和中子能聚成穩定的原子核。 • 核力又稱為強交互作用力。為一短程力,在長距離(大於原子核半徑),則迅速地隨距離而遞減。 • 核力和與核子所帶的電荷無關,所有核子間的核力作用均相同。
鉛座 α γ β 放射源 §10-7原子核的放射性與衰變 • 1. 天然的放射性衰變 : • (1) 放射性元素的發現: • 1896年,法國人貝克勒發現鈾礦可放出一種使底片感光的射線。 • 1898年4月,居里夫婦發現釷元素也具有放射性。 • 1898年 7月和 12月,居里夫婦又發現從瀝青提煉出來的新元素釙和鐳也具有放射性。 (2) 天然放射線的種類: 1898年,拉塞福分離出兩種不同的 射線,分別稱為α射線與β射線。
1900年,貝克勒證明β射線為電子。 • 1900年,維拉德發現另一種不受磁塲偏折,且穿透力極強的放射線,後來由拉塞福命名為γ射線。 • 1909年,拉塞福證明α粒子是帶正電的氦離子。 (a) α衰變: 原子核產生α衰變後,其核內的質子數和中子數各減少兩個,故原子序減 2,而質量數減 4,可以下列的核反應式表示之:
(b) β衰變: • 在β衰變中,中子會轉變成質子,另外生成電子和反微中子。 • 當原子核產生β衰變後,其核內的中子數減少一個,但質子數增加一個,故其原子序加 1,但質量數不變,可以下列的核反應式表示之: • 例如:
(c) γ衰變: • γ 射線是高能量的光子。當原子核的能態從高能階躍遷至低能階時,就會將兩能階的差值,以光子的形式釋放出來。 • 通常原子核在產生α 或β衰變時,都會伴隨γ射線的放射。 • 原子核產生γ衰變時,其原子序和質量數都不會改變。 • (3) 原子核反應方程式: • 利用類似化學反應方程式的方式來說明原子核的變化情形 • 遵守電荷守恆及質量數守恆,即反應前的電荷總和及質量數總和在反應後須保持不變,但質量不守恆。
(4) 自發衰變: 原子序大於 82(鉛)的元素,由於質子數太多,彼此強大的靜電排斥力,使得原子核(稱為母核)不穩定,會經一系列的α、β、γ衰變,而成為較穩定的原子核(稱為子核)。這些自發衰變,可區分成四種系列:
例題:原子核作一次α-衰變時,其原子序減少 2,質量數減少 4;作一次β-衰變時,原子核內一中子放出一電子後變成一質子,因此質量數不變,但原子序增加 1。一 23892U(鈾)原子核衰變成 20682Pb(鉛)原子核。途中產生α-衰變和β-衰變的次數分別為 (A)8次和3次 (B)3次和5次 (C)5次和6次 (D)8次和6次 (E)5次和3次。 [72.日大]
2. 半衰期: • (1)放射性元素的衰變定律: • 原子核衰變的發生是一種機率性的過程,我們無從預測那一個原子核,在哪一時刻會發生衰變,每一次衰變都是獨立事件,且不受溫度和化學作用的影響。 • 從統計學上來看,如果原子核的數目夠大,則每隔一定的時間間隔,將有半數的原子核發生衰變,此時間間隔稱為半衰期,以τ或 T1/2表示。 • 如某一放射性元素的半衰期為τ,原來有 N0個放射性原子核,經過時間 t 後,該放射性元素所剩尚未衰變的原子核個數 N,則