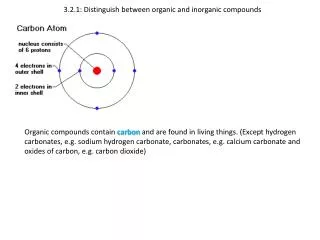
The difference between organic and inorganic compounds
410 likes | 1.17k Views
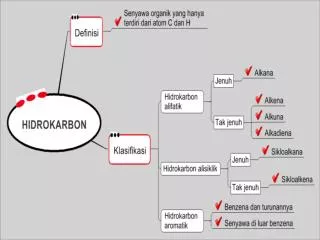
The difference between organic and inorganic compounds. The difference between organic and inorganic compounds. Senyawa Hidrokarbon = Senyawa karbon yang terdiri atas unsur karbon dan hidrogen.

The difference between organic and inorganic compounds
E N D
Presentation Transcript
Senyawa Hidrokarbon = Senyawa karbon yang terdiri atas unsur karbon dan hidrogen. Senyawa karbon yang paling sederhana adalah metana dan yang sangat kompleks diantaranya molekul DNA yang terdiri atas jutaan atom, senyawa protein, polisakarida dan lain-lain. • Kekhasan atom karbon: • Atom C memiliki 4 elektronvalensi (Gol IV A) sehingga dapat membentuk 4 ikatan kovalen. • Atom C dapat membentuk rantai karbon tak bercabang maupun bercabang. • Atom C dapat membentuk rantai C terbuka (alifatik) maupun rantai tertutup (siklik). • Atom C dapat membentuk ikatan tunggal (ikatan jenuh), rangkap 2 (gol alkena) dan rangkap 3 (gol alkuna).
Denganev = 4 membentuk 4 ikatankovalen Sbb : | ― C ― | Dapatmembentukrantaikarbon , yaituikatanantara atom karbon yang satudengan atom karbon yang lain.
C C – C – C C – C C – C – C C Atom C dapat membentuk ikatan tunggal (ikatan jenuh), rangkap 2 (gol alkena) dan rangkap 3 (gol alkuna). A. Senyawa jenuh jika semua ikatan C nya tunggal Contoh : | | | | | - C - C - C - C - C | | | | | B. Senyawa tidak jenuh Jika terdapat ikatan rangkap dua atau tiga. C= C - C - C atau -C C - C- C H2C = CH – CH2– CH3
H C H • CH2 − CH2 • | | • CH2 − CH2 H C C Alifatik (Rantai terbuka) Alisiklik (Rantai Tertutup) C C C H H H Aromatik (Benzena & Turunannya)
O O O H C C H C C C 2 C H H O H 3 styrene acetophenone benzaldehyde benzoic acid SENYAWA TURUNAN BENZENA O H C H O C H N H 3 3 2 phenol toluene aniline anisole
jumlah atomC Rumus Struktur Nama • 1 CH4 Metana • C2H6 ditulis CH3 CH3 Etana • 3. C3H8 ditulis C H3 C H2 C H3 Propana
MENGGOLONGKAN SENYAWA HIDROKARBONSenyawa hidrokarbon digolongkan berdasarkan ada atau tidaknya ikatan rangkap ( ganda ).
HOMOLOG = Deretan senyawa yang mengalami penambahan jumlah atom secara teratur Cont: CH4 , C2H6 , C3H8 dst C2H4 , C3H6 , C4H8 dst
JENIS ATOM C • Atom C primer = atom C yang mengikat 1 atom C lain. • Atom C sekunder = atom C yang mengikat 2 atom C lain. • Atom C tersier = atom C yang mengikat 3 atom C lain • Atom C kuarterner = atom C yang mengikat 4 atom c lain.
JENIS ATOM C DALAM SENYAWA HIDROKARBONTerdapat 4 jenis atom C ( karbon ) dalam senyawa hidrokarbon. • 2. Atom C sekunder ialah atom C yang mengikat 2 atom C lain. • Contoh : 1. Atom C primer ialah atom C yang mengikat 1 atom C lain. Contoh :
3. Atom C tersier ialah atom C yang mengikat 3 atom C lain.Contoh : • 4. Atom C kuarterner ialah atom C yang mengikat 4 • atom C lain. Contoh :
4. 1. 2. 5. 3. Latihan : Tentukan jumlah atom C primer, sekunder, tertier, dan kuarterner nya
MENGGOLONGKAN SENYAWA HIDROKARBONSenyawa hidrokarbon digolongkan berdasarkan ada atau tidaknya ikatan rangkap ( ganda ).
AlkanaAlkana ialah senyawa hidrokarbon yang seluruh ikatannya tunggal ( jenuh ). Semua senyawa alkana memiliki rumus umum : CnH2n+2 di mana n adalah jumlah atom karbon. jumlah atomC Rumus Struktur Nama 1 CH4 Metana 2 C2H6 ditulis CH3 CH3 Etana
C3H8 ditulis C H3 C H2 C H3 Propana
jumlah atom C Rumus Struktur Nama RUMUS LENGKAP 1 CH4 ditulis CH4 Metana 2 C2H6 ditulis CH3 CH3 Etana 3 C3H8 ditulis CH3 CH2 CH3 Propana
TATA NAMA SENYAWA ALKANA • Menentukanrantai C terpanjangsebagairantaiutama. • Atom-atom C diluarrantaiutamasebagaicabang. Cabangmerupakangugusalkil (-CnH2n+1) -CH3 : metil -C2H5 : -CH2-CH3 : etil -C3H7 : -CH2-CH2-CH3 : propil
3. Penomoran pada atom C rantai utama dimulai dari ujung yang terdekat dengan cabang. 4. Jika ada dua/lebih cabang yang sama maka diawali dengan di, tri, tetra, penta dst 5. Penulisan nama senyawa dg urutan: no cabang-nama cabang- nama rantai utama. 6. Penulisan nama cabang sesuai urutan abjad.
Beri nama senyawa berikut: 1. • (CH3)2CH-(CH2)2-CH(C2H5)-CH2(C2H5) • (C2H5)3C-(CH2)2-C(CH3)(C2H5)-CH(CH3)(C2H5)
GUGUS ALKIL sebagai cabang dengan rumus CnH2n+1
Contoh penentuan posisi yang salah : 6. Jika terdapat 2 cabang atau lebih yang sama, maka jumlah cabang yang sama dinyatakan dengan : 2 = di 6 = heksa 3 = tri 7 = hepta 4 = tetra 8 = okta 5 = penta 9 = nona 2,3-dimetilheksana
Contoh lain : 2,2-dimetilheksana 4-etil-2-metilheptana bukan 2-metil-4-etilheptana
Rangka Struktur Posisi Gugus fungsi Isomer Geometri Ruang Optis
Isomer rantai = isomer yang disebabkan kerangka karbon yang berbeda. • Isomer posisi = isomer yang disebabkan perbedaan letak dari gugus fungsi pada rantai induk. • Isomer Fungsi = isomer yang disebabkan perbedaan gugus fungsi. • Isomer Geometri = isomer yang disebabkan perbedaan letak atom(gugus atom) yang sama dalam ruang. • syarat : • Rantai induknya memiliki atom C yang berikatan rangkap (-C=C-) • Pada atom C berikatan rangkap mengikat 2 atom/gugus atom yang berbeda.
Stereoisomer = Senyawa berlainan yang memiliki struktur sama, tetapi berbeda dalam hal penataan atom-atom dalam ruangan. • 4. Isomer Geometri = Isomer yang disebabkan perbedaan letak atom/gugus atom yang sama disekitar atom C yang berikatan rangkap. • syarat : • Rantai induknya memiliki atom C yang berikatan rangkap (-C=C-) • Pada atom C berikatan rangkap mengikat 2 atom/gugus atom yang berbeda. • 5. Isomer optik = isomer yang disebabkan perbedaan dalam memutar cahaya terpolarisasi.
H Cl C l Cl C C C C Cl H H H Trans-1,2-dikloroetena t.d. 48oC Cis-1,2-dikloroetena t.d. 60oC
KEISOMERAN ISOMER = Senyawa yang berbedatetapimempunyairumusmolekulsama Contoh : Senyawadenganrumus C4H10memiliki 2 isomer 1. normal butana / n butana n-butana (t.d = -0.5°C) 2. 2-metilpropana (IUPAC) Isobutana (TRIVIAL)
ISOMER = Senyawa yang berbedatetapimempunyairumus molekulsama Senyawadenganrumus C5H12memiliki 3 isomer Contoh : • n pentana • 2-metilbutana (IUPAC) atau isopentana (TRIVIAL) • 2,2-dimetilpropana (IUPAC ) atau neopentana (TRIVIAL) KEISOMERAN pentana (t.d = 36,1°C) isopentana (2-metil butana) t.d = 27,9°C
Isomer Alkana Contoh : • C4H10 2 isomer butana 2-metil propana • C5H12 3 isomer • C6H14 5 isomer • C7H16 9 isomer • C8H18 18 isomer