TERMODINAMIKA
TERMODINAMIKA. Energ ia. A RENDSZER TULAJDONSÁGA HOGY MUNKÁT VÉGEZZEN, VAGY HOGY HŐT TERMELJEN. Az energia két típusa. Poten ciális : az objektum helyzetéből vagy összetételéből adódik és munkává konvertálható Kineti kus : az o bje k t um mozgásából adódik KE = 1 / 2 mv 2

TERMODINAMIKA
E N D
Presentation Transcript
Energia • A RENDSZER TULAJDONSÁGA HOGY MUNKÁT VÉGEZZEN, VAGY HOGY HŐT TERMELJEN.
Az energia két típusa • Potenciális: az objektum helyzetéből vagy összetételéből adódik és munkává konvertálható • Kinetikus: az objektum mozgásából adódik • KE = 1/2 mv2 • (m = tömeg, v = sebesség)
Az energiamegmaradás törvénye • Az energiafajták egymásba konvertálhatók, de az energia se nem teremthető, se nem megsemmisíthető. • (Euniverzum= konstans, állandó)
Hőmérsékletill. Hőmennyiség átadás • A hőmérsékleta részecskék random mozgásábóladódik, így a rendszer kinetikus energiájához kötött. • A hőmennyiség átadás két eltérő hőmérsékletű tárgy közötti energia transzfert jelenti.
A rendszer és környezete • Rendszer: Az a rész amire figyelmünk irányul • Környezet: Minden más az univerzumban • Univerzum = Rendszer + Környezet
A termodinamika fogalomrendszere arendszer: az általunk vizsgált „világ” valamilyen „fallal” (részben) elhatárolt része a környezet: a „világ” rendszert körülvevő része rendszer- anyagcsere energiacseretípus - faltípus - faltípus nyíltvanvan - (szemi)perm. - diatermikus zártnincs van - inpermiábilis - diatermikus izoláltnincs nincs - inpermiábilis - adiabatikus mechanikai kölcsönhatás: merev/mozgó fal
A vizsgált rendszer belső felépítése szerint: • fizikai és kémia tulajdonságok eloszlása alapján: • homogén (minden pontban azonosak) • inhomogén(folytonosan változnak) • heterogén(ugrásszerűen változnak) • a tulajdonságok irányfüggése alapján: • izotróp(minden irányban azonos) • anizotróp (kitüntetett irányok vannak) • egyszerű – összetett(egyszerű alrendszerekből) • alkotói: • egy vagy több fázis(fizikai azonosság) és • egy vagy több komponens(kémiai azonosság)
V V V V Állapothatározók P • Isobar • P = constant • Isochor • V = constant • Isotermikus • T = constant • Adiabatikus • Q = 0 P P P
Állapotfüggvény • Értéke a kezdeti és végállapot függvénye csupán, független az úttól, ahogy a végállapotba érkezett.
Exo and Endothermikus rendszer • Ha hőcsere kíséri a folyamatot. • Exothermikus: Ha hőmennyiséghagyja el a rendszert (a környezetbe). • Endothermikus: Ha hőmennyiség kerül bea rendszerbe (a környezetből).
A TERMODINAMIKA ELSŐ TÖRVÉNYE • A termodinamika első törvénye: Az univerzum energiája állandó.
A termodinamika I. főtétele: • Zárt rendszer belső energiája állandó, amíg azt munkavégzés vagy hőcsere nem változtatja meg. • A rendszer belső energiájának változását a végzett munka és a hőcsere mértéke adja meg:ΔU= q + w (rendszercentrikus előjellekkel). • A belső energia ΔU megváltozása csak a kezdeti és végállapottól függ: ΔU= Uf – Ui. (= állapot függvény) • Az energiamegmaradás elve: energia a semmiből nem keletkezik és nem semmisülhet meg. • I. fajú perpetum mobile nem készíthető. • Nem levezethető: általános, kivétel nélküli tapasztalat!
Az első főtétel • U = q + w • U = a rendszer belső energiájának megváltozása • q = hőmennyiség változás • w = munkavégzés
Az U és H:állapotfüggvényés extenzívsajátság. Abszolút értékük nem ismert, változásaikat számítjuk. Egységeik: 1Nm = 1joule(J) 1cal = 4,184 J Extenzív sajátság: értéke függ a rendszer anyagmennyiségétől
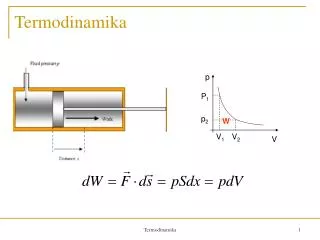
Térfogati munka Munkavégzés = hasznos munka + térfogati munka • wrendszer = PV
Entalpia • Entalpia = H = U + PV • U = HPV • H = U + PV • Állandó nyomáson, qP = E + PV, aholqP = Hállandó nyomáson • H = hőmennyiség változás (ha a nyomás állandó)
Hőkapacitás • C = átadott hőmennyiség / hőmérséklet változás = J/K • Specifikus hőkapacitás hőkapacitás per gram = J/°C g vagy J/K g • Moláris hőkapacitás hőkapacitás per mol = J/°C mol vagy J/K mol
Hess Törvénye • ReagensekTermékek • Az entalpia változásfüggetlen attól, hogy a reakció egy vagy több lépésben játszódik-e le.
Számítások a Hess törvény segítségével • 1. Ha a reakciót a fordított irányba írjuk fel, Hértéke szintén ellentett. • N2(g) + O2(g) 2NO(g) H = 180 kJ • 2NO(g) N2(g) + O2(g) H = 180 kJ • 2. Ha a reakció koefficienseket megszorozzuk egy számmal, aH-t is ugyanazzal a számmal szorozzuk. • 6NO(g) 3N2(g) + 3O2(g) H = 540 kJ
Standard Képződési Entalpia Az az entalpiaváltozás mely azt a reakciót kíséri mikor egy mól standard állapotú anyag standard állapotú elemeiből képződik. Hfo
Az entalpia változás számítható • Egy reakció entalpia változásakiszámítható a reagensek és a termékek képződési entalpiáiból. • Hreakció° = npHf(produktumok) nrHf(reagensek)
Spontán Folyamatok • Spontán folyamatok azok, melyek bárminemű külső beavatkozás nélkül önmaguktól is végbemennek. • A Bféltekében levő gáz a csap kinyitása után spontán megoszlik A és B között. Magától sohasem húzódik vissza a B edénybe.
Spontán folyamatok A szög spontán megrozsdásodik, a folyamat visszafelé önként nem megy végbe.
Spontán folyamatok • Egy adott hőmérsékleten spontán lezajló folyamat más hőfokon önmagától esetleg nem zajlik le. • A víz 0C felett önmagától megolvad. • 0C alatti hőmérsékleten a fordított folyamat (megfagyás) az amelyik önmagától lezajlik.
Reverzibilis folyamat A reverzibilis folyamatban a változás infinitézimálisan kicsiny behatással visszafordítható az eredeti állapotba. Egyensúlyi állapotokon megy át a rendszer.
Irreverzibilis folyamat • Irreverzibilis folyamatok nem fordíthatók meg energiabefektetés nélkül. • Minden SPONTÁN folyamat irreverzibilis. • Minden a valóságban végbemenő folyamat irreverzibilis.
Entrópia • Az entrópia (S) fogalmát Rudolph Clausius vezette be a 19. században. • Az entrópia állapotfüggvény, változása kiszámítható S = SvégállapotSkezdet
Entrópia • Állandó hőmérsékleten lezajló folyamatra: • ΔS ≥ qrev / T qrev = az izoterm reverzibilis folyamatban átment hőmennyiség. T = hőmérséklet Kelvin fokokban.
Entrópia • A statisztikus termodinamikai megfontolás szerint az entrópia a rendszer rendezetlenségének mértéke, ami a molekulák mozgásához kapcsolható. • S= klnw, ahol w= a mikroállapotok számával.
A termodinamika második főtétele Az univerzum entrópiája reverzibils folyamatokban nem változik, míg spontán (irreverzibils) folyamatokban mindig nő. Reverzibilis (ideális): ΔSuniverzum =ΔSrendszer +ΔSkörnyezet = 0 Irreverziblis (valódi, spontán): ΔSuniverzum =ΔSrendszer +ΔSkörnyezet> 0
A termodinamika második főtétele Az univerzum entrópiája valódi, spontán folyamatokban mindig nő. Ugyanakkor a rendszer entrópiája csökkenhet is, ha a környezet entrópia növekedése túlkompenzálja azt. Reverzibilis (ideális): ΔSuniverzum =ΔSrendszer +ΔSkörnyezet = 0 Irreverziblis (valódi, spontán): ΔSuniverzum =ΔSrendszer +ΔSkörnyezet > 0
Entrópiamolekulárisszinten • Ludwig Boltzmann megalkotta az entrópiaértelmezését molekuláris szinten. • A minta hőmérséklete a benne levő molekulák kinetikus energiájának a mértéke.
Entrópiamolekulárisszinten • A molekulák többféle mozgást végeznek: • Transzlációs. • Vibrációs. • Rotációs.
Entrópiamolekulárisszinten • Boltzmann elképzelte a molekulák mozgásának eloszlását egy adott idő pillanatban (mintegy fénykép) és azt az adott termodinamikai rendszer egy mikroállapotának nevezte el
Entrópiamolekulárisszinten • Mindenegyes termodinamikai állapotot így meghatározott számú mikroállapot (w) jellemez. • Az entrópiaígy S = k lnw aholka Boltzmann állandó, 1.38 1023 J/K.
Entrópiamolekulárisszinten Következtetések • több partikulum -> több állapot-> magasabb entrópia • magasabb T -> több energiaállapot-> magasabb entrópia • nagyobb mozgási szabadság(szilárd-gáz átmenet ) -> több állapot-> magasabb entropia
Entrópiamolekulárisszinten • A mikroállapotok száma és így az entrópia nő, ha nő a • hőmérséklet. • térfogat (gázok). • egymástól függetlenül mozgó részek száma.
Entrópiaés a rendszer fizikai állapota • Az entrópia nő, ha a részecskék mozgási szabadsága nő. • Ezért, S(g) > S(l) > S(s)
Oldatok entrópiája Sók feloldása: Ionoknak magasabb az entrópiája (több állapot ) Ugyanakkor, A hidrátburkot kialakító víz molekulák entrópiája csökken.
Entrópia növekedésel jár • Folyadék forrása, szublimáció. • olvadás. • Ha a gázmolekulák száma nő. • Ha a rendszerben levő mólok száma nő.
A termodinamika harmadik főtétele Egy szabályos kristály entrópiája 0, az abszolút nulla fokon.
A termodinamika harmadik főtétele http://www.garageband.com/artist/entropy_1
Standard Entrópiák • A táblázat különböző standard állapotú anyag moláris entrópia értékeit tartalmazza. • A standard entrópia értékek nőnek a molekula tömeg növekedésével.