ATOM
Střední odborná škola a Střední odborné učiliště Čs. armády 777 399 01 Milevsko www.issou-milevsko.cz. ATOM. Anotace a metodické pokyny: Tato prezentace je určena pro výuku předmětu Chemie ve 2. ročníku. Tento předmět je součástí bloku RVP –

ATOM
E N D
Presentation Transcript
Střední odborná škola a Střední odborné učiliště Čs. armády 777 399 01 Milevsko www.issou-milevsko.cz ATOM
Anotace a metodické pokyny: Tato prezentace je určena pro výuku předmětu Chemie ve 2. ročníku. Tento předmět je součástí bloku RVP – přírodovědné vzdělávání. Nejprve si řekneme, co je to atom. Probereme historii poznání atomu, základy atomistické teorie a objevy v 19. století. Projdeme stavbu atomu a jeho vlastnosti. Str. 5 – obrázky – Démokritos, Leukippos. Str. 7 – obrázek – Marie Curie Sklodowská. Str. 9 – obrázek – schéma rozdělení částic chemických látek. Str. 10 – schéma elektronového obalu. Str. 11 – na kliknutí – odpuzování, přitahování el. nábojů. Str. 12- na kliknutí obrázek k otázce. Str. 13 – využijeme při úkolu funkci pera v Office 2010.
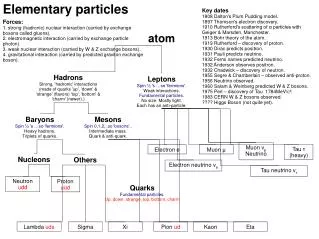
základní částice hmoty • částice, která už chemickými prostředky dále nelze dělit
HISTORIE • řecký filozof Démokritos, Leukippos • hmota se skládá z malých nedělitelných částic • atom ( z řeckého átomos = nedělitelný) Obr. Obr.
Základy klasické atomistické teorie • atomy jsou základními a dále nedělitelnými částicemi hmoty • existuje právě tolik atomů, kolik je chemických prvků • chemické sloučeniny vznikají spojením různých prvků
Objevy v 19. století • John Dalton – změna základů nauky o vnitřní stavbě hmoty • výzkumy: Antoine H. Becquerel (1896) Marie Curie – Sklodowská (1898) Joseph J. Thomson Ernest Rutherford Obr.
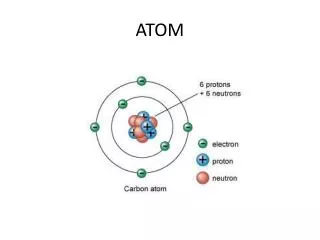
Vlastnosti atomu • definuje vlastnosti daného chemického prvku • skládá se z atomového jádra ( protony, neutrony) a obalu (elektrony) • elektricky neutrální • jsou chemickými vazbami vázány do molekul
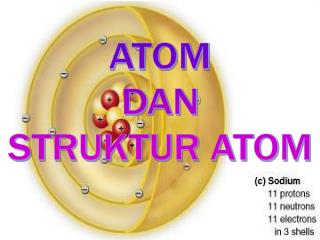
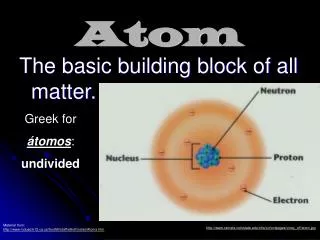
Složení atomu Obr. JÁDRO ATOMU • 99,9 % hmotnosti atomu • skládá se z nukleonů – protonů a neutronů PROTON • pozitivní náboj • hmotnost 1 836krát > elektron NEUTRON • elektricky neutrální • hmotnost o málo větší než proton
ELEKTRONOVÝ OBAL • obklopuje atomové jádro • zaujímá většinu prostoru atomu Elektrony • tvoří obal • má záporný elektrický náboj • hmotnost elektrického obalu je přibližně 0,01% celkové hmotnosti atomu Obr.
Elektrické náboje • stejné = odpuzují se • různé = přitahují se
Napište počet protonů, elektronů a neutronů v následujících atomech p = e = n = p = e = n = p = e = n =
ZDROJE • Obrázky z klipartu Microsoft Power Pointu 2010 • BLAŽEK, Jaroslav; FABINI, Ján. Chemie pro studijní obory SOŠ a SOU nechemického zaměření. Praha: SPN, 1999, ISBN 80-7235-104-4.