白血病 ( Leukemia)
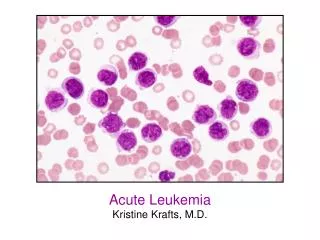
白血病 ( Leukemia). 血液内科 苏国宏. 定义. 是一类造血干细胞的恶性克隆性疾病,其克隆中的白血病细胞增殖失控、分化障碍、调亡受阻,而停滞在细胞发育的不同阶段。它由于血细胞中,主要是白细胞某一系列细胞异常肿瘤性增生,并在骨髓、肝、脾、淋巴结等各脏器广泛浸润,外周血中白细胞有质和量的异常,红细胞与血小板数量减少,导致贫血、出血、感染、浸润等征象。. 急性白血病( AL) : 细胞分化停滞在较早阶段,多为原始细胞及早期幼稚细胞,病情发展迅速,自然病程仅几个月。 据受累细胞系列分为:急非淋( ANLL) 急淋 ( ALL).

白血病 ( Leukemia)
E N D
Presentation Transcript
白血病(Leukemia) 血液内科 苏国宏
定义 • 是一类造血干细胞的恶性克隆性疾病,其克隆中的白血病细胞增殖失控、分化障碍、调亡受阻,而停滞在细胞发育的不同阶段。它由于血细胞中,主要是白细胞某一系列细胞异常肿瘤性增生,并在骨髓、肝、脾、淋巴结等各脏器广泛浸润,外周血中白细胞有质和量的异常,红细胞与血小板数量减少,导致贫血、出血、感染、浸润等征象。
急性白血病(AL):细胞分化停滞在较早阶段,多为原始细胞及早期幼稚细胞,病情发展迅速,自然病程仅几个月。急性白血病(AL):细胞分化停滞在较早阶段,多为原始细胞及早期幼稚细胞,病情发展迅速,自然病程仅几个月。 据受累细胞系列分为:急非淋(ANLL) 急淋 (ALL) 慢性白血病(CL):细胞分化停滞在较早阶段,多为较成熟幼稚细胞和成熟细胞,病情发展缓慢,自然病程数年。 据受累细胞系列分为:慢粒 (CML) 慢淋 (CLL) 少见类型 分类(据白血病细胞的成熟程度和自然病程)
发病情况 • 1.发病率2.76/10万。 2.AL>CL; ANLL>ALL CML>CLL 3.男性>女性; 成人ANLL多见,儿童ALL 多见。 4. CML随年龄增长发病率增高。CLL50岁以后发病明显增多,我国CLL比欧美少见,5%:25%-30%。
病因及发病机制 1.病毒:成人T-白血病/淋巴瘤可由T淋巴细胞病毒I型(HTLV-1)所致。其他如EB病毒、HIV病毒。病毒感染 整合并潜伏在宿主细胞 某些理化因素激活表达诱导白血病。 2.电离辐射:X、γ射线,电离辐射 早期放射科医生发病率>非放射科医生 日本原子弹爆炸、放疗。 机制:骨髓抑制、免疫力下降、DNA突 变、断裂、重组导致发病。
3.化学因素:苯类及含苯的有机溶剂 药物:乙双吗啉,烷化剂 4.遗传因素:家族史 5.其他血液病转化:MDS、淋巴瘤、多发性骨髓瘤、CML急变。 • 发病机制:1.各种原因所致单个细胞原癌基因决定性的突变导致克隆性的异常造血细胞生成(由理化因素引起) 2.遗传易感、免疫力低下、病毒感染、染色体畸变。通过遗传学改变可能涉及一个或多个癌基因激活,抑癌基因失活,从而导致白血病。
一、分类 • MICM分型: M—morphology 形态学 I—immunology 免疫学 C—cytogenetics 细胞遗传学 M—molecular biology 分子生物学
形态学分类 • AML分为M0-M7共8型 NEC:非红系有核细胞,指不包括浆细胞、淋巴细胞、组织嗜碱细胞、巨噬细胞及所有红系有核细胞的骨髓有核细胞。 M0(急性髓细胞白血病微分化型) 骨髓原始细胞>30%,无嗜天青颗粒及Auer小体,核仁明显,CD33或CD13髓系标志(+),淋巴系表达(-),髓过氧化物酶(MPO)<3%,血小板抗原(-)。 M1(急性粒细胞白血病未分化型) 原粒细胞≥90%NEC,MPO(+)>3%。 M2(急性粒细胞白血病部分分化型)
M2a:原粒细胞30~89%,粒细胞>10%,单核细胞<20% • M2b:骨髓中原始及早幼粒细胞增多,但以异常的中性中幼粒细胞为主,有明显的核浆发育不平衡,核仁常见,此类细胞>30%。 • M3(急性早幼粒细胞白血病) 以颗粒增多的异常早幼粒细胞增生为主, >30%NEC,胞核大小不一,胞浆中有大小不等的颗粒。 M3a:粗颗粒型;M3b:细颗粒型。 M4(急性粒-单核细胞白血病) 原始细胞>30%NEC,粒系30 ~ 80%,单核>20%。 M4a:原始+早幼粒细胞增生为主, 原幼单+单核细胞>20%NEC
M4b :原幼单核细胞增生为主, 原粒+早幼粒>20%NEC M4c:原始细胞既有粒系又有 单核系细胞特征,>30%NEC M4Eo:嗜酸颗粒粗大的嗜酸粒细胞>5%NEC M5(急性单核细胞白血病) 单核细胞(原+早+成) ≥80%NEC M5a:原幼单≥80% M5b:原幼单<80% M6(急性红白血病)骨髓中幼红细胞≥50%
由于形态学不能区分T、B细胞,M0、M7或形态偏差,采用I、C、M协助诊断由于形态学不能区分T、B细胞,M0、M7或形态偏差,采用I、C、M协助诊断 • 免疫学:髓细胞早期分化抗原: CD34、CD33、CD31、CD13、HLA-DR 髓细胞晚期分化抗原: CD15、CD14、CD11b、CD11c T细胞标志:CyCD3、CD7、CD2、及 CD1、CD5、CD4、CDIa 非T细胞标志:CyCD22、CD19、CD10 CD20、CD24、
临床常见的MICM分型 • AML、ALL、CML t(9;22)BCR/ABL基因 • M2: CD33、CD15、CD34、CD13 t(8;21) AML/ETO基因 • M3: CD 13、CD33、HLA-DR(-) t(15;17) PML/RARα基因 • M4E0: CD34.33.15.14.13 inv(16) CBFβ-MYH11基因 • L3(B-cell) CD10, t(8;14) MYC-IgH基因
二、临床表现 • 临床症状:感染、贫血、出血、浸润。 • (一)正常骨髓造血功能受抑表现 1.贫血:急性起病可无贫血。症状…. 2.发热:半数为早期表现,可低热、高热合并感染。感染可发生在各个部位:以口腔炎、牙龈炎、咽峡炎;肺感染、肛周炎、肛旁脓肿常见。 致病菌: a.细菌:G-杆菌,如绿脓、肺炎克雷白、大肠杆菌多见,G+球菌,如金葡菌、表皮葡萄球菌、粪链球菌、肠球菌等。
b.真菌:白细胞功能低下、长期抗生素。 白念、曲霉等。呼吸道,消化道等。 c.病毒:单纯疱疹、带状疱疹、巨细胞病毒 3.出血:皮肤、鼻、口、月经、眼底、肺、消化道、颅内出血。APL—DIC出血表现重。AL多死于出血(62.24%),87%颅内出血死亡。 (二)白血病细胞增殖浸润 1.淋巴结和肝脾肿大:ALL多淋巴结肿大,T-ALL纵隔淋巴结大,肝脾多中度大,CML急变可脾大明显。 2.骨骼和关节:胸骨压痛,儿童关节骨骼疼痛,骨髓坏死时可巨痛。 3.眼部:粒细胞AL眼眶部骨膜浸润(绿色瘤),可眼球突出、复视、失明。
4.口腔、皮肤:M4、M5可牙龈增生肿胀;皮肤表现灰色斑丘疹,局部隆起变硬,呈紫兰色结节。 4.口腔、皮肤:M4、M5可牙龈增生肿胀;皮肤表现灰色斑丘疹,局部隆起变硬,呈紫兰色结节。 5.CNSL: ALL多见,儿童较多;M4、M5、M2其次。血脑屏障。症状…. 6.睾丸:血睾屏障。多为单侧无痛性肿大。 7.其他:心、肺、消化道、泌尿生殖系等。
三、实验室检查 1.血常规:WBC升高(多见)、正常、降低;血涂片可见幼稚细胞;贫血(正细胞性);血小板降低。 2.Bm:主要检查、依据。 3.细胞化学:POX、PAS、NAP 4.免疫学检查: 5.染色体、基因。 6.血液生化:高WBC-高尿酸;M3-DIC;LDH;CNSL脑脊液…..
四、诊断与鉴别诊断 1.MDS:病态造血,幼稚细胞<20% 2.感染引起WBC异常:类白反应、病毒感染-淋巴细胞增高,传单-异淋 3.巨幼贫:红系增生-M6。 4.粒缺恢复期:原幼粒增多(无Auer小体),病因明确,血小板正常,短期内粒系恢复正常,无染色体异常。
五、治疗 (一)一般治疗: 1.高白细胞血症:白细胞淤滞(>20万)呼吸困难、呼吸窘迫、低氧血症,反应迟钝、言语不清、颅内出血,阴茎异常勃起。防止高尿酸、酸中毒、电解质紊乱等。处理:白细胞分离,水化、碱化,化疗药物,ALL-DEX;AML-HU。 2.防治感染:粒细胞减少所致, 层流、隔离病房 升高WBC….. 抗生素…… 3.成分输血支持 4.防尿酸肾病:别嘌呤醇,尿量 5.维持营养
(二)抗白血病治疗 治疗策略 1.诱导缓解治疗:化疗迅速达CR(指白血病症状、体征消失,外周粒细胞大于1.5,BPC正常,Bm正常… 2.缓解后治疗:争取长期无病生存和治愈,初治时WBC1010-1012, CR时降至108-109 并髓外浸润可能 巩固化疗,HSCT 复发
ALL: 诱导方案:VP、VDCP、VDLP、 VDCP+L-ASP VCR.. ,DNR..,CTX..,Pred.. 巩固治疗:HD-MTX、HD-Ara-c、 EA、MA、 复发难治:Flu,造血干细胞移植 CNSL治疗..
AML治疗: 诱导:除M3外,DA、HA M3:维甲酸、亚砷酸 巩固:HD-Ara-c,副作用:皮疹,皮肤充血、松解、剥脱,发热,球结膜充血,小脑共济失调。 MA、AA等 复发难治:Flu、IDA.. (三)其他:干细胞移植、免疫治疗
预后:不经特殊治疗,平均生存期3个 月左右,较重者数天死亡。 预后较好:APL,早期… ALL(1-9岁儿童)WBC<5万 无CNSL, inv(16) t(8;21)、t(15;17) 预后较差:年龄大、高白细胞 ALL有t(9;22) 继发放、化疗,MDS转化 复发、难治 髓外浸润
慢粒(CML)发生在早期多能干细胞上的恶性骨髓增殖性疾病,病程缓慢,主要涉及髓系,外周血粒细胞显著增多并有不成熟性,脾大,Ph染色体阳性,BCR/ABL融合基因(+),中位生存期3~5年。分为CP、AP、BP三期。慢粒(CML)发生在早期多能干细胞上的恶性骨髓增殖性疾病,病程缓慢,主要涉及髓系,外周血粒细胞显著增多并有不成熟性,脾大,Ph染色体阳性,BCR/ABL融合基因(+),中位生存期3~5年。分为CP、AP、BP三期。
临床表现 (一)慢性期: 代谢亢进症状:乏力、发热、多汗、盗汗 脾大:左上腹坠胀感,巨脾达脐下,质硬;脾栓塞时脾区压痛明显,脾摩擦音 胸骨压痛,白细胞淤滞。 CP一般持续1~4年 (二)加速期: 发热、虚弱、体重下降、骨骼疼痛,逐渐贫血、出血,脾进行性肿大 ,原药物治疗无效。AP维持几个月~数年。 (三)急变期: CML终末期,临床表现同AL。多急粒变、可(少)见急淋、急单变,偶有巨核、红细胞类型急变。预后差,数月死亡。
实验室检查 (一)慢性期: 1.血常规:WBC>2万,血涂片粒细胞显著增多,可见各阶段粒细胞,以中性中幼、晚幼、杆状粒细胞为主,原始细胞<10%,嗜酸、嗜碱 增多。血小板正常或增多,晚期血小板减少、贫血。 2.NAP:活性减低/阴性。 3.BM:增生明显或极度活跃,以粒系为主,粒/红增高,以中性中幼、晚幼、杆状粒细胞为主,原始细胞<10%,嗜酸、嗜碱 增多;红系减少;巨核正常/增多,晚期减少。 4.生化:血、尿尿酸增高,LDH升高
5.细胞遗传学、分子生物学: 90%Ph染色体t(9;22)(q34;q11),产生BCR/ABL基因,编码P210蛋白,其具有酪氨酸激酶活性,导致CML发生。 (二)加速期: 1.血/骨髓原粒≥10% 2.外周血嗜碱>20% 3.不明原因血小板减少/增加 4.出现Ph染色体以外的其他染色体异常 5.CFU-GM培养集簇增加、集落减少 6.Bm活检示胶原纤维显著增加。 (三)急变期1.Bm原粒、原幼单/淋>20% 2.原+早>30%(BL)/>50%(Bm)3.髓外浸润
诊断及鉴别诊断 • 症状、体征、血常规、Bm、Ph染色体 • 鉴别: 1.脾大:肝硬化、脾亢、疟疾、血吸虫 等均脾大。但无血常规、Bm、 Ph染色体异常。 2.类白反应:严重感染、恶性肿瘤等引 起白细胞增高、细胞出现中毒颗 粒、空泡,无嗜酸、嗜碱增高, NAP(+),Ph(-),BPC、Hb 正常,随治疗类白反应消失。
3.MF:与CML均有脾大、WBC增高、 幼粒细胞。 不同:WBC计数低于CML, NAP(+),可见幼红细胞 红细胞形态异常可呈泪滴形 Ph(-),穿刺干抽, 活检示网状纤维增加,染色 阳性
治 疗 • 慢性期治疗: (一)WBC增高处理:去除、水化、碱化 (二)化疗: 1.HU:为细胞周期特异性抑制DNA合成药 物,起效快、持续短,停药后WBC 升高快。1.0 Bid PO。据血象调整 用药。 2.马利兰(白消安):烷化剂 用药2-3周后WBC下降,停药2-4周可恢 复WBC,骨髓抑制、WBC恢复缓慢,副 作用多,不常用。 3.其他:H、Ara-c、CTX、砷剂、异靛甲
(三)α-干扰素: 机制:1.通过直接抑制DNA多聚酶活性 和干扰素调节因子的基因表达, 从而影响自杀因子(Fas)介导 的凋亡; 2.增加Ph(+)阳性细胞HLA分子 的表达量,有利于抗原递呈细 胞和T细胞更有效地识别。 剂量:300万单位 ih 隔日一次 大于6个月 疗效:50-70%获血液学完全缓解(HCR): 血象、骨髓象恢复正常 10-26%获显著细胞遗传学缓解MCR: Ph+细胞<35%,但BCR/ABL融 合基因(+),可延长生存期
不良反应:类流感症状,畏寒、发热、 疲劳、头痛及肌肉、骨骼疼痛,多能 耐受,可用解热镇痛药物治疗、预防。 (四)伊马替尼:格列卫、STI571 机制:2-苯胺嘧啶衍生物,能特异性阻断ATP 在ABL激酶上的结合位置,使酪氨酸的残 基不能磷酸化,从而抑BCR/ABL阳性细胞 的增殖;也能抑制另外两种酪氨酸激酶 C-Kit和血小板衍化生长因子受体的活性。 剂量:400-600mg/d 顿服 不良反应:1.血象下降较常见 2.非血液:恶心、呕吐、腹泻、肌 肉痉挛、水肿、皮疹等
疗效:CP:HCR 98% MCR 83% CCR(Ph+为0) 68% IFN- α不能耐受、治疗失败 HCR 95% MCR60% CCR41% (五)ALLO-SCT 根治性治疗办法,需HLA配型,一般年龄45岁以下。HLA相合同胞移植,3-5年无病生存率60-80%。
CML晚期治疗 1.AP:Allo-SCT、伊马替尼、干扰素+联 合化疗 2.BP:AML;ANLL;伊马替尼 Allo-SCT:复发率高60%,长期 DFS15-20%。 五、预后:化疗后中位生存期39-47个月 5年生存率25-35% 8年生存率8-17% 个别生存10-20年。
CLL是由于单克隆小淋巴细胞凋亡受阻,存活时间延长而大量积聚在骨髓、血液、淋巴结和其他器官,最终导致正常造血功能衰竭的低度恶性疾病。这类细胞在形态上类似成熟淋巴细胞,是一种免疫学不成熟的、功能不全的细胞。CLL是由于单克隆小淋巴细胞凋亡受阻,存活时间延长而大量积聚在骨髓、血液、淋巴结和其他器官,最终导致正常造血功能衰竭的低度恶性疾病。这类细胞在形态上类似成熟淋巴细胞,是一种免疫学不成熟的、功能不全的细胞。 • CLL绝大多数起源于B细胞,T细胞少见。欧美常见,亚洲(我国)少见。
临床表现 • 多系老年,男性多于女性,90%患者在50岁以上发病,起病缓慢,往往无自觉症状,因其他疾病就诊时发现。 • 早期症状:乏力、疲倦。 • 后期症状:消瘦、食欲减退、低热、盗汗、贫血。 • 常以淋巴结肿大为首发表现:占60-80%,浅表…深部…淋巴结无压痛、质地中等、可移动。
50-70%轻中度脾大 ,轻度肝大、胸骨压痛少见。 • 晚期患者出现贫血、血小板减少的表现 • T-CLL可皮肤增厚、结节、全身红皮病等表现。 • 免疫功能低下、合并感染。8%患者自免溶贫。
实验室检查 • 血象:持续淋巴细胞增多,WBC大于1 万,淋巴细胞50%以上,绝对值 大于5千(持续4周),小淋巴细 胞为主,中性粒细胞减少。晚期 贫血、血小板减少。 骨髓:增生活跃,淋巴细胞大于40%, 成熟淋巴细胞为主,红系、粒系、 巨核系均减少,溶贫时幼红细胞 可代偿增生。
免疫表型:淋巴细胞呈单克隆性 多源于B细胞,CD10、22阴性 CD5、19、20、21阳性 2-5%T细胞CD2、3、4、8阳性 20%抗人球蛋白试验(+) 明显溶贫8% 染色体异常:50-80%存在。 预后好:13q-、正常核型。 预后差:12号染色体三体、11q- 17P-
诊断与鉴别诊断 • 据临床表现、血象、骨髓象、免疫表型 • 鉴别诊断: 1.病毒感染:淋巴细胞比例相对增多, 暂时性,抗病毒治疗好转。 2.淋巴瘤细胞白血病:淋巴瘤病史,多 与滤泡或弥漫性小裂细胞淋巴瘤 混淆,CD5(-)。 3.幼淋巴细胞白血病(PLL):起病急,脾大 明显,淋巴结肿大较少,血、骨髓涂片 中有较多带核仁的幼淋巴细胞。
4.毛细胞白血病(HCL):全血细胞减少伴脾大,部分HCL白细胞升高。细胞特点:纤毛状胞浆突出物,酒石酸抵抗的酸性磷酸酶染色反应阳性。CD5(-),高表达CD25、11c、103。 4.毛细胞白血病(HCL):全血细胞减少伴脾大,部分HCL白细胞升高。细胞特点:纤毛状胞浆突出物,酒石酸抵抗的酸性磷酸酶染色反应阳性。CD5(-),高表达CD25、11c、103。 5.伴循环绒毛淋巴细胞的脾淋巴瘤(SLVL) 为原发脾恶性肿瘤,多发于老年人,脾大明显,血、骨髓中出现数量不等的绒毛状细胞,1/2-1/3有血、尿单克隆免疫球蛋白增高。CD5、25、11c、103阴性, CD22、24阳性。脾切除有效,预后好。
临床分期 • Binet分期: 5个区域淋巴结:头颈、腋下、腹股沟、 脾、肝 血和骨髓中淋巴细胞增多 A:淋巴结肿大<3个区域。 10年 B:淋巴结肿大≥ 3个区域。 7年 C:除B外,有贫血或血小板减少。2年
治 疗 • A期:无需治疗,定期复查。 B期:外周血基本正常、无症状,不治疗,随诊。出现下列情况化疗: 1.体重减少≥10%、极度疲劳、发热、盗汗 2.进行性脾大 3.淋巴结肿大:>10cm 4.淋巴细胞增生>50%(2个月);倍增<6个月 5.AHIA、ITP激素治疗反应差 6.骨髓进行性衰竭:贫血、血小板减少。 C期:化疗。
化疗: 苯丁酸氮芥(CLB)4-8mg/m2.d 氟达拉宾(Flu)25-30mg/m2.d 联合化疗:CP、COP、CHOP FC:效果好,难治CLL 并发症治疗:感染(低丙球、中性粒缺乏、 老年),抗感染、输注丙球。 AIHA、ITP应用激素。
免疫治疗: 1.阿来组单抗:CD52单抗。 对肿瘤负荷高的淋巴结肿大者较差。 清除血液、骨髓中的CLL细胞 用于维持治疗较理想。 2.利妥昔单抗(美罗华):CD20单抗 与化疗药物联合使用,50mg/h起步 逐渐加量,防止过敏反应。 造血干细胞移植: 自体:4年50%复发 ALLO-SCT:长生存。老年人并发症多。 Flu为基础NST降低死亡率。 >
预后 • 病程长短不一,可长达10余年,平均3-4年。 • 主要死亡原因:骨髓衰竭导致严重贫血、出血、感染。