Adenovirus
Adenovirus. Adenovirus. Virus che infettano svariate specie e tessuti Isolati per la prima volta nel 1953 da tessuto di adenoidi umane messe in coltura. Classificazione Famiglia Adenoviridae , genus Mastadenovirus 51 sierotipi isolati dall’uomo

Adenovirus
E N D
Presentation Transcript
Adenovirus • Virus che infettano svariate specie e tessuti • Isolati per la prima volta nel 1953 da tessuto di adenoidi umane messe in coltura
Classificazione Famiglia Adenoviridae, genus Mastadenovirus 51 sierotipi isolati dall’uomo Adenoviruses sono ulteriormente classificati in 6 sottogruppi (A -F), in base alle proprietà emagglutinanti e alla omologia di DNA Patologie respiratorie: Sottogruppi B1,C,E Patologie oculari: Sottogruppi B,D,E Patologie intestinali (enteriti): Sottogruppo F (Sierotipi 40, 41) Patologie renali e urinarie: Sottogruppo B2
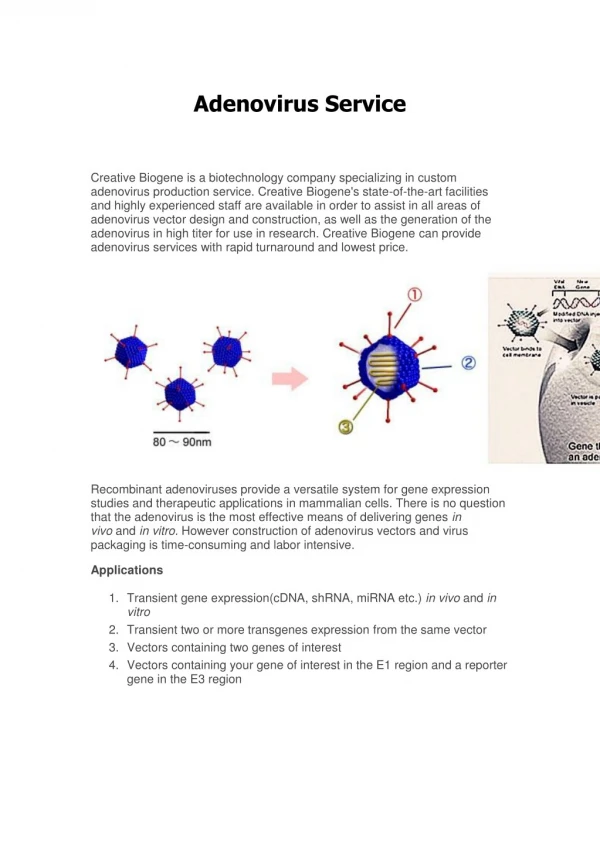
ADENOVIRUS Struttura Virus senza envelope Capside icosaedrico 70-90 nm Genoma: DNA lineare a doppia elica Capside 252 capsomeri: 240 esoni, 12 pentoni La fibra (IV) media il contatto con il recettore cellulare, protrudendo dal pentone (III) Pentoni (III) ed esoni (II) Proteine minori del capside (VI, VIII, IX) Core V, VII, Mu, IVa2, TP (terminal protein) associate al DNA virale Proteasi importante per l’assemblaggio
STRUTTURA capside costituito da 252 capsomeri di cui 240 esoni (trimero prot II + VI, VIII e IX) e 12 pentoni (pentamero prot III + 5 prot IIIa) core contiene almeno 4 proteine (TP, V, VII, Mu) ESONI: Determinanti antigenici PENTONI: Attività tossina-simile FIBRE (trimeri proteina IV): mediano il riconoscimento dei recettori sulla superficie delle cellule permissive (CAR, integrine); sono responsabili dell’emoagglutinazione
Adenovirusrecettori principali • Sottogruppo A (12,18,31)— proteina CAR (membro della superfamiglia delle Ig), funzione ignota, presente su molti tipi cellulari • Sottogruppo B • B1 (3,7,16,21,50) –CD46 (proteina regolatoria nel sistema del complemento), CD80, CD86 • B2 (11,14,34,35) • Sottogruppo C—CAR • Sottogruppo D—acido sialico
Altre molecole importanti 1) Le fibre si legano ai due al recettore primario: ex a CAR (coxackie/adenoviral receptor) 2) I motivi RGD presenti nel pentone si legano alle integrine avb3 e avb5
FASI del CICLO VITALE DI ADENOVIRUS 1° fase 2° fase • - Avviene nel nucleo delle cellule permissive (cellule di origine epiteliale), il ciclo ha una durata di circa 32-36 ore (ciclo litico) • Un unico ciclo di replicazione è in grado di generare 10.000 virioni per cellula infettata;
ADESIONE E ASSORBIMENTO • CAR è una proteina di adesione che è espressa ad alti livelli: • fegato, rene, cuore, cervello, pancreas, colon, prostata, endotelio • CAR non è espressa in: • linfociti periferici, milza, muscolo scheletrico e fibroblasti • Adenovirus del gruppo B riconoscono un recettore diverso dal CAR (CD46) • Adenovirus di tipo 5 riconosce come recettore anche il dominio α2 del MHC di tipo I • Alcuni tumori in stadio avanzato perdono l’espressione del CAR (es. ovarico, colon...) • Un dominio RGD esposto in un loop dei pentoni promuove l’interazione con le integrine promuovendo l’endocitosi • Il colesterolo gioca un ruolo nell’uptake virale e fuoriuscita dall’endosoma
Penetrazione nella cellula Ingresso mediato da endocitosi clatrina-dipendente/pH dipendente Perdita delle fibre Lisidella membrana degli endosomi mediato dalla proteina della base dei pentoni A livello dei pori nucleari la struttura capsidica subisce un disassemblaggio parziale : - perdita dei pentoni III e della proteina IIIa - dissociazione della proteina VIII - degradazione proteolitica dellaproteina VI da parte della proteasi presente nel virione -perdita della proteina IX pH
Genoma degli adenovirus • Il genoma è costituito da una molecola di DNA lineare a doppia elica di 30-40 kb, a seconda del gruppo preso in analisi. • Alle estremità sono presenti le sequenze ITRs, inverted terminal repeats, che fungono da origini di replicazione e da promotori per alcuni geni. • Vicino alla ITRs in 5’ vi è la sequenza segnale (sequenza Ψ) per l’inserimento del genoma all’interno del virione. • I geni vengono espressi con una precisa sequenza temporale (immediate-early, early, late genes). • I geni immediate-early sono E1A e E1B e servono ad innescare la replicazione nella cellula ospite. • I geni early servono per la replicazione del genoma virale • I geni late sono geni strutturali
ITR ITR SEQUENZE ITR (100bp) Il GENOMA degli ADENOVIRUS (ds DNA: 30-36 Kb) regione ORI (replicazione del genoma) regioni di controllo trascrizionale siti di legame per fattori trascrizionali e proteine enhancer cellulari : NF-I e Oct-I sequenza di impacchettamento
Rappresentazione schematica del genoma di adenovirus:ds DNA lineare di 36 kb • le regioni da E1 a E4 codificano i geni precoci (early) • le regioni da L1 a L5 codificano i geni tardivi (late) • Trascrizione bidirezionale mediata da RNA pol-II, si ottengono diversi mRNA grazie all’uso di diversi siti poli-A o per splicing alternativo
Rappresentazione schematica deli trascritti virali • Trascrizione bidirezionale mediata da RNA pol-II, si ottengono diversi mRNA grazie all’uso di diversi siti poli-A o per splicing alternativo
50 proteine geni precoci geni tardivi ESPRESSIONE GENICA degli ADENOVIRUS E- geni precoci L- geni tardivi
Regione E1: orientamento • Indurre la cellula ospite ad entrare nella fase S del ciclo cellulare • Sintetizzare i prodotti dei geni virali necessari per la replicazione del DNA virale • Down regola l’espressione dell’MHC I (effetto immuno regolatore) L’espressione di E1A fa sfuggire al normale controllo da parte dell’interazione pRb-E2F Co-immunoprecipitazione di numerose proteine cellulari con la proteina E1A
Regione E2 orientamento • suddivisa in 2 regioni trascrizionali • separate: E2A ed E2B. • la regione E2A codifica una proteina che lega ssDNA (DBP), altamente fosforilata nella regione N-terminale e richiesta per la replicazione del DNA: probabilmente funziona come fattore di regolazione della trascrizione. • la regione E2B codifica un precursore della proteina TP (80kDa) che viene convertita in una proteina di 55 kDa durante l’assemblaggio virale. Questa regione codifica anche una DNA polimerasi di 240kDa.
Regione E3(“cell death protein”) • codifica prodotti genici antiapoptotici e inibisce l’espressione di MHC • facilita il rilascio delle particelle virali dalle cellule infettate, • riduce la produzione di linfociti T citotossici E3 orientamento Promuove il rilascio del virus Funzione sconosciuta Funzione Sconosciuta Inibisce l’apoptosi Lega l’ MHC I Inibisce la trascrizione Inibisce l’apoptosi regolata da TNFa Agisce su NF-KB
Modula l’attività di E2F Funzione sconosciuta Facilita la trasformazione Interagisce con E1B 55K Interagisce con E1B 55K agevolando la produzione degli mRNA Inibisce l’attivazione di E2F mediata da E1A • Regione E4(modula il metabolismo dell’ospite!) • stimola lo sviluppo di una risposta umorale : aumentando IL6 e IL8 per la maturazione delle cellule B • modula l’attività di trascrizione del virus • inibisce la sintesi proteica dell’ospite. orientamento
Replicazione del genoma La replicazione del DNA avviene grazie all’intervento di pTP, polimerasi virale, DBP che interagiscono con altre proteine cellulari Entrambe le estremità del genoma fungono da origini Protein priming and strand displacement model
proteine strutturali proteine scaffold proteasi IVa 52 kd ESPRESSIONE DEI GENI TARDIVI VA ITR E1A/B E2A/B E4 ITR E3 L1 L2 L3 L4 L5 unico trascritto viene processato per formare circa 18 mRNA con estremità 5’ identiche, divisi nei 5 gruppi L E1A MLTF L1 L2 L3 L4 L5 promotore MLP
GENI TARDIVI Proteine tardive = componenti strutturali del virione • I geni tardivi sono trascritti a partire da un major late promoter (MLP) • A partire da un trascritto primario di 29.000 nucleotidi, circa 18 specie di mRNA sono prodotte in seguito a splicing alternativi, tali mRNA sono stati raggruppati in 5 famiglie classificate da L1 a L5 che hanno porzioni 5’ variabili • Altri RNA (VA) vengono generati dalla polimerasi III e si possono attribuire diverse funzioni a questi RNA: • - regolazione degli splicing degli mRNA tardivi • - controllo degli stadi della migrazione dei peptidi tardivi • - inibizione degli effetti dell’INF mediante blocco del legame dei dsRNA alle proteine chinasi cellulari Rappresentazione di un modello delle strutture secondarie (dsRNA) che si generano a livello dell’Ad-tipo2
Assemblaggio degli adenovirus • proteine singole(no poliproteina) • ruolo critico della proteina L1 • (funzione scaffold ?) • citoplasma • - formazione dei trimeri di proteina II (esoni). Funzione essenziale della proteina L4. nucleo - formazione dei pentameri di proteina III (pentoni) - formazione dei trimeri di proteina IV (fibre) formazione di capsidi vuoti
RILASCIO DEL VIRUS disaggregazione del citoscheletro della cellula ospite (L3 proteasi) E3 - death protein (meccanismo sconosciuto)
REPLICAZIONE E PATOGENESI Infezione delle cellule mucoepiteliali a livello del sito di ingresso ovvero della congiuntiva, del tratto respiratorio, gastrointestinale e genitourinario. Replicazione del DNA genomico intranucleare Fasi di replicazione precoci e tardive a cui segue l’assemblaggio e il rilascio dei virioni Danno diretto cellule mucoepiteliali ( tratto respiratorio, gastrointestinale, congiuntiva)
ADENOVIRUSINFEZIONE Tre tipi di infezione: • Litica – cellule mucoepiteliali, porta alla morte cellulare • Produzione di 10.000-1X106 virioni/cellula • 1-5% dei virioni sono infettivi • Latente / persistente – il virus permane in tonsille, adenoidi, placche di Peyers • Scarsa produzione virale
ADENOVIRUSINFEZIONE • Trasformazione oncogenica– crescita cellulare e replicazione senza morte cellulare. Integrazione del DNA Espressione costitutiva di geni E1A- E1B (importanti per immortalizzazione cellulare; inattivazione p53, Rb)
Patogenesi • Molto diffusi • Virus citolitici per effetto di accumulo dei virioni nel nucleo e per l’effetto citotossico di E3 (death protein) • Infezioni acute del tratto respiratorio e in misura minore gastro-intestinale, possono dare cistiti emorragiche, miocarditi e cheratocongiuntiviti • Molte infezioni sono subcliniche
ONCOGENESI • Soltanto alcuni sottogruppi di adenovirus possono indurre direttamente la formazione di masse tumorali nel topo: • Adenovirus del gruppo A (Ad12, Ad18,..) sono altamente oncogenici, e producono il tumore nella quasi totalità dei topi nell’arco di 4 mesi; • Adenovirus del gruppo B (Ad3, Ad7,..) sono debolmente oncogenici, inducono il tumore in 4-18 mesi. • Adenovirus del gruppo C eE non sono stati mai visti implicatinella induzione di tumori nell’animale.
E1A pRB g geni proliferativi a IKK E1A b IB E1B 19kd NF-kB risposta innata E1B 55kd p53 geni pro-apoptotici MECCANISMO DI TRASFORMAZIONE CAR integrine
ADENOVIRUSTRASMISSIONE • Aerosol • Contatto diretto • Oro-fecale • Eliminazione intermittente • Aree affollate • Diffusione mondiale • Diffusione interumana
ADENOVIRUSINFEZIONE • Adenovirus replica nei tessuti linfoide-associati, la viremia puo’ causare infezione secondaria in organi viscerali. • La replicazione del virus causa un eccesso di componenti antigeniche liberate nel sovranatante come antigeni solubili. Colorazione basofila intra-nucleare corpi inclusi nelle cellule.
Adenovirus Immunita’ • Infezioni controllate dalla risposta immunitaria • Risposta anticorpale e T cellulare
Manifestazioni cliniche Infezioni subcliniche nella maggior parte dei casi Infezione primaria avviene nell’infanzia Tipi 1,2,5,6 tipicamente isolati dal tessuto adenoide o tonsille dei bambini Isolato dalle feci 5% malattie neonato, 3 % tra i 2-4 anni di vita Frequente nelle caserme
Manifestazioni cliniche • Patologie respiratorie: Riniti, faringiti (con o senza febbre), tonsilliti, bronchiti, pertosse-simile, polmoniti • Patologia oculare: cherato-congiuntiviti • Patologie renali e urinarie: cistite emorragica, orchite, nefrite
Manifestazioni cliniche • Patologia intestinale (gastroenteriti): • diarrea per periodo più lungo che con altre infezioni virali, adeniti mesenteriche, epatiti, appendiciti (sierotipi 40,41,42) • Patologie più rare nell’individuo immunocompetente: Meningiti, encefaliti, artriti, rash cutaneo, mioocarditi, pericarditi: • Infezioni molto grave (o riattivazione infezione latente) in pazienti immunocompromessi
AdenovirusDiagnosi Ricerca del virus: • Metodi immunologici • Metodi molecolari • Isolamento colturale In campioni di sangue, secrezioni, tamponi nasali, tamponi oculari, feci, urine, liquor….