AGUA
460 likes | 725 Views
AGUA. H2O. Funciones del Agua. Aporta el líquido para las secreciones glandulares. Solvente de las reacciones químicas inorgánicas del cuerpo. Medio de transporte. Diluente para la digestión y absorción de los alimentos. Termorregulador. Mantiene la volemia. Mantiene la PA.

AGUA
E N D
Presentation Transcript
AGUA H2O
Funciones del Agua Aporta el líquido para las secreciones glandulares. Solvente de las reacciones químicas inorgánicas del cuerpo. Medio de transporte. Diluente para la digestión y absorción de los alimentos. Termorregulador. Mantiene la volemia. Mantiene la PA. Mantiene la función renal. Mantiene la concentración normal de electrolitos
AGUA Central para la bioquímica; Prácticamente todas las moléculas biológicas toman su forma, en respuesta a las propiedades físicas y químicas del agua que las rodea. El medio para la mayoría de las reacciones bioquímicas es el agua Participa activamente en muchas reacciones químicas que sostienen la vida, sus componentes ionicos,los iones H+ y OH- son los verdaderos reactivos
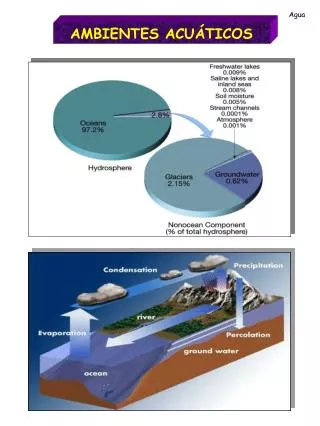
CAMBIOS DEL AGUA CORPORAL TOTAL Y DE LOS COMPARTIMIENTOS CORPORALESDURANTE EL DESARROLLO Es el componente mas abundante del cuerpo y constituye cerca del 60% del peso del adulto y desde 70% hasta 80% que tiene el neonato y el recién nacido prematuro Ocurre una disminución rápida del agua corporal total como porcentaje del peso del cuerpo durante el primer año de vida; desde el 75% al nacer, hasta cerca de 70% a los seis meses y de 60% al año de edad El porcentaje de agua corporal disminuye de manera gradual hasta que el niño llega a la pubertad El agua intracelular llega a una meseta de cerca de un 35% del peso corporal después que el niño cumple tres años El agua extracelular disminuye desde 45% del peso corporal al nacer hasta 35% a los 6 meses y hasta 27% al año
Cambios en los compartimientos corporales de agua con el paso de la edad El agua corporal total varia en proporción inversa al contenido de grasa del cuerpo ( la grasa no contiene agua) Los RN prematuros tienen un porcentaje de agua elevado, pues su grasa corporal es escasa Las mujeres adultas tienen un porcentaje de agua mas bajo de agua en comparación con los varones adultos(su contenido en grasa es mas elevado en promedio) La obesidad reduce el porcentaje de agua corporal y la delgadez lo incrementa
ESTRUCTURA MOLECULAR Esta formada por dos átomos de hidrogeno y uno de oxigeno Tiene una geometría tetraédrica debido a que su átomo de oxigeno tiene una hibridación SP3 En el centro del tetraedro se encuentra el átomo de oxigeno, dos de las esquinas están ocupadas por átomos de hidrogeno, cada uno de los cuales esta unido al átomo de oxigeno por un enlace covalente sencillo. Las otra dos esquinas están ocupadas por los pares de electrones del oxigeno sin compartir
ESTRUCTURA DEL AGUA La distancia del enlace O-H es de 0.958 A Los orbitales sp3 del o2 ordenados de manera tetraédrica Los átomos de hidrogeno no están ubicados de manera lineal, los cuatro orbitales híbridos sp3 del átomo de oxigeno se extienden hacia los vértices del tetraedro
CARGAS DE UNA MOLECULA DE AGUA • El oxigeno es mas electronegativo que el hidrogeno (tiene una capacidad mayor para atraer electrones cuando esta unido al hidrogeno) • El átomo de oxigeno mas grande lleva una carga negativa parcial, y cada uno de los átomos de hidrogeno llevan una carga positiva parcial • La distribución electrónica de los enlaces oxigeno-hidrogeno se desplaza hacia el oxigeno y por lo tanto el enlace es polar
MODELO DE RELLENO ESPACIAL Las moléculas de agua están dobladas con un ángulo de enlace de 104.5° Si las moléculas de agua fueran lineales , la polaridad de los enlaces se equilibraría y el agua seria apolar Debido a que la molécula de agua tiene una geometría doblada, la distribución de carga dentro de la molécula es asimétrica(es polar)
ENLACE DE HIDROGENO Debido a la gran diferencia de electronegatividad de el hidrogeno y el oxigeno, los hidrógenos con deficiencia de electrones de una molécula de agua son atraídos hacia el par de electrones sin compartir de otra molécula de agua Interacción conocida como enlace de hidrogeno(atracción débil entre un átomo electronegativo en una molécula y un átomo de hidrogeno en otra molécula)
PUENTE DE HIDROGENO EN EL AGUA La fuerza de interacción es máxima cuando el enlace covalente O-H la molécula apunta directamente hacia la nube de electrones del par libre de la otra
INTERACCIONES ELECTROSTATICAS Las interacciones no covalentes son normalmente electrostáticas(se producen entre el núcleo positivo de un átomo y las nubes electrónicas negativas de otro átomo cercano Las interacciones no covalentes individuales son realmente débiles y por lo tanto se rompen con facilidad Determinan las propiedades químicas y físicas del agua
PROPIEDADES DEL AGUA La mayoría de los compuestos de bajo peso molecular son gases a temperatura ambiente y tienen unos puntos de ebullición muy inferiores a los del agua Tanto el calor de evaporación como el punto de ebullición del agua son excepcionalmente elevados, y el agua permanece en estado liquido a temperatura ambiente
PROPIEDADES DEL AGUA En consecuencia del calor de vaporización ( energía que se requiere para evaporar un mol de un liquido a la presión de una atmosfera) y la capacidad calorífica(energía que debe añadirse o eliminarse para cambiar la temperatura un grado Celsius)elevados del agua es que esta actúa como un modulador eficaz de la temperatura climática Desempeña un papel importante en la regulación térmica de los seres vivos
EL AGUA COMO DISOLVENTE Funciona como un disolvente universal en los medios intracelulares y extracelulares La propiedad de disolvente surge gracias a; tendencia a formar enlaces de hidrogeno y su carácter dipolar Disolvente universal; debido a la gran variedad de sustancias iónicas y polares que puede disolver con una constante dieléctrica muy elevada(capacidad de un disolvente para reducir las fuerzas de atracción entre los iones)
LAS MOLECULAS HIDROFILAS EN UNA SOLUCION ACUOSA Las moléculas con grupos capaces de formar enlaces de hidrogeno tienden a unirse con el agua con este tipo de enlace; compuestos hidroxilicos,las aminas, grupos sulfihidrilo, los esteres , las cetonas y sustancias iónicas y polares (NaCl) se unen mediante fuerzas iónicas El agua al ser polar es atraída hacia los iones cargados como el Na y el Cl(hidrata los iones) Los caparazones de las moléculas de agua(esferas de solvatación)se agrupan alrededor de los iones positivos y negativos
PUENTES DE HIDROGENO SEGÚN LOS GRUPOS FUNCIONALES La solubilidad de las sustancias polares y iónicas se incrementa cuando llevan grupos funcionales como: Los grupos hidroxilo(OH) Carbonilo(C=O) Carboxilato(COO-) Amonio(NH4)
LAS MOLECULAS HIDROFOBAS EN UNA SOLUCION ACUOSA Las moléculas hidrófobas(aversión al agua); insolubles en agua No se forman capas de solvatación, se forman estructuras de clatrato o jaulas alrededor de moléculas no polares La tendencia del agua a reducir al mínimo su contacto con moléculas hidrófobas se denomina efecto hidrófobo
LAS MOLECULAS ANFIPATICAS(ANFIFILAS) EN UNA SOLUCION ACUOSA Moléculas anfipaticas;contienen grupos polares y apolares, muestran propiedades hidrófilas e hidrófobas al mismo tiempo Incluyen ácidos grasos y detergentes Tienen un grupo de cabeza muy hidrófilo, acoplado a una cola hidrófoba(generalmente un hidrocarburo) Constituyen la base de la membrana bicapa biológica que rodea las células
IONIZACION DEL AGUA Es una molécula fundamentalmente neutra, tiene la ligera tendencia a ionizarse(capacidad limitada) El agua puede puede actuar como un acido y tambien como una base Una molécula de agua puede transferir un protón a otra molécula de agua y dar un ion hidronio(H3O+)Y un ion hidroxilo(OH-) O bien en una ecuación mas sencilla; H2O +H2O=H3O + OH- H2O=H+ +OH-
DISOCIACION DE LA MOLECULA DEL AGUA EN SUS DOS ESPECIES IONICAS
IONIZACION DEL AGUA El protón de ion hidronio puede saltar rápidamente a una molécula de agua y luego a otra Las movilidades de los iones H+ y OH- en solución son mucho mayor que la de otros iones El salto de los protones explica del porque las reacciones acido básicas están entre las reacciones mas rápidas que tienen lugar en solución acuosa
LA IONIZACION(DISOCIACION) DEL AGUA Se describe como una expresión de equilibrio en la que la concentración de la sustancia madre esta en el denominador y la concentración de los productos disociados se encuentran en el numerador
CONSTANTE DE DISOCIACION La concentración de H2O sin disociar es mucho mayor que la concentración de los iones que la componen, puede considerarse constante e incorporarse en K para obtener una expresión para la ionización del agua
IONIZACION DEL AGUA El valor de Kw , la constante de ionización del agua es de 10 a la menos 14 a 25°c El agua pura debe de tener cantidades equimolares de H+ y OH-,por lo tanto [H+]=[OH-]=Kw(1/2)=10 a la menos 7 Se afirma que las soluciones con [H+]=10 a la menos 7 M son neutras, las que tienen [H+] mayor de 10 a la menos 7 M son acidas y las que presentan una [H+] menor de 10 al menos 7M son básicas
EL PH El PH de una disolución es una medida de la concentración de los protones; como los protones reaccionan con el agua para dar iones hidronio, se puede considerar el PH como la concentración de esta ultima
EL PH La acides de una solución se mide por la concentración de iones hidronio o protones , que presente. esta concentración abarca desde 1 molar en una solución muy acida , hasta una concentración de 14 molar en una solución muy alcalina o basica,para evitar el uso de números tan pequeños se deicidio convertir estas concentraciones a una escala logarítmica; escala logarítmica
LA [H+] Y [OH-] ESTAN INVERSAMENTE RELACIONADAS Los valores de [H+] para la mayoría de las soluciones son pequeños y por lo tanto no son prácticos para establecer comparaciones En 1909 Soren Sorenson propone el pH
RELACION ENTRE EL PH Y LA [H+] Y [OH-] La [H+] y [OH-] están inversamente relacionados Las soluciones con relativamente mas H+ son acidas(pH < 7) Las soluciones con relativamente mas OH- son básicas( pH > 7) Las soluciones en las cuales la [H+]= [OH-] son neutras (pH = 7)
BRONSTED-LOWRY ACIDO; Sustancia capaz de ceder un protón BASE; sustancia que puede aceptar un protón al reaccionar con el agua ANFOTERA; sustancia que puede comportarse como como acido y como base
MECANISMOS REGULADORES DEL PH La neutralidad del plasma y otros líquidos corporales es de vital importancia para el correcto funcionamiento de la célula Cambios mínimos en las cifras del PH representan variaciones en la concentración de iones hidrogeno, un descenso del PH de 7.41 a 7.1 repercute en un aumento del doble de la concentración de iones hidrogeno La presencia de grupos ionizables en moléculas biológicas como las enzimas , al cambiar de carga hace que esta pierda su actividad catalítica
pH (H) 80 40 ACIDEMIA 20 ALCALEMIA 7.4 7 7.5 7.6 7.2 7.35 7.45
FISIOLOGIA RENAL REGULACION DEL EQUILIBRIO ACIDO BASICOAMORTIGUACION DE LOS IONES HIDROGENO EN LOS LIQUIDOS CORPORALES • Amortiguador ; cualquier sustancia capaz de unirse de manera reversible a los iones hidrogeno ( H+ ) Amortiguador + H+Hamortiguador • Minimiza los cambios de la concentración de H+ • Ante la producción diaria a través del metabolismo de unos 80 mEq diarios de H+ Sistema amortiguador del bicarbonato Sistema amortiguador del fosfato Las proteínas amortiguadoras intracelulares
TAMPON O BUFFER Son sistemas que tienden amortiguar los cambios que se producen en el PH, cuando se añade una pequeña cantidad de acido(H+) o de base(OH-) Amortiguadores químicos; sistema bicarbonato/acido carbónico sistema de fosfatos sistema de proteínas sistema amortiguador de la hemoglobina mecanismo regulador respiratorio Mecanismo regulador renal