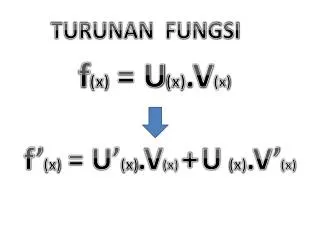
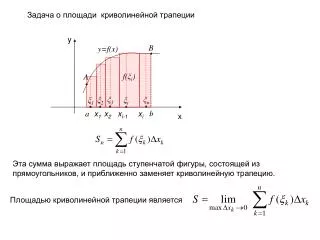
Cromossomo X
Cromossomo X . Mamíferos: fêmeas XX e machos XY inativação de um dos cromossomos X durante o desenvolvimento inicial. compensação de dose nas fêmeas. Inativação do X. Três “ondas” de inativação: Trofoectoderme Endoderme primitiva do blastocisto

Cromossomo X
E N D
Presentation Transcript
Cromossomo X Mamíferos: fêmeas XX e machos XY inativação de um dos cromossomos X durante o desenvolvimento inicial. compensação de dose nas fêmeas
Inativação do X • Três “ondas” de inativação: • Trofoectoderme • Endoderme primitiva do blastocisto Inativação sujeita ao impriting, exclusiva do X paterno (Xp) • Células do epiblasto originadas da massa de células interna (ICM) Inativação aleatória (Xp ou Xm) Tecidos extraembrionários
Xist • Responsável pela inativação do X. • RNA não traduzido. • Cobre o cromossomo X in cis. • Causa o silenciamento de genes do cromossomo X que cobriu. • Cromossomo X ativo: Xist inativo. • Cromossomo X inativo: Xist ativo.
Xist • Em células do tecido embrionário: • “encapamento” do cromossomo X pelo Xist é rapidamente seguido de silenciamento gênico. • Durante o desenvolvimento inicial: • Expressão do Xist a partir do estágio de duas a quatro células. • Expressão apenas de origem paterna. • Expressão do Xist materno: apenas no estágio de mórula.
Primeiros sinais citológicos detectáveis da inativação do X: apenas no estágio de cinquenta células. • Logo após a fertilização: Xm e Xp ativos. • Estudos com RT-PCR: alguns genes paternos já possuem transcrição diminuída na embriogênese inicial. • Predisposição do X paterno à inativação: devido à sua passagem pela linhagem geminativa masculina (vesícula sexual).
Muitas questões não resolvidas a respeito da iniciação e cinética da inativação do X
Metodologia • Exame do Xp “encapado” com Xist durante a embriogênese pré-implantação. • Embriões nos estágios de duas células até blastocisto. • Análise direta, sem cultura in vitro. • Hibridização in situ com RNA fluorescente (FISH). • Imunofluorescência.
Detecção de Xist • Acúmulo de Xist em todos os blastômeros interfásicos a partir do estágio de quatro células. • Estágio de duas células: pequeno sinal de Xist.
Estado inicial da cromatina no Xp • Fisch • Imunofluorescência H3K9 e H3K27 e interações com Eed e Enx1 características de cromossomos X em inativação * H3K9 está associada com o Xp durante a espermatogênese
Estado inicial da cromatina no Xp • Estágio de quatro a oito células: • Não há acumulação de H3 metilada em K9 ou K27.
Estágio de 16 células: • Detecção destes marcadores em alguns blastômeros.
Estado inicial da cromatina no Xp • Acumulação dos marcadores no Xp tem intervalo similar • Enx => metiltransferase de histonas que metila a K27 • H2A => acumula no mesmo intervalo de tempo que esses marcadores. Mudanças principais na cromatina do Xp começam neste estágio (16 células)
Estado inicial da cromatina no Xp • Proporção de blastômeros que contêm os marcadores varia nos estágios de 16 a 32 células. • Blastocisto: 90% dos blastômeros possuem os marcadores. * Metilação na H3K9 começa mais tarde (32 células) => marcador independente
Estado inicial da cromatina no Xp • Outras análises: • hipoacetilação da H3K9 • hipometilação da H3K4 • eventos iniciais na inativação do X em células de tecidos embrionários
4 células: nenhum sinal destas modificações • 8 células: detectados em alguns blastômeros
32 células: mais de 90% dos blastômeros • ocorrem após o “empacotamento” pelo Xist mas antes dos outros marcadores
Metodologia • Análise do silenciamento do Xp em nível transcricional em células únicas. • Anticorpo (H5): reconhece a forma elongadora da RNA PolII (presente em cromatina transcricionalmente ativa). • Em células ES em diferenciação: exclusão da RNA PolII do cromossomo X logo após o empacotamento pelo Xist.
Atividade transcricional do Xp • Em embriões na pré-implantação: • 2 células: não há exclusão da RNA polII.
4 células: primeiros sinais de exclusão. • 32 células: quase 100% de exclusão.
Atividade transcricional do Xp • Confirmação do silenciamento transcricional de Xp: • RNA FISH para detectar transcritos do gene Chic1/Brx do cromossomo X.
2 células: dois sinais de transcrição, um adjacente ao Xist em alguns embriões. • 8 células: um sinal dentro do domínio do Xist em alguns blastômeros. • 16 células: sinal não é mais visto em mais de um blastômero.
Atividade transcricional do Xp • Início da inativação da transcrição do Xp: • Estágio de quatro a oito células • Inativação do Xp: • No estágio de 32 células atinge a grande maioria dos blastômeros Inativação do X começa bem antes da diferenciação celular
Blastômeros contêm o Xp inativo • Exclusão de Pol II • Modificação de histonas • Associação de Eed/ Enx1
Blastômeros contêm o Xp inativo • Presença de RNA Xist • Presença de Eed e Enx1
Inativação de Xp no ICM • Imunocirurgia: retirada do trofoectoderma • Blastocistos no início: • Presença de RNA Xist • Exclusão de RNA Pol II • Hipoacetilação na H3K9 • Hipometilação na H3K4 • Metilação na H3K9 e K27 • Acumulação de Eed e Enx1
Inativação de Xp no ICMBlastocisto no início • Acumulação de Eed e Enx1
Inativação de Xp no ICM Blastocisto no início • Metilação na K27
Inativação de Xp no ICM • Blastocistos tardios: • RNA xist estava disperso ou ausente • Ausência de acumulação de Eed e Enx1 • Metilação na H3K27 • Blastocistos no início cultivados por 24hs • Presença de RNA xist e as características da mórula e trofoectoderma • Blastocistos tardios cultivados por 24hs • Perda de RNA xist, Eed e Enx
Inativação de Xp no ICMBlastocisto tardio • Ausência de acumulação de Eed e Enx1
Inativação de Xp no ICM Blastocisto tardio • Metilação na H3K27
Inativação de Xp no ICMBlastocisto em cultura • Presença de RNA Xist
Conclusão • Ciclo dinâmico da inativação de Xp Xp inativado – reativação – inativação randômica Esse estudo propõe que RNA Xist é o único imprint necessário para levar modificações na cromatina que levam a inativação preferencial do Xp.