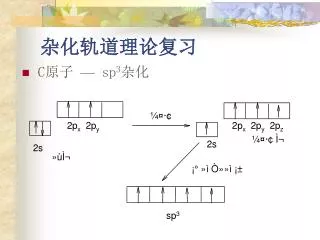
杂化轨道理论复习
杂化轨道理论复习. C 原子 — sp 3 杂化. sp 3 杂化轨道的形状与分布. ★ 键特征: ( 1 )成键电子云呈圆柱型对称 ; ( 2 )可以任意旋转而不被破坏 ; ( 3 )形成方式举例:. p x. s. p x. p x. sp 2 杂化. ★. 激发态. 3. sp 2 杂化轨道形状及其空间分布. ∏ 键的形成. ★. p y. p y. ∏ 键特征. p 轨道侧面重叠才能形成∏键 ; ∏ 键不能单独存在 ; ∏ 键不能旋转,否则断裂 ∏键电子云对称分布于单键平面的上、下方。 ∏键不牢固 .

杂化轨道理论复习
E N D
Presentation Transcript
杂化轨道理论复习 • C原子 — sp3杂化
★ 键特征: (1)成键电子云呈圆柱型对称; (2)可以任意旋转而不被破坏; (3)形成方式举例: px s px px
sp2杂化 ★ 激发态 3
∏键的形成 ★ py py
∏键特征 • p轨道侧面重叠才能形成∏键; • ∏键不能单独存在; • ∏键不能旋转,否则断裂 • ∏键电子云对称分布于单键平面的上、下方。 • ∏键不牢固.
C原子 — sp杂化 • 形成过程
乙炔两个∏键的形成 pz pz ◆
小 结 • 杂化轨道有三种:sp3、sp2、sp • 杂化轨道的形状是:一头大,一头小 • sp3轨道由1个s,3个p轨道形成,共4个杂化轨道。它们在空间呈正四面体型。 • sp2轨道由1个s,2个p轨道形成,共3个杂化轨道。它们在空间呈平面三角型。
sp杂化轨道由1个s、1个p轨道形成,共2个杂化轨道。在空间呈直线型。sp杂化轨道由1个s、1个p轨道形成,共2个杂化轨道。在空间呈直线型。 • 键可由sp3-s、sp2-s、sp-s及sp3-sp3,sp3-sp2,sp3-sp,sp2-sp2,sp2-sp,sp-sp以“头碰头”方式形成。 • ∏键只能由py-py、pz-pz之间以侧面重叠方式形成。 • ∏键不能单独存在.
第一节 烷烃 (alkane) 一、结构特点 1、C原子sp3杂化;2、通式:CnH2n+2 二、同分异构现象 1、构造异构; 2、构象异构 三、命名方法
★ 乙烷的链状结构(C — sp3) ◆ 一系列公用一个顶点的四面体
熔点 ★ 同分异构现象 (isomerism)-构造异构 -1300C -170C -1600C
如:乙烷的2种典型构象: (1).交叉式构象(staggered conformer) ◆ 构象异构体(conformational isomer) 投影式 锯架式
(2)重叠式构象(eclipsed conformer) Newman投影式 (Newman projection formula) 锯架式 (sawhorse formula)
* 乙烷分子的能量曲线 内 能 12.5 00 600 1200 3600 2400 旋转角度
普通命名法 (common nomenclature) 1.直链烷烃的命名:直链烷烃(10C以内 )按碳原子数叫“正某烷”(n-)。 2.含侧链烷烃的命名:若在链的一端含有 且无其它侧链的烷烃,则按碳原 子总数叫做异某烷(iso- 或i)。
3、若具有基团 且无其它侧链的含五或六个碳原子的烷烃,分别命名为新戊烷及新己烷 (neo-)。
系统命名法 (systematic nomenclature) 1、常见烷基(alkyl group, R-) (n-) (iso-) (tert-)
正丁基(n-) 仲丁基(sec-) 异丁基( iso-) 次甲基 CH2 CH 亚甲基
2、系统命名法: (1) 选主链 ● (2) 给主链编号 ● (3)取代基按次序规则排列 (4)相同取代基合并,其位置分别标出 (5)选取代基最多者为主链 (6)取代基位次和应最小
例 ** 优先基团后列出
四、化学性质 1.卤代反应(halogenation reaction)
** Reaction mechanism —— free radical chain reaction (1). Chain-initiating step (2).Chain-propagating step (3) Chain-terminating step
常见烷烃类物质 1、汽油:7C—8C 2、石油醚: (1)b.p. 30~600C (5C—6C) (2) b.p. 60~1200C (7C—8C) 3、液体石蜡:18C~24C 4、(固体)石蜡:25C~34C 5、凡士林:液体石蜡与石蜡混合物
第二节 烯烃(alkene) 一、结构 二、同分异构现象 三、命名 ★ CH2=CH- 乙烯基 CH3-CH=CH- 丙烯基(1-丙烯基) -CH2-CH=CH2烯丙基(2-丙烯基)
双键键能:610kj/mol 双键键长:134pm 单键键能:347kj/mol 单键键长:154pm
* 顺反异构现象 ★ 2-丁烯 b.p. 3.5°C b.p. 0.9°C
Ingold顺序规则基本要点 (1)基团排序:原子序数大者较优(如I>Br) (2)基团原子逐级比较; (3)有双键或叁键者视为2或3个相同原子。 (4)定构型:两个较优基团同侧 — Z构型 两个较优基团异侧 — E构型
对C2= # #
化学性质 一、加成反应(addition reaction)
1、催化加氢 2、加卤素(Cl2、Br2) 3、加HX(HCl、HBr、HI) * 马氏规则:不对称烯烃和HX加成时,氢原子主要加在含氢较多的双键碳原子上( Markovnikov’s rule ).
* 过氧化物效应:当存在R-O-O-R时, 不对称烯烃与HBr的加成主产物 是反马氏加成方向的。
☆ CCl4 (无色) (红棕色)