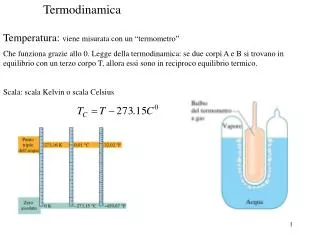
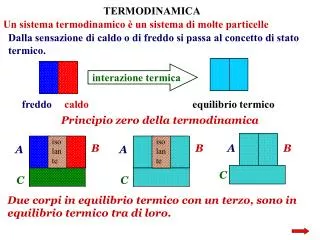
TERMODINAMICA
340 likes | 612 Views
TERMODINAMICA. TERMODINAMICA . La termodinámica puede definirse como el tema de la Física que estudia los procesos en los que se transfiere energía como calor y como trabajo. CALOR.

TERMODINAMICA
E N D
Presentation Transcript
TERMODINAMICA Luz H. Lasso
TERMODINAMICA La termodinámica puede definirse como el tema de la Física que estudia los procesos en los que se transfiere energía como calor y como trabajo. Luz H. Lasso
CALOR • El calor es la transferencia de energía entre diferentes cuerpos o diferentes zonas de un mismo cuerpo que se encuentran a distintas temperaturas. Este flujo siempre ocurre desde el cuerpo de mayor temperatura hacia el cuerpo de menor temperatura, ocurriendo la transferencia de calor hasta que ambos cuerpos se encuentren en equilibrio térmico. Luz H. Lasso
TEMPERATURA • La temperatura es una magnitud referida a las nociones comunes de caliente o fría. Por lo general, un objeto más "caliente" que otro puede considerarse que tiene una temperatura mayor, y si es frío, se considera que tiene una temperatura menor. En física, se define como una magnitud escalar relacionada con la energía interna de un sistema termodinámico, definida por el principio cero de la termodinámica. Luz H. Lasso
Más específicamente, está relacionada directamente con la parte de la energía interna conocida como "energía sensible", que es la energía asociada a los movimientos de las partículas del sistema, sea en un sentido traslacional, rotacional, o en forma de vibraciones. A medida de que sea mayor la energía sensible de un sistema, se observa que éste se encuentra más "caliente"; es decir, que su temperatura es mayor. Luz H. Lasso
CALOR TRANSFERIDO CON VARIACIÓN DE TEMPERATURA • Calor absorbido por un cuerpo. Q = c·m·Δt = c·m·(t-t0) • Si Q es positivo indica que el calor es absorbido, en cambio se Q es negativo indica que el calor es cedido. • Una caloria (cal) es la cantidad de calor que debe recibir un gramo de agua para que su temperatura aumente un grado celsius. Luz H. Lasso
ESCALA DE TEMPERATURAS Luz H. Lasso
PROPAGACION DEL CALOR • es la forma de la energía que se puede transferir de un sistema a otro como resultado de la diferencia de temperatura. • Se propagan por: • Conducción • Convección • Radiación Luz H. Lasso
La conducción de calor • Flujo de calor a través de medios sólidos por la vibración interna de las moléculas y de los electrones libres y por choques entre ellas. Las moléculas y los electrones libres de la fracción de un sistema con temperatura alta vibran con más intensidad que las moléculas de otras regiones del mismo sistema o de otros sistemas en contacto con temperaturas más bajas. Las moléculas con una velocidad más alta chocan con las moléculas menos excitadas y transfieren parte de su energía a las moléculas con menos energía en las regiones más frías del sistema. Las moléculas que absorben el excedente de energía también adquirirán una mayor velocidad vibratoria y generarán más calor (energía potencial -absorbe calor- <--> energía cinética -emite calor). Luz H. Lasso
Por ejemplo, la conducción de calor a través de la carrocería de un coche. Los metales son los mejores conductores térmicos; mientras que los materiales no metálicos son conductores térmicos imperfectos Luz H. Lasso
convección • La convección es una de las tres formas de transferencia de calor y se caracteriza porque se produce por intermedio de un fluido (aire, agua) que transporta el calor entre zonas con diferentes temperaturas. La convección se produce únicamente por medio de materiales fluidos. Estos, al calentarse, aumentan de volumen y, por lo tanto, su densidad disminuye y ascienden desplazando el fluido que se encuentra en la parte superior y que está a menor temperatura Luz H. Lasso
Lo que se llama convección en sí, es el transporte de calor por medio de las corrientes ascendente y descendente del fluido. Luz H. Lasso
radiación • ¿Qué es calor radiante? Con el sistema de calor radiante de ondas largas el aparato emite ondas infrarrojas en todas las direcciones. Estas, independientes de corrientes de aire, calientan todos los objetos. Por tanto, se calientan los muebles, las paredes y también las personas en la habitación. Todos estos materiales devuelven el calor al espacio y al aire, lo que nos da un bienestar agradable. Luz H. Lasso
El fenómeno de la radiación consiste en la propagación de energía en forma de ondas electromagnéticas o partículas subatómicas a través del vacío o de un medio material Luz H. Lasso
Dilatación térmica. • La experiencia muestra que los sólidos se dilatan cuando se calientan y se contraen cuando se enfrían. La dilatación y la contracción ocurren en tres (3) dimensiones: largo, ancho y alto. • La dilatación de los sólidos con el aumento de la temperatura ocurre porque aumenta la energía térmica y esto hace que aumente las vibraciones de los átomos y moléculas que forman el cuerpo, haciendo que pase a posiciones de equilibrio más alejadas que las originales. Este alejamiento mayor de los átomos y de las moléculas del sólido produce su dilatación en todas las direcciones. Luz H. Lasso
A la variación en las dimensiones de un sólido causada por calentamiento (se dilata) o enfriamiento (se contrae) se denomina Dilatación térmica La dilatación lineal es aquella en la cual predomina la variación en una única dimensión. largo o altura del cuerpo. Si calentamos esa barra hasta que la misma sufra una variación de temperatura notaremos que su longitud pasa a ser igual a L (conforme podemos ver en la siguiente figura): Luz H. Lasso
Donde:L0 = longitud inicial.L = longitud final.ΔL = dilatación (DL > 0) ó contracción (DL < 0)Δθ= θ0 – θ (variación de la temperatura) α = es una constante de proporcionalidad característica del material que constituye la barra, denominada como coeficiente de dilatación térmica lineal. Luz H. Lasso
Dilatación superficial • Es aquella en que predomina la variación en dos dimensiones, o sea, la variación del área del cuerpo • Para estudiar este tipo de dilatación, podemos imaginar una placa metálica de área inicial S0 y temperatura inicial θ0. Si la calentáramos hasta la temperatura final θ, su área pasará a tener un valor final igual a S. Luz H. Lasso
Dilatación cúbica • Es aquella en que predomina la variación en tres dimensiones, o sea, la variación del volumen del cuerpo.Para estudiar este tipo de dilatación, podemos imaginar un cubo metálico de volumen inicial V0 y la temperatura inicial θ0. Si lo calentamos hasta la temperatura final, su volumen pasará a tener un valor final igual a V. Luz H. Lasso
CALORIMETRÍA • Experimentalmente se conoce que la energía calorífica absorbida o cedida por un cuerpo es proporcional a su masa(m) a la variación de temperatura que experimenta el cuerpo (T) y también a la naturaleza del cuerpo. • Todo esto se relacionaría con la siguiente expresión: Q=m c T • Que seria la cantidad de calor ganada o cedida por el cuerpo. En la formula c es el calor especifico del cuerpo es decir la cantidad de calor necesaria para incrementar 1ºC la temperatura de 1 g de dicha sustancia. • La unidad de calor es la caloría (cal) o también cal-gr que es la cantidad de calor necesaria para elevar en 1ºC la temperatura de 1 g de H2O, también se utiliza la Kcal que es la cantidad de calor necesaria para elevar en 1ºC la temperatura de 1 Kg de H2O. • 1 caloría= 4.18 J Luz H. Lasso
Ecuación fundamental de la calorimetría Q=m c ∆T Q... cantidad de calor m... masa del cuerpo c... calor específico del cuerpo Δt... variación de temperatura Observación: Para que el cuerpo aumente de temperatura; tiene que recibir calor, para eso la temperatura tf debe ser mayor que la temperatura to ; y recibe el nombre de calor recibido. tf> to® calor recibido (Q > 0) Para disminuir la temperatura; tiene que ceder calor, para eso la temperatura tf debe ser menor que la temperatura to ; y recibe el nombre de calor cedido. tf< to® calor cedido (Q < 0) Luz H. Lasso
Principio de conservación de energía • er Principio: Cuando 2 o más cuerpos con temperaturas diferentes son puestos en contacto, ellos intercambian calor entre sí hasta alcanzar el equilibrio térmico. • Luego, considerando un sistema térmicamente aislado, "La cantidad de calor recibida por unos es igual a la cantidad de calor cedida por los otros". • 2do Principio: "La cantidad de calor recibida por un sistema durante una transformación es igual a la cantidad de calor cedida por él en la transformación inversa". • Q absorbido = Q cedido Luz H. Lasso
Normalmente, una sustancia experimenta un cambio de temperatura cuando absorbe o cede calor al ambiente que le rodea. Sin embargo, cuando una sustancia cambia de fase absorbe o cede calor sin que se produzca un cambio de su temperatura. El calor Q que es necesario aportar para que una masa m de cierta sustancia cambie de fase es igual a Q=mL donde L se denomina calor latente de la sustancia y depende del tipo de cambio de fase. Por ejemplo, para que el agua cambie de sólido (hielo) a líquido, a 0ºC se necesitan 334·103 J/kg. Para que cambie de líquido a vapor a 100 ºC se precisan 2260·103 J/kg. Luz H. Lasso
En la siguiente tabla, se proporcionan los datos referentes a los cambios de estado de algunas sustancias. Luz H. Lasso
Cambios de estado del agua En la figura, que no se ha hecho a escala, se muestra cómo se va incrementando la temperatura a medida que se aporta calor al sistema. La vaporización del agua requiere de gran cantidad de calor como podemos observar en la gráfica Luz H. Lasso
http://es.wikipedia.org • http://jfinternational.com/mf/termodinamica.html • http://adrigarxia.blogspot.com/2011/06/trnsferencia-de-calory-sus-tipos.html • http://www.calor-radiante.com/1.php • http://www.fisicanet.com.ar/fisica/termoestatica/ap05_dilatacion.php • http://fisica.laguia2000.com/fisica-del-estado-solido/dilatacion-lineal-superficial-y-volumetrica • http://html.rincondelvago.com/calorimetria_1.html • http://www.youtube.com/watch?v=ZQl890ugKcQ • http://www.youtube.com/watch?v=6-udN4cZ6HU&feature=relat • ed Luz H. Lasso