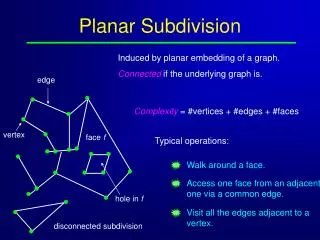
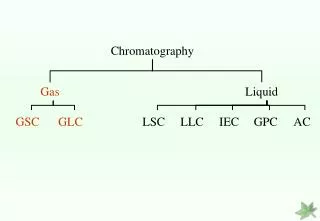
Planar Chromatography
Planar Chromatography. อ.พุทธรักษา วรานุศุภากุล ภาควิชาเคมี คณะวิทยาศาสตร์ จุฬาลงกรณ์มหาวิทยาลัย. Planar Chromatography. เป็นเทคนิคทางโครมาโทกราฟีที่มีรูปแบบของการบรรจุหรือวางตัวของเฟสคงที่แบบแผ่นเรียบ (Planar Chromatography) เฟสคงที่และเฟสเคลื่อนที่ใน Planar Chromatography

Planar Chromatography
E N D
Presentation Transcript
Planar Chromatography อ.พุทธรักษา วรานุศุภากุล ภาควิชาเคมี คณะวิทยาศาสตร์ จุฬาลงกรณ์มหาวิทยาลัย
Planar Chromatography • เป็นเทคนิคทางโครมาโทกราฟีที่มีรูปแบบของการบรรจุหรือวางตัวของเฟสคงที่แบบแผ่นเรียบ (Planar Chromatography) • เฟสคงที่และเฟสเคลื่อนที่ใน Planar Chromatography • เฟสคงที่: ติดอยู่บนแผ่นเรียบหรือในรูพรุนของกระดาษ • เฟสเคลื่อนที่: เคลื่อนผ่านเฟสคงที่ด้วยแรงแคพิลลารี (capillary action) หรือแรงโน้มถ่วง (gravity) • เทคนิคทาง Planar Chromatography • Paper Chromatography (PC) – ง่ายที่สุดในโครมาโทกราฟี • Thin-Layer Chromatography (TLC) เฟสคงที่ flat plate
Why Planar Chromatography? • เป็นเทคนิคที่ง่าย • เครื่องมือและอุปกรณ์ที่ใช้ไม่ซับซ้อน • ค่าใช้จ่ายในการวิเคราะห์ไม่สูง • เวลาที่ใช้ในการแยกไม่นานมาก • มีความไวในการวิเคราะห์ (sensitivity) พอสมควร • สามารถทำวิเคราะห์สารตัวอย่างได้หลายๆ ตัวในเวลาเดียวกัน
เทคนิคของ Planar Chromatography • Paper Chromatography (PC) • ใช้กระดาษกรองซึ่งเป็นพวกเซลลูโลสเป็นเฟสคงที่ • ขนาดรูพรุนของกระดาษกรองเป็นตัวกำหนดการเคลื่อนที่ของตัวทำละลาย (เฟสเคลื่อนที่) • กระดาษที่มีรูพรุนน้อยหรือละเอียดมากจะทำให้การเคลื่อนที่ของตัวทำละลายช้า และเกิดการแยกที่ดี • กระดาษที่หนาจะทำให้มีความจุของสารตัวอย่างเพิ่มขึ้น – เหมาะกับงานด้าน preparative separation • Thin Layer Chromatography (TLC) • ทำการยึดเฟสคงที่บนแผ่นเรียบ เช่น แผ่นกระจก อะลูมิเนียม หรือพลาสติก • องค์ประกอบของแผ่น TLC • Support – แผ่นเรียบที่ใช้ยึดเฟสคงที่ • เฟสคงที่ (Sorbent) • ตัวยึด (Binder) – เพิ่มความแข็งแรงของการยึดติดเฟสคงที่กับแผ่นเรียบ (มีหรือไม่มีก็ได้) • Fluorescent indicator (มีหรือไม่มีก็ได้)
การแยกโดย Planar Chromatography • อาศัยความแตกต่างในการเคลื่อนที่ของสารผ่านเฟสคงที่บนแผ่นเรียบหรือรูพรุนของแผ่นกระดาษ • กลไกของการแยกใน Planar Chromatography • การดูดซับ (Adsorption): กลไกที่ใช้มากที่สุด • การแพร่ (Partition) • การแลกเปลี่ยนไอออน (Ion-exchange) • อัตราการเคลื่อนที่ของสารบอกด้วยค่า retardation factor (Rf)
Retardation Factor, Rf Solvent front Mid-point of substance zone จุดเริ่มต้น • บอกอัตราการเคลื่อนที่ของสารบนแผ่นเรียบ ซึ่งเท่ากับอัตราการเคลื่อนที่สัมพัทธ์ของสาร • ค่า Rf คำนวณจากอัตราส่วนของระยะทางที่สารเคลื่อนที่กับระยะทางที่เฟสเคลื่อนที่เคลื่อนไป ดังนั้น ค่า Rfจะมีค่าน้อยกว่าหรือเท่ากับ 1 เท่านั้น
ธรรมชาติของตัวดูดซับ (sorbents) ธรรมชาติทางเคมี ขนาดของอนุภาคและพื้นที่ผิว ตัวยึด (binder) ธรรมชาติของเฟสเคลื่อนที่ ความบริสุทธิ์ ความถูกต้องของส่วนผสม ความชื้น (humidity) การระเหย การยึดตัวดูดซับกับแผ่นเรียบ Activity ของตัวดูดซับ ความหนาของตัวดูดซับ ความสม่ำเสมอของการยึด อุณหภูมิ ปริมาณของสารตัวอย่างที่ใช้ สมดุลของความดันไอของเฟสเคลื่อนที่บนแผ่นเรียบกับบรรยากาศในถัง (chamber) ปัจจัยที่ส่งผลต่อค่า Rf
Thin Layer Chromatography (TLC) องค์ประกอบของแผ่น TLC • Support: แผ่นเรียบที่ใช้ยึดเฟสคงที่ • ควรมีความแข็งแรง ไม่ว่องไวและทนต่อตัวทำละลายที่ใช้เป็นเฟสเคลื่อนที่ และมีความสม่ำเสมอของพื้นผิว • วัสดุที่ใช้ เช่น แผ่นกระจก อะลูมิเนียม หรือพลาสติก • ตัวดูดซับ (Sorbent): เฟสคงที่ที่ใช้ • สิ่งที่ต้องคำนึงถึงคือ ชนิดของสารที่ต้องการแยก เทคนิคในการตรวจวัด ความหนาและความเสถียรของชั้นที่เคลือบ และชนิดของเฟสเคลื่อนที่ • ตัวยึด (Binder) – เพิ่มความแข็งแรงของการยึดติดเฟสคงที่กับแผ่นเรียบ (มีหรือไม่มีก็ได้) • Fluorescent indicator - ช่วยการตรวจหาสารหลังการแยก (มีหรือไม่มีก็ได้)
ตัวดูดซับ (Sorbents) ชนิด Polar Inorganic • ลำดับการเคลื่อนที่ของสาร (elution) จะขึ้นอยู่กับ polarity/polarizability ของหมู่ functional groups ของสารเป็นหลัก • สามารถเลือกใช้ตัวเฟสเคลื่อนที่ได้หลายชนิดเพราะมีความเสถียรสูง • ข้อเสีย: • มี selectivity ที่ต่ำในการแยกสารบางกลุ่ม เช่น การแยกสารที่ใน homologues series • สารตัวอย่างที่มีความมีขั้วสูงอาจยึดกับตัวดูดซับได้แข็งแรงเกินไป ทำให้ยากต่อการชะสาร (ทำให้สารเคลื่อนที่) ชนิด Non-polar Bonded Phases • A reversed-phase system • ข้อดี: • เป็นการ screening เพื่อเป็นแนวทางสำหรับการแยกโดยคอลัมน์โครมาโทกราฟีได้ • เมื่อเปลี่ยนองค์ประกอบหรือสัดส่วนของเฟสเคลื่อนที่ มีผลต่อค่าการแยก (Rf) และรูปร่างของจุดสารที่ได้จากการแยกมาก • มีความถูกต้องของการทำซ้ำ (reproducibility) ที่ดี
ตัวดูดซับ (Sorbent) ที่ใช้ใน TLC Mostly use Limited use Reverse phase mode
ตัวยึด (Binders) และ Florescent Indicators • ไม่จำเป็นต้องมี • ตัวยึดที่นิยมใช้ เช่น Calcium sulfate (gypsum), Silicon dioxide, แป้ง หรือ polyesters • ข้อดีของการมีตัวยึด: ช่วยเพิ่มความแข็งแรง ความคงทน และการแตกร้าวของชั้นเคลือบของเฟสคงที่ • ข้อเสียของการมีตัวยึด: ส่งผลต่อพฤติกรรมการดูดซับสารของเฟสคงที่ และลักษณะการแยกสารเมื่อใช้ support ที่แตกต่างกัน • Florescent Indicators ช่วยให้มองเห็นสารที่ไม่มีสีในแผ่นเรียบหลังการแยก (visualization) โดยอินดิเคเตอร์ที่นิยมใช้มี 2 แบบ Short-wave UV light (254 nm) และ Long-wave UV light (366 nm)
Florescent Indicators • Long-wave UV light (366 nm): สารจะเห็นเป็นจุดสีสว่างซึ่งเกิดได้หลายสี บนพื้นที่มืดของแผ่น TLC เมื่อทำการส่องด้วยแสงยูวี • Short-wave UV light (254 nm): สารจะเห็นเป็นจุดสีดำบนพื้น fluorescence สีเขียวสว่างของแผ่น TLC เมื่อทำการส่องด้วยแสงยูวี
เฟสเคลื่อนที่ใน Planar Chromatography • ตัวทำละลายที่ดีในการทำ Planar Chromatography • มีความบริสุทธิ์สูง ไม่ทำปฏิกิริยากับสารและชั้นของเฟสคงที่ มีจุดเดือดต่ำ (เพื่อสะดวกขั้นตอนการทำให้แห้ง) มีความสามารถในการรวมกันได้ (miscibility) ในกรณีที่ใช้ตัวทำละลายผสม ไม่ไวไฟและไม่เป็นพิษ • เฟสเคลื่อนที่ในระบบ Normal phase (Non-polar MP with a polar SP) • ใช้ตัวทำละลายที่ไม่มีขั้วซึ่งอาจเติม polar modifier เพื่อช่วยควบคุมความแรงของการชะและ selectivity ของการแยก • การเพิ่ม polarity ของตัวทำละลาย จะทำให้ความแรงในการชะของเฟสเคลื่อนที่สูงขึ้น ส่งผลให้ค่า Rfมากขึ้น • เฟสเคลื่อนที่ในระบบ Reversed phase (Polar MP with a non-polar SP) • นิยมใช้สารละลายผสมของน้ำกับ organic modifier เช่น methanol, acetonitrile, tetrahydrofuran • ความสามารถในการชะเพิ่มขึ้นเมื่อเพิ่มความเข้มข้นของ organic modifier หรือลด polarity ของ organic modifier
หลักการหาเฟสเคลื่อนที่ (Solvent Optimization) • จากข้อมูลที่มีการตีพิมพ์ • การลองผิดลองถูก (trial-and-error) • โดยใช้ประสบการณ์ที่เคยทำมา • ใช้ข้อมูลความแรงของตัวทำละลาย • จากการทำ Model หรือการคาดคะเนทางทฤษฏี
การเตรียมแผ่น • ใน PC: ใช้กระดาษกรองซึ่งเป็นพวกเซลลูโลส • กระดาษกรองที่ใช้จะต้องเก็บในที่ที่มีการควบคุมความชื้น เนื่องจากปริมาณน้ำในเซลลูโลสจะเป็นตัวกำหนดลักษณะการแยกของกระดาษกรอง • ใน TLC: เคลือบของแข็งของเฟสคงที่กับแผ่นเรียบ เช่น กระจก อะลูมิเนียมหรือแผ่นพลาสติก • การเคลือบของแข็งของเฟสคงที่กับแผ่นจะต้องเรียบ (smooth) และสม่ำเสมอ (uniform layer) • การเคลือบทำโดยนำเฟสคงที่ใส่น้ำหรือตัวทำละลายให้เป็น slurry แล้วนำไปเคลือบบนแผ่น หลังจากนั้นทำให้แห้งในอากาศ แล้วนำไปอบให้แห้งอีกครั้ง • การเคลือบแผ่นเรียบทำได้หลายวิธี โดยที่นิยมทำมากที่สุด คือ การแผ่กระจาย (Spreading) ซึ่งมีวิธีการที่ง่าย ไม่ยุ่งยาก
Spreading Technique • ความถูกต้องของการทำซ้ำ (reproducibility) ดีและสามารถปรับความหนาของชั้นที่เคลือบได้ง่าย • ขั้นตอนในการเคลือบ • เช็ดแผ่นที่เป็นตัว support ให้สะอาด • ทำการกระจายชั้นของเฟสคงที่โดยใช้แท่งแก้วค่อยปาดเกลี่ยหรือใช้เครื่องสำหรับการทำให้กระจายตัว (spreading apparatus) • ทำแผ่นที่เคลือบให้แห้งโดยตั้งให้แห้งที่อุณหภูมิห้อง แล้วทำการอบให้แห้งอีกครั้งประมาณ 15-18 ชั่วโมง Plate coater
ตัวอย่างคำนำหน้าที่ใช้บอกชนิดของเฟสคงที่ในแผ่นแบบ Precoated J.C. Touchstone, Practice of Thin Layer Chromatography, 3rd ed., John Wiley & Sons, 1992.
Sample Application • การใส่สารบนแผ่นควรทำให้มีขนาดเล็กๆ • การใส่สารสามารถทำเป็นจุด (spot) หรือ เป็นแถบ (streak) ก็ได้ • สามารถเพิ่มปริมาณของสารที่บรรจุ โดยยังทำให้จุดหรือแถบมีขนาดเล็ก ได้โดยการทำซ้ำหลายๆ ครั้ง โดยแต่ละครั้งต้องทำให้ตัวทำละลายระเหยออกหมดก่อน • การเลือกวิธี sample application ขึ้นอยู่กับ • ปริมาตรของสารตังอย่าง • จำนวนตัวอย่างที่ต้องการทำต่อครั้ง • ความเที่ยงและการทำอัตโนมัติ
อุปกรณ์การบรรจุสาร • ทำด้วยตนเอง • Capillary tube • Micropipette • Syringe • เครื่องอัตโนมัติ • Auto spotter/Auto streaker
การแยกโดย Linear Development • การแยกเกิดขึ้นภายในภาชนะที่มีฝาปิดมิดชิด โดยแผ่นเรียบหรือกระดาษจะถูกวางไว้ในแนวเดียวกับการไหลของเฟสเคลื่อนที่ • การเคลื่อนที่ของเฟสเคลื่อนที่มี 2 แบบ คือ • เคลื่อนที่ขึ้นตามแนวของแผ่นเรียบหรือกระดาษ (ascenting) • เคลื่อนที่ลงตามแนวของแผ่นเรียบหรือกระดาษ (decending) Ascenting development
โครมาโทแกรมที่ได้จากการแยกโดย Linear Development
การแยกโดย Multiple Development • ทำการ develop ซ้ำหลายๆ รอบ • เป็นการเพิ่มประสิทธิภาพของการแยก แต่จะเสียเวลาเพิ่มมากขึ้น • การทำ multiple development สามารถทำได้โดย • ทำซ้ำโดยใช้ระบบเฟสเคลื่อนที่เหมือนเดิมในทิศทางเดิม: ทำให้การแยกสารที่มีค่า Rfใกล้ๆ กัน แยกได้ดีขึ้น • ทำซ้ำโดยใช้ระบบเฟสเคลื่อนที่ใหม่ในทิศทางการแยกเดิม: ช่วยในการแยกสารที่มีความแตกต่างของ polarity มากๆ • การ development แบบ 2 มิติ: ทำการ developed ครั้งที่ 2 โดยเฟสเคลื่อนที่ที่แตกต่างกัน ในทิศทางที่ตั้งฉากกับทิศทางเดิม
การตรวจวัด (Detection) • วิธีการตรวจวัดทางกายภาพ • การตรวจวัดโดยตรง: สำหรับสารที่มีสี • ภายใต้แสงยูวี • Fluorescent analyte • Plate with indicator • วิธีการตรวจวัดทางเคมี • ให้สารทำปฏิกิริยาทางเคมีเพื่อให้เกิดสารที่มีสีหรือ fluorescent spots โดยการพ่น (spraying) หรือ จุ่ม (dipping) กับรีเอเจนต์ • ชนิดของ reagents ที่ใช้ • สารก่อให้เกิดอนุพันธ์ (Derivatization) • Reversible color reaction เช่นไอของไอโอดีน, water spray, pH อินดิเคเตอร์ • การทำให้สารอินทรีย์เกิดเป็นสีดำ (Charring) ด้วยกรดซัลฟูริกเข้มข้น • Reagents เฉพาะ
อุปกรณ์สำหรับการทำ TLC ถังสำหรับดำเนินการแยก (Developing) กล่องส่อง UV แผ่นช่วยการอิ่มตัว ชุดพ่นสารตรวจวัด (Reagent Sprayer) แผ่น TLC ชุดอุปกรณ์การใส่สารบนแผ่นเรียบ
การวิเคราะห์ด้วย Planar Chromatography การทำคุณภาพวิเคราะห์ • เทียบค่า Rf ของสารตัวอย่างกับสารมาตรฐานโดยใช้ภาวะในการแยกที่มีเหมือนกัน • นิยมทำสารมาตรฐานควบคู่ไปกับสารตัวอย่างบนแผ่นเดียวกันเลย การทำปริมาณวิเคราะห์ • หาปริมาณสารโดยการวัดโดยตรงจากจุดที่แยกได้บนแผ่น หรือนำสารออกมาแล้วค่อยทำการวัดด้วยวิธีการอื่นๆ ก็ได้ • การทำปริมาณวิเคราะห์โดยตรงจากแผ่น (In situ) • เปรียบเทียบพื้นที่ของจุด (visual evaluation) ระหว่างสารตัวอย่างกับสารมาตรฐานที่ทราบปริมาณแน่นอนแล้ว • เปรียบเทียบค่าความเข้มของแสง (optical scanners) ระหว่างสารตัวอย่างกับสารมาตรฐานที่ทราบปริมาณแน่นอนแล้ว จากการสะท้อนแสงหรือฟลูออเรสเซนต์หรือการดูดกลืนแสง ด้วยเครื่อง scanning densitometer • การทำปริมาณวิเคราะห์โดยเอาสารออกจากแผ่น (Elution technique) • ขูดจุดของสารที่แยกออกมาจากแผ่น (จะมี sorbent ติดออกมาด้วย) แล้วทำการสกัดออกมาเพื่อทำการวิเคราะหืต่อไป
Quantitative Analysis • Elution technique • Scarping of the spots and eluting the substance from the sorbent • In situ visual evaluation • Comparing the spot sizes between sample and standards • In situ optical scanners • Scanning densitometers • Imaging scanners