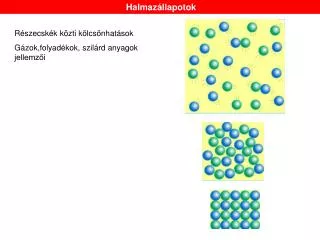
Halmazállapotok
Halmazállapotok. Készítette Varga István VEGYÉSZETI-ÉLELMISZERIPARI KÖZÉPISKOLA CSÓKA. A molekulákban levő atomokat, valamint az anyagot alkotó molekulákat különböző nagyságú vonzóerők kapcsolják egymáshoz . A VONZÓERŐ kohéziós erő nagyságától függően, az anyag lehet: Gáznemű,

Halmazállapotok
E N D
Presentation Transcript
Halmazállapotok Készítette Varga István VEGYÉSZETI-ÉLELMISZERIPARI KÖZÉPISKOLA CSÓKA
A molekulákban levő atomokat, valamint az anyagot alkotó molekulákat különböző nagyságú vonzóerők kapcsolják egymáshoz. • A VONZÓERŐ kohéziós erő nagyságától függően, az anyag lehet: • Gáznemű, • Cseppfolyós és • Szilárd halmazállapotú.
A gázokban a molekulák távol vannak egymástól, és ezért kicsiny közöttük a kohézió. A gázoknál (alacsony nyomáson) nemis vesszük a kohéziót tekintetbe. • A gázok legszembetűnőbb tulajdonsága, hogy igyekeznek a rendelkezésükre álló teret teljesen és egyenletesen kitölteni.
Agázmolekulák nagy sebességgel mozognaka tér minden irányában. • Meddig haladhat egyenes vonalban a molekula? • Nyilván addig, amíg egy másik molekulába, vagy esetleg az edény falába nem ütközik. Az ütközés rugalmas, hasonló a biliárdgolyók ütközéséhez. • Milyen sebességgel halad a molekula? Ez két tényezőtől függ: • a molekula tömegétől és • a hőmérséklettől.
Egy példa: • Az argon egy atomja 0°C-on 400 métert tesz meg másodpercenként, 100°C-on 470 métert, 200°C-on pedig már 530 m/s a sebessége. • Látjuk, hogy a részecske sebessége a hőmérséklettel arányosan növekszik. • A tömeg fordítva hat: ugyanazon a hőmérsékleten a kétszeres tömegű molekula csak fél sebességgel repül.
Mi történik, ha egy gáz molekulái beleütköznek az edény falába? • A molekulák-tömegük és sebességük szorzatának megfelelő- impulzust adnak át a falnak. A sok molekula összegeződő űtődése nyomás alakjában jelentkezik. • Mitől függ a nyomás nagysága? • Megint csak két tényezőtől: a molekulák mennyiségétől és impulzusától.
Ideális (tökéletes) gázok Olyan gázok, amelyek részecskéi egymással nincsenek kölcsönhatásban és nincs saját térfogatuk. • A kis sűrűségű és nem túl alacsony hőmérsékletű gázok kielégítő közelítéssel ideális gázoknak tekinthetők. • A hidrogén, az oxigén, a nitrogén és a hélium általános feltételek mellett legjobban megközelítik az ideális gázállapotot.
Egy adott mennyiségű gáz állapotát a termodinamikai állapotjelzők ismeretében tudjuk definiálni. • A termodinamikai állapotjelzők a: • nyomás, • hőmérséklet és a • térfogat.
Gáztörvények A tömeg, a hőmérséklet, a nyomás és a térfogat jellemzőek a gáz állapotára. Bármelyik mennyiség változása a gáz állapotának változását eredményezi. • A gázok állapotváltozásainak törvényeit könnyebben felismerhetjük, ha először külön-külön vizsgáljuk azokat a változásokat, amelyekben egy állapotjelző állandó marad.
Boyle-Mariotte-törvénye Ha T = const. Edme Mariotte (1620-1684) Robert Boyle (1627-1691) Adott tömegű gáz nyomásának és térfogatának a szorzata állandó.
A Boyle-Mariotte törvényt gyakran úgy használjuk, hogy egy adott gázmennyiség két különböző állapotát hasonlítjuk össze, ha mindkét állapotban a hőmérséklet ugyanakkora:
Gay-Lussac I. törvénye p = const. Ha Ha adott tömegű gáz hőmérsékletét 1°C-al megváltóztatjuk, akkor a gáz 0°C-on mért térfogata 1/273-ad résszel változik, függetlenül a gáz minőségétől. Joseph Louis Gay-Lussac (1778 – 1850) α - a gáz hőtágulási együtthatója
Gay-Lussac II. törvénye V = const. Ha Ha adott tömegű gáz hőmérsékletét 1°C-al megváltóztatjuk, akkor a gáz 0°C-on mért nyomása1/273-ad résszel változik, függetlenül a gáz minőségétől. Joseph Louis Gay-Lussac (1778 – 1850) β - a gáz hőmérsékleti tényezője
A gázok állandó nyomás és állandó térfogat melletti hőtágulása lineáris.
egyesített gáztörvény Boyle-Mariotte és Gay-Lussac I. törvényéből kiindulva kifejezhetjük az ideális gázok egyesített gáztörvényét: illetve 1 mól mennyiségű, T0= 273 K hőmérsékletű gáz, légköri nyomáson (p0=101325 Pa) V0=22,4·10-3 m3 térfogatú.
Behelyettesítjük az 1 mólnyi gáz adatait: Az állandót R-rel jelöljük, és egyetemes gázállandónak nevezzük.
Tetszőleges mennyiségű gázra, a törvény a következőképpen fejezhető ki: illetve
Dalton törvénye Az ideális gázok keveréke által kifejtett nyomás egyenlő azon nyomások összegével, amelyet az egyes gázalkotók akkor fejtenek ki, ha egyedül töltenék ki az adott térfogatot. John Dalton (1766-1844)
A folyadékállapot közbenső helyet foglal el a gáz- és szilárd halmazállapot között. Szemben a gázokkal, a folyadékrészecskék egymástól való távolsága olyan kicsi, hogy már érvényesülnek a vonzóerők, az ún. van der Waals-erők, amelyek részben elektrosztatikus jellegűek, de fellépnek elektromosan semleges molekulák között is. A folyadékok különböznek a szilárd anyagoktól is.
A folyadékban uralkodó kohéziós erők nagyságára több jelenségből következtethetünk. Ilyen jelenségek pl. : • a párolgáshő • a belső súrlódás és • a felületi feszültség. • A folyadékok igen nagy ellenállást tanúsítanak az összenyomás ellen. Gyakorlatilag a folyadékokat összenyomhatatlanoknak tekintjük.
A Gőznyomás • A nyitott edényben levő folyadék párolgása során a folyadékgőzök a környezetbe kerülnek. A párolgás mindaddig tart, míg az összes folyadék el nem párolog. • A zárt edényben levő folyadék párolgása során a folyadékgőzök koncentrációja egy bizonyos ideig növekszik, ezt követően nem változik. Néhány gőzmolekula a mozgása során a folyadékfelszínre kerül és visszajut a folyadékba. Ezáltal a párolgással egyidejűleg a lecsapódás(kondenzáció) is végbemegy.
Ha a párolgás sebessége kiegyenlítődik a lecsapódás sebességével, vagyis ha egységnyi idő alatt a folyadékból kirepülő gőzmolekulák száma megegyezik a folyadékba visszakerülő gőzmolekulák számával, akkor beáll a dinamikus egyensúly. A saját folyadékával egyensúlyban levő gőzt telített gőznek, a nyomását pedig a telített gőznyomásnak nevezzük. A telített gőz nyomása a folyadék anyagi minőségétől és a hőmérséklettől függ. A hőmérséklet növelésével a gőznyomás is növekszik.
A folyadék forrása azon a hőmérsékleten indul meg, amelyen telített gőzének nyomása kiegyenlítődik a folyadék felszínére ható külső nyomással. • A gőznyomás változását a hőmérséklet függvényében matematikailag a Clausius-Klapeyron egyenlet fejezi ki: ∆Hi – moláris párolgáshő
A párolgáshő Azt a hőmennyiséget, amelyet 1kg folyadékkal kell közölni, hogy ugyanolyan hőmérsékletű gőzzé alakuljon, párolgáshőnek nevezzük. A párolgáshőt r-rel jelöljük. Mértékegysége a J/ kgvagy kJ/kg. • A víz párolgáshője, forráshője 2256 kJ/kg. A párolgáshoz szükséges energia nagysága kismértékben függ a párolgó folyadék hőmérsékletétől és a környezet nyomásától is.
A telített gőz hűtésekor, a hőmérséklete változatlan marad, mert latens (rejtett) párolgási hő szabadul fel, a gőz pedig lecsapódik (kondenzálódik). Ebből kifolyólag a párolgási hő és a kondenzációshő egyenlőek, de ellentétes előjellel rendelkeznek. –párolgási hő =+ kondenzációs hő • A latin eredetű kifejezés – „latens hő” – rejtett hőt jelent, amelyet a tudósok a XVIII. század második felében vezettek be, amikor a jég olvadását és a víz forrását vizsgálták. Ha pl. –25oC-os jeget egyenletesen melegítünk, a hőmérséklet 0oC-ig emelkedik. 0oC-on a jég olvadni kezd, és hőmérséklete nem növekszik tovább, ameddig az egész jég el nem olvadt, a víz-jég keverék hőmérséklete mindvégig 0oC marad. Tehát olvadás közben a melegítés hatása nem mutatkozik meg a hőmérséklet-növekedésében, ilyen értelemben a közölt hő rejtve marad, ez a magyarázata a latens hő kifejezésnek.
A belső súrlódás (viszkozitás) Áramlásakor belső súrlódási erők keletkeznek, amelyek gátolják a fluidum mozgását. Ezek az erők, az egymáson elcsúszó szomszédos fluidumrétegek között jönnek létre. A fluidumrétegek az 1 álló, és 2mozgó felületek között helyezkednek el. A felső2-es felület c sebességgel mozog. Kísérletileg bizonyított, hogy a 2-es felülettel határos fluidumréteg is c sebességgel mozog, míg az 1-es felülettel határos, mozdulatlan marad.
A fluidumnak azt a tulajdonságát, hogy ellenállást tanúsít a részecskék egymás közti relatív elmozdulása során keletkezett erőhatásokkal szemben, viszkozitásnak nevezzük. • Megkülönböztetünk dinamikaiés kinematikaiviszkozitást. Ha valamely fluidumréteg egy másikhoz képest elmozdul, akkor az így fellépő súrlódási erő nem függ a nyomástól, egyenesen arányos az elmozdult rétegek viszonylagos sebességével és felületével, valamint fordítottan arányos a rétegek közötti távolsággal, továbbá függ a fluidum tulajdonságaitól (Newton törvénye).
A gyakorlatban a fluidum viszkozitását a kinematikai viszkozitási tényezővel (ν) fejezik ki, ami a dinamikus viszkozitás (μ) és a fluidum sűrűségének (ρ) hányadosa: A folyadékok viszkozitása a hőmérséklet növekedésével jelentősencsökken, a gázok viszkozitása növekszik.
A felületi feszültség • Ha folyadék érintkezik gázzal (vagy gőzzel) vagy másik nem elegyedő folyadékkal, az érintkezési felületek a felületi feszültség következtében, minimális értéket igyekeznek felvenni (gömb alakúak lesznek). • Ez azzal magyarázható, hogy a folyadék belsejében azonos molekulák közötti kölcsönhatások érvényesülnek, míg azokra a molekulákra, amelyek közvetlenül a fázisfelületnél helyezkednek el nagyobb vonzás érvényesül a belső folyadékréteg irányába, mint a környező anyag molekuláihoz.
Ennek eredményeképpen a folyadékfelszínen a felszínre merőleges irányú, a folyadék belseje felé mutató nyomás hat, amely ezt a felületet minimálisra igyekszik csökkenteni. Tehát, ha a felületet növelni akarjuk, akkor ehhez energiabefektetés szükséges. Az egységnyi új felület létrehozásához szükséges energiát fázisok közötti vagy felületi feszültségnek nevezzük és σ-val jelöljük.
A szilárd anyagoknak meghatározott térfogatuk és alakjuk van. Az anyagokban az alkotó részecskék közel vannak egymáshoz és erős a részecskék közötti vonzás. A részecskék nincsenek nyugalomban, hanem állandó rezgő mozgást végeznek. A rezgésamplitúdója a hőmérséklettől függ. • A hőmérséklet emelkedésével növekszik a rezgések amplitúdója. • A szilárd anyagok lehetnek: • kristályos felépítésűek és • amorfak.
Azokat az anyagokat, amelyekben a részecskék szabályosan helyezkednek el, kristályos anyagoknak nevezzük. • A szilárd anyagok egy kisebb részében a részecskék szabálytalanul helyezkednek el. Ezeket amorf anyagoknak nevezzük. • Amorf anyagok pl. az üveg, a gyantafélék, műanyagok, a vízben oldhatatlan proteinek stb. • Az amorf anyagoknak a szabálytalan térbeli elrendeződés miatt nincs meghatározott olvadáspontjuk, melegítéskor fokozatosan megpuhulnak.
Kristályos anyagok • A kristályok szabályos sík lapokkal határolt különböző geometriai formájú homogén testek. A kristályt felépítő alkotórészek milyensége szerint megkülönböztetünk: • atomrácsos, • ionrácsos, • molekularácsos és • fémrácsos anyagokat.
A kristályos anyagok jellemzői: • a rácsenergia, • az elemi cella és • a koordinációs szám. • A rácsenergia (Er) egyenlő azzal az energiával, amely szükséges, hogy 1 mól kristályos anyagból gáz halmazállapotú ionok keletkezzenek. NaCl(sz)= Na+(g) + Cl-(g)Er(NaCl)=756 kJ/mol
Az elemi cella (elemi kristályrács) a kristály legkisebb jellemző része, amely még ugyanolyan tulajdonságokkal rendelkezik, mint a makroszkópikus kristály. Az elemi cellák alakja azonos a kristályéval.
Az elemi kristályrács alakja szerint a kristályos anyagokat hét kristályrendszerbe sorolhatjuk.
Lapközepes kockarács Térközepes kockarács Hexagonális (hatszöges) rács
A koordinációs száma központi atom vagy ion ligandumainak száma. A kristályrács esetén egy kiszemelt atomtörzshöz, molekulákhoz vagy ionhoz legközelebb lévő atomtörzsek, molekulák vagy ellentétes töltésű ionok száma.
Kristályrácstípusok • A kristályos anyagokat az alkotórészek minősége szerint feloszthatjuk: • molekularácsos, • ionrácsos, • atomrácsos és • fémrácsos anyagokra.
A molekularácsban két- vagy többatomos molekulák vannak. A molekulák között ható vonzóerőt van der Waals-kötésnek nevezzük. • Két szomszédos molekula atommagjának a távolsága, a van der Waals kötéstávolság. Ez a kötés minden irányban egyformán hat.
A molekularácsos anyagok: • nem kemények, • olvadáspontjuk, forráspontjuk alacsony, • vízben főleg kémiailag oldódnak. Molekularácsos anyagok pl. a: jég, szilárd CO2, szilárd HCl, fehérfoszfor (P4), Cl2, Br2, H2O, H2SO4, HNO3, stb.
Az ionrácsban egymás mellett ellentétes töltésű ionok vannak. Az ellentétes töltésű ionok között elektrosztatikus vonzóerő hat.
Az ionok között ható erős vonzóerő miatt az ionrácsos anyagok: • kemények, • olvadáspontjuk, forráspontjuk magas, • vizes oldatuk és olvadékuk vezeti az áramot. • Az áram vezetésében az oldatban és olvadékban mozgó ionok vesznek részt. Ionrácsos anyagok pl. a: NaCl, ZuCl2, NaNO3, KCl, NaOH, ZuSO4, K2CO3 stb.
Az atomrácsban az atomok összefüggően, lokalizált kovalens kötésekkel kapcsolódnak egymáshoz.
Az atomrácsos anyagok: • nagyon kemények, • olvadáspontjuk, forráspontjuk magas, • a hőt és az elektromosságot nem, vagy rosszul vezetik. Atomrácsos anyagok pl. a: C, B, Si, Ge, SiC, SiO2, ZuS, stb.