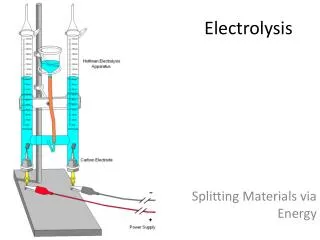
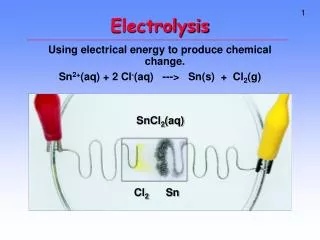
Electrolysis & Coulometry
Electrolysis & Coulometry. Assoc. Prof. Dr. Jaroon Jakmunee SCB2324 E-mail: jakmunee@gmail.com. Electrolysis. การแยกสลายด้วยไฟฟ้า – การใช้ไฟฟ้าไปทำให้เกิดปฏิกิริยา (รีดอกซ์) จะต้องให้ศักย์ไฟฟ้าจากภายนอกแก่เซลล์ไฟฟ้า - ศักย์ที่ให้จะต้องสูงพอจึงจะเกิดปฏิกิริยาได้

Electrolysis & Coulometry
E N D
Presentation Transcript
Electrolysis & Coulometry Assoc. Prof. Dr. Jaroon Jakmunee SCB2324 E-mail: jakmunee@gmail.com
Electrolysis การแยกสลายด้วยไฟฟ้า – การใช้ไฟฟ้าไปทำให้เกิดปฏิกิริยา (รีดอกซ์) จะต้องให้ศักย์ไฟฟ้าจากภายนอกแก่เซลล์ไฟฟ้า - ศักย์ที่ให้จะต้องสูงพอจึงจะเกิดปฏิกิริยาได้ เมื่อเกิดปฏิกิริยาจะมีกระแสไฟฟ้าไหลผ่านเซลล์ไฟฟ้า ต้องให้ศักย์เท่าไรจึงจะเกิดปฏิกิริยา....
เซลล์ไฟฟ้าเคมีชนิดอิเล็กโทรไลติกเซลล์ไฟฟ้าเคมีชนิดอิเล็กโทรไลติก • ให้ศักย์ไฟฟ้าจากภายนอกแก่เซลล์ไฟฟ้า • เกิดปฏิกิริยาตรงข้ามกับกัลวานิกเซลล์ • ศักย์ไฟฟ้าที่ต้องให้จะมากกว่าศักย์ของกัลวานิกเซลล์เสมอ Minimum decomposition potential, Ed
การเกิดปฏิกิริยาในเซลล์กัลวานิกและเซลล์อิเล็กโทรไลติก ทิศทางการเปลี่ยนแปลงของศักย์ไฟฟ้าเมื่อมีปฏิกิริยาเกิดขึ้นในเซลล์กัลวานิก Zn -0.76 Cu +0.34 Zn -0.76 Cu +0.34 Erev = 1.10 V ทิศทางการให้ศักย์ไฟฟ้าเพื่อให้เกิดปฏิกิริยาในทางตรงกันข้ามในเซลล์อิเล็กโทรไลติก
ศักย์ไฟฟ้าที่เกี่ยวข้องในเซลล์อิเล็กโทรไลติก Ed = Erev + EIR + EC + Ea • Erev = ศักย์ไฟฟ้าที่ต้องใช้เพื่อต้านศักย์ไฟฟ้าของเซลล์กัลวานิกซึ่งมีค่าเท่ากับ ศักย์ไฟฟ้าของเซลล์ที่จุดสมดุล (reversible cell potential) จะมีค่าศักย์ไฟฟ้าเท่ากับที่วัดได้จากเทคนิคโพเทนชิออเมตรี • EIR = Ohmic drop หรือ IR drop เป็นศักย์ที่ตกคร่อมความต้านทานของอิเล็กโทรไลต์ในเซลล์(ความต้านทานหรือความนำไฟฟ้าของเซลล์วัดได้โดยเทคนิคการวัดความนำไฟฟ้า) • EC = ศักย์ไฟฟ้าโพลาไรเซชันความเข้มข้น (concentration polarization potential) คือศักย์ไฟฟ้าที่เกิดจากการเปลี่ยนแปลงความเข้มข้นที่ผิวขั้วไฟฟ้า โดยเมื่อเกิดปฏิกิริยาขึ้นทำให้ความเข้มข้นของสารที่ผิวขั้วไฟฟ้าต่ำกว่าความเข้มข้นในสารละลายส่วนใหญ่ (bulk solution) ทำให้ต้องให้ศักย์ไฟฟ้าเพิ่มขึ้นเพื่อให้เกิดปฏิกิริยาได้เท่าเดิม • Ea = ศักย์ไฟฟ้าเกินกัมมันต์ (activation overpotential) คือศักย์ไฟฟ้าที่เกี่ยวข้องกับจลนศาสตร์ของปฏิกิริยา โดยต้องให้ศักย์ไฟฟ้าเพิ่มขึ้นเพื่อเอาชนะพลังงานก่อกัมมันต์ที่จะทำให้เกิดปฏิกิริยาได้
ศักย์ไฟฟ้าที่เกี่ยวข้องในเซลล์อิเล็กโทรไลติกศักย์ไฟฟ้าที่เกี่ยวข้องในเซลล์อิเล็กโทรไลติก Eapplied = Erev + EIR + EC + Ea Ea คือ ศักย์ไฟฟ้าเกิน ซึ่งจะเกิดขึ้นที่ทั้ง 2 ขั้ว
การวัดศักย์ไฟฟ้าเกิน หรือการโพลาไรซ์ของขั้วไฟฟ้า • วัดศักย์ไฟฟ้าของขั้ว C เมื่อมีกระแสไหล • วัดอีกครั้งเมื่อไม่มีกระแสไหล • = E ครั้งที่ 1 – E ครั้งที่ 2 • รูป set up ของเครื่องมือในการวัดศักย์ไฟฟ้าเกิน Tafel’s equation: = a + b log | i | | i | คือ ขนาดของความหนาแน่นของกระแสไฟฟ้า (ไม่คิดเครื่องหมาย) มีหน่วยเป็น A/cm2, a และ b คือค่าคงที่
จลนศาสตร์ของปฏิกิริยาไฟฟ้าเคมีจลนศาสตร์ของปฏิกิริยาไฟฟ้าเคมี • (a) เป็นขณะที่ยังไม่มีการให้ศักย์แก่ขั้วไฟฟ้า: อิเล็กตรอนที่ขั้วและออร์บิทัลว่างของสารที่อยู่ในสารละลายมีพลังงานต่างกันเท่ากับ zFE • (b) เมื่อให้ศักย์ไฟฟ้า (ไปทางลบ) เป็นการเพิ่มพลังงานให้อิเล็กตรอนที่ขั้วไฟฟ้าจนขึ้นไปเท่ากับออร์บิทัลว่างของสารในสารละลาย • (c) เมื่อเพิ่มศักย์ไฟฟ้าขึ้นไปอีกเท่ากับศักย์ไฟฟ้าเกิน () จะทำให้อิเล็กตรอนมีพลังงานสูงขึ้น ซึ่งพลังงานส่วนหนึ่งจะลด G# ลงเท่ากับ FE ทำให้ระยะในการทะลุผ่านลดลง ทำให้เกิดปฏิกิริยาได้เร็วขึ้น
สมการที่เกี่ยวข้อง สมการArrhenius: k = A e-Ea/RT; k = rate constant ใช้อธิบายจลนศาสตร์ของปฏิกิริยาเคมี สามารถเขียนสมการสำหรับกรณีปฏิกิริยาไฟฟ้าเคมีได้เป็น กรณีรูป (b) io = C e-G#/RT กรณีรูป (c) จะมีกระแสไฟฟ้าไหลเท่ากับ i (กระแส แปรผันโดยตรงกับอัตราการเกิดปฏิกิริยา) i= C e-(G# - FE/RT) = C e-G#/RT .e FE/RT = io eFE/RT หรือเขียนอย่างง่ายเป็นi = Ae ซึ่งเมื่อ take log จะได้สมการ Tafel = a + b log | i | แสดงว่า overpotential เกี่ยวข้องกับจลนศาสตร์ของปฏิกิริยา ถ้ามีค่ามาก แสดงว่ามีพลังงานกระตุ้นหรือกำแพงพลังงานในการเกิดปฏิกิริยาสูง
ข้อดี-ข้อเสียของ overpotential ศักย์ไฟฟ้าเกินทำให้เกิดปฏิกิริยายากขึ้นต้องใช้พลังงานไฟฟ้ามากขึ้นเพื่อให้เกิดปฏิกิริยาได้ผลิตผลเท่าเดิม เรียกว่ามี energy efficiency ต่ำลง ตัวแปรที่มีผลต่อ : -ชนิดขั้วไฟฟ้า, ความขรุขระของผิวขั้ว กระบวนการผลิตอลูมิเนียม พลังงานที่ใช้ = ศักย์ไฟฟ้า x ปริมาณประจุ
ข้อดีของ overpotential Hydrogen overvoltage on Hg electrode การเกิดปฏิกิริยารีดักชันของไฮโดรเจนไอออนไปเป็นแก๊สไฮโดรเจนบนขั้วแพลทินัมจะเกิดที่ 0 โวลต์เทียบกับ NHE แต่บนขั้วปรอท (Hg) จะต้องให้ศักย์เป็นลบมากกว่านี้ (-2 V) จึงจะเกิดปฏิกิริยา ซึ่งช่วงศักย์ 0 ถึง -2V นี้เป็นช่วงที่สารหลายชนิดเกิดรีดักชัน จึงใช้ขั้วปรอทในการศึกษาปฏิกิริยาเหล่านั้นได้โดยไม่มีการรบกวนจาก H+ บนขั้วตะกั่วในแบตเตอรีก็มี Hydrogen overvoltage สูงเช่นกัน แต่ถ้ามีโลหะปนเปื้อน แบตเตอรีจะเสื่อมเพราะชาร์ตไฟไม่เข้าเนื่องจากเกิดปฏิกิริยาของ H+ แทน Pb2+ Lead acid battery
ขั้วไฟฟ้าชนิดโพลาไรซ์ได้และชนิดนอนโพลาไรซ์ขั้วไฟฟ้าชนิดโพลาไรซ์ได้และชนิดนอนโพลาไรซ์ • ขั้วไฟฟ้าโพลาไรซ์(polarized electrode) เมื่อมีการให้ศักย์ไฟฟ้าจากภายนอกแก่ขั้วไฟฟ้าจะทำให้ขั้วไฟฟ้ามีศักย์ไฟฟ้าเปลี่ยนไปตามศักย์ไฟฟ้าจากภายนอกโดยไม่เกิดกระแสไหลผ่านขั้ว ขั้วไฟฟ้าส่วนใหญ่จะมีสมบัติเป็นขั้วโพลาไรซ์ในบางช่วงศักย์ไฟฟ้าเท่านั้น • ขั้วไฟฟ้านอนโพลาไรซ์(nonpolarized electrode) จะเกิดปฏิกิริยาให้กระแสสูงมากเพื่อต้านการเปลี่ยนแปลงศักย์ไฟฟ้าเมื่อมีการให้ศักย์จากภายนอกเข้าไป
ขั้วไฟฟ้าอ้างอิง-กลไกการเป็นขั้วนอนโพลาไรซ์ขั้วไฟฟ้าอ้างอิง-กลไกการเป็นขั้วนอนโพลาไรซ์ • Saturated calomel electrode (SCE) สามารถรักษาศักย์ไฟฟ้าให้คงที่ได้ แม้จะมีการให้สนามไฟฟ้าจากภายนอก
การนำเซลล์อิเล็กโทรไลติกมาใช้ในการวิเคราะห์การนำเซลล์อิเล็กโทรไลติกมาใช้ในการวิเคราะห์ อิเล็กโทรกราวิเมตรี คูลอมบ์เมตรี โวลแทมเมตรี
คูลอมบ์เมตรี (coulometry) คูลอมบ์เมตรีเป็นเทคนิคในการหาปริมาณสาร โดยการวัดปริมาณไฟฟ้าที่สัมพันธ์โดยตรงกับปฏิกิริยาเคมีที่เกิดขึ้น ตามกฎของฟาราเดย์เกี่ยวกับการแยกสลายด้วยไฟฟ้า โดยปริมาณไฟฟ้า 1 ฟาราเดย์ (F) จะเกี่ยวข้องกับการเกิดปฏิกิริยาของสาร 1 สมมูล ซึ่งเกี่ยวข้องกับอิเล็กตรอนจำนวน 1 โมล เช่น Ag+(aq) + e- Ag(s) และ Zn2+(aq) + 2e- Zn(s) ในกรณีของ Ag+ปริมาณ 1 สมมูลเท่ากับ 1 โมล ส่วนกรณี Zn2+ปริมาณ Zn2+ 1 สมมูลจะเท่ากับ 0.5 โมล เป็นต้น ไฟฟ้าทำหน้าที่เป็นรีเอเจนต์ตัวหนึ่งนั่นเอง โดยขั้วไฟฟ้าอาจทำหน้าที่ให้หรือรับอิเล็กตรอนขึ้นอยู่กับศักย์ของขั้วไฟฟ้าเมื่อเทียบกับสารที่มาเกิดปฏิกิริยา โดย ปริมาณไฟฟ้า 1 F = 6.022x1023 e- x 1.6022x10-19 C/e- = 96487 คูลอมบ์ (C)
คูลอมบ์เมตรี (coulometry) ปริมาณไฟฟ้า (หรือจำนวนอิเล็กตรอน) สามารถวัดได้จากกระแสไฟฟ้าและเวลา โดยในกรณีกระแสคงที่ปริมาณไฟฟ้า (Q) ในหน่วยคูลอมบ์เท่ากับผลคูณของกระแสไฟฟ้า (A) กับเวลา (s) Q = it ปริมาณไฟฟ้าในหน่วยฟาราเดย์ = ปริมาณไฟฟ้าในหน่วยคูลอมบ์ /96487 จำนวนโมล (n) ของสารสัมพันธ์กับปริมาณไฟฟ้า ดังสมการ n = Q / zF ; z = จำนวนโมลของอิเล็กตรอน เทคนิคคูลอมบ์เมตรี อาศัยการวัดปริมาณไฟฟ้าที่ใช้ในการเกิดปฏิกิริยาของสารทั้งหมดแล้วคำนวณหาปริมาณสารจากปริมาณไฟฟ้าที่ใช้ไป การวิเคราะห์จะถูกต้องก็ต่อเมื่อประสิทธิภาพกระแส (current efficiency) เป็น 100 เปอร์เซ็นต์
คูลอมบ์เมตรี (coulometry) เพื่อให้สารที่สนใจวิเคราะห์ในสารละลายเกิดปฏิกิริยาจนหมดอย่างมีประสิทธิภาพกระแสสูง ต้องใช้ขั้วไฟฟ้าขนาดใหญ่เท่าที่จะทำได้ เช่น mercury pool, Pt foil เป็นต้น คูลอมบ์เมตรีแบ่งออกเป็น 2 เทคนิคย่อย คือ 1. คูลอมบ์เมตรีแบบควบคุมศักย์ไฟฟ้า (controlled potential (potentiostatic) coulometry) - เพื่อให้สารบางชนิดเท่านั้นเกิดปฏิกิริยา 2. คูลอมบ์เมตรีแบบควบคุมกระแสไฟฟ้า (controlled current coulometry หรือ coulometric titration) - ใช้ไฟฟ้ามาผลิตไทแทรนต์
คูลอมบ์เมตรีแบบควบคุมศักย์ไฟฟ้าคูลอมบ์เมตรีแบบควบคุมศักย์ไฟฟ้า ในคูลอมบ์เมตรีแบบควบคุมศักย์ไฟฟ้า ศักย์ไฟฟ้าของขั้วทำงานจะถูกควบคุมให้คงที่ตลอดเวลาเทียบกับขั้วอ้างอิง ลักษณะของเซลล์ไฟฟ้า (coulometric cell) แสดงดังรูป ซึ่งจะใช้ขั้วไฟฟ้าขนาดใหญ่และมีการคนสารละลายอย่างสม่ำเสมอเพื่อให้ได้ประสิทธิภาพกระแสสูง โดยเลือกศักย์ไฟฟ้าที่ analyte สามารถเกิดปฏิกิริยาโดยไม่มีการรบกวนจากสารอื่น เมื่อทำการแยกสลายด้วยไฟฟ้าจะพบว่ากระแสไฟฟ้าจะลดลงแบบเอ็กโปเนนเชียลเทียบกับเวลา (ตามความเข้มข้นที่ลดลง) ดังรูป ปริมาณไฟฟ้าหาได้จากการอินติเกรตพื้นที่ใต้กราฟ • it = io e-kt ; k = first order electrolytic rate constant • In it = ln io - kt ; • k = AD/ V • A = พื้นที่ผิวของขั้วไฟฟ้า • D = ค่าสัมประสิทธิ์ของการแพร่ • = ความหนาของชั้นการแพร่ • V = ปริมาตรของสารละลาย • log it = log io – kt /2.303 • ถ้าสร้างกราฟระหว่าง log it กับ t จะได้เส้นตรงที่มีความชันเท่ากับ –k /2.303
คูลอมบ์เมตรีแบบควบคุมศักย์ไฟฟ้า มีการประยุกต์ในการวิเคราะห์สารอนินทรีย์หลายชนิด โดยเฉพาะอย่างยิ่งเป็นเทคนิคการวิเคราะห์ยูเรเนียมและพลูโตเนียมที่มีการรบกวนการวิเคราะห์น้อยมาก รวมทั้งใช้ในการวิเคราะห์ (และสังเคราะห์) สารอินทรีย์หลายชนิด เช่น กรดไตรคลอโรอะซิติก (trichloroacetic acid) และ กรดพิคริก (picric acid) ดังสมการ ซึ่งเทคนิคนี้สามารถใช้หาจำนวนอิเล็กตรอนที่เกี่ยวข้องในปฏิกิริยาได้ด้วย คูลอมบ์เมตรีแบบควบคุมศักย์ไฟฟ้า
คูลอมบ์เมตรีแบบควบคุมกระแส อาจเรียกอีกอย่างว่า คูลอมบ์เมตริกไทเทรชันเนื่องจากเป็นการนำเทคนิคคูลอมบ์เมตรี มาใช้ในการผลิตไทแทรนต์สำหรับการไทเทรตด้วยอัตราคงที่ (ด้วยการให้กระแสคงที่) ลักษณะคล้ายกับการเติมไทแทรนต์จากบิวเรตด้วยอัตราคงที่ ไทแทรนต์ที่ผลิตขึ้นจะทำปฏิกิริยากับสารที่ต้องการวิเคราะห์ (titrand) จนกระทั่งถึงจุดยุติ แล้วจึงคำนวณหาปริมาณไทแทรนต์ที่ใช้ในการไทเทรตจากปริมาณไฟฟ้าที่ใช้ไป ซึ่งจะใช้หาปริมาณ analyte หรือ titrand ที่เกี่ยวข้องในปฏิกิริยาการไทเทรต ต่อไป เพื่อให้ได้ผลการวิเคราะห์ที่ถูกต้อง ปฏิกิริยาไฟฟ้าเคมีในการผลิตไทแทรนต์จะต้องมี ประสิทธิภาพกระแส 100 เปอร์เซ็นต์ นั่นคือ ต้องไม่มีปฏิกิริยาข้างเคียงอื่น ๆ เกิดขึ้น และ titrand เองต้องไม่เกิดปฏิกิริยาที่ขั้วไฟฟ้า วิธีคูลอมบ์เมตรีจะมีความละเอียดกว่าการวัดปริมาตร เนื่องจากใช้ 96487 คูลอมบ์ต่อการเกิดปฏิกิริยา 1 สมมูล ซึ่งถ้าใช้กระแสคงที่ 1 มิลลิแอมแปร์ใช้เวลา 1 วินาที จะเทียบเท่ากับปริมาณ 10-8 สมมูล ปกติจะใช้กระแสคงที่ในช่วง 1-100 มิลลิแอมแปร์ โดยมีความคลาดเคลื่อนของกระแสไฟฟ้าน้อยกว่า 0.1 เปอร์เซ็นต์ ตัวแปรสำคัญอีกส่วน คือ การตรวจวัดจุดยุติและเวลาให้ถูกต้อง ซึ่งมักจะใช้การตรวจวัดแบบโพเทนชิออเมตรีและแอมเพอโรเมตรี ไทแทรนต์จะถูกผลิตจากสารเริ่มต้น (precursor) ในขณะที่ทำการไทเทรตและถูกใช้ในทันที จึงสามารถใช้ไทแทรนต์ที่ไม่เสถียรในการไทเทรตได้ คูลอมบ์เมตรีแบบควบคุมกระแสหรือคูลอมบ์เมตริกไทรเทรชัน
มีการพัฒนาวิธีคูลอมบ์เมตริกไทเทรชันไปใช้กับการไทเทรตปฏิกิริยาต่าง ๆ ดังตาราง คูลอมบ์เมตรีแบบควบคุมกระแสหรือคูลอมบ์เมตริกไทรเทรชัน
การประยุกต์ที่ใช้อย่างกว้างขวางมากที่สุด และเป็นระบบวิเคราะห์ที่ดีที่สุดสำหรับการวิเคราะห์น้ำปริมาณน้อย ๆ คือ Karl-Fisher titrationsในระบบดังกล่าวจะมีการผลิตไอโอดีนที่ขั้วแอโนด ซึ่งเป็นส่วนประกอบสำคัญของ Karl-Fisher titrant ปฏิกิริยาที่เกี่ยวข้องแสดงดังสมการ C6H5N.I2+ C6H5.SO2 + C6H5N + CH3OH + H2O 2C6H5N.HI + C6H5NH.SO4CH3 โดยตรวจวัดจุดยุติด้วยเทคนิคแอมเพอโรเมตรี (biamperometric detection) ซึ่งมีความไวสูงและตอบสนองเร็ว ทำให้การวิเคราะห์มีความถูกต้องและแม่นยำสูง คูลอมบ์เมตรีแบบควบคุมกระแสหรือคูลอมบ์เมตริกไทรเทรชัน
ลักษณะเซลล์สำหรับทำคูลอมบ์เมตริกไทเทรชัน แสดงดังรูป ซึ่งมักจะแยกขั้วไฟฟ้าทั้งสองออกจากกันโดยมีสะพานเกลือคั่นเพื่อป้องกันการเกิดปฏิกิริยารบกวน นอกจากนี้ ยังมีการออกแบบระบบผลิต ไทแทรนต์ที่ใช้การไหล ทั้งแบบแขนเดียวและ 2 แขน ดังรูป ซึ่งช่วยให้การผลิตไทแทรนต์ทำได้ต่อเนื่องโดยไม่มีการรบกวนจากองค์ประกอบของสารตัวอย่าง เนื่องจากขั้วไฟฟ้าจะสัมผัสกับสารละลายอิเล็กโทรไลต์เท่านั้น เซลล์คูลอมเมตริกไทเทรชัน