请用图示法表示物质的分类,并思考分类的依据。
请用图示法表示物质的分类,并思考分类的依据。. 氧化物. 有机物. 化合物. 酸. 无机物. 纯净物. 碱. 盐. 金 属. 物质. 单 质. 非金属. 混合物. 惰性气体. 一、纯净物和混合物 二、单质和化合物 三、氧化物、酸、碱、盐. 第二节 物质的分类. 第二节 物质的分类. 思考 : 纯净物与混合物的主要区別在什么地方? 如何判断?请举例说明。. 纯净物 混合物 区别 有固定组成 没有固定组成 性质能确定 性质不能确定 联系 混合物是由多种物质简单混合形成.

请用图示法表示物质的分类,并思考分类的依据。
E N D
Presentation Transcript
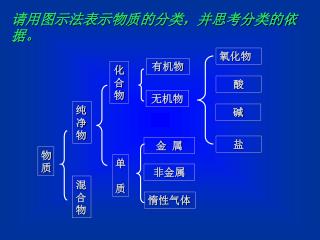
请用图示法表示物质的分类,并思考分类的依据。 氧化物 有机物 化合物 酸 无机物 纯净物 碱 盐 金 属 物质 单 质 非金属 混合物 惰性气体
一、纯净物和混合物 二、单质和化合物 三、氧化物、酸、碱、盐 第二节 物质的分类 第二节 物质的分类
思考:纯净物与混合物的主要区別在什么地方? 如何判断?请举例说明。 纯净物 混合物 区别 有固定组成 没有固定组成 性质能确定 性质不能确定 联系 混合物是由多种物质简单混合形成 讨论:如何通过实验证明某瓶水是纯净物? 练习p.11 返回
思考:单质与化合物的区分点在什么地方? 讨论p12 单质 化合物 区别 a 由一种元素组成 由多种元素组成 b 元素化合价为零 元素化合价不为零 c 元素以游离态存在 元素以化合态存在 联系 都是纯净物,都有固定的组成和确定的性质 讨论: 一种元素组成 的物质是否一定是纯净物?
某物质经分析,只含一种元素,则此物质 A、一定是一种单质 B、一定是纯净物 C、一定是混和物 D、可能是纯净物,也可能是混和物
思考:请举例说明单质中物质的分类有哪些? 分类 依据是什么? 举例说明。 金属单质 非金属单质 区别 原子易失电子 原子易得电子 性质 还原性有光泽 有氧化性一般无光泽 良好的导热导电延展性 不导电,导热性差 常温下为固体 (汞) 通常为固体和气体(溴) 联系 金属和非金属之间没有绝对的界限。 如: 锗和硅是常见的半导体,它们既能表现出金属性,有时又能表现出非金属性 。
有机物 无机物 区别 大多数有可燃性 大多数无可燃性 结构较复杂 结构较简单 能在发生反应的同时 一般无副反应 伴有副反应 发生 联系 有机物与无机物之间没有绝对的界限 如 H2CO3 返回
酸性氧化物 碱性氧化物 两性氧化物 不成盐氧化物 金属氧化物 非金属氧化物 思考:化合物中物质的分类有哪些? 分类依据是什么? 举例说明。 三、氧化物、酸、碱、盐 1、氧化物 练习P12
下列说法是否正确? 请举例说明。 (A) 酸性氧化物一定是非金属氧化物 (B)碱性氧化物一定是金属氧化物 (C)非金属氧化物一定是酸性氧化物 (D)金属氧化物一定是碱性氧化物 请用实验证明氧化铁、氧化硅、氧化铝分别属于哪一类氧化物?。
无氧酸 含氧酸 一元酸 强酸 高沸点酸 二元酸 弱酸 挥发性酸 多元酸 2、酸 d 酸酐 a定义 c 通性 b分类 Lx-p13 注意:金属活动顺序表在金属与酸的反应中的应用 什么是酸酐? 如何确定? 酸性氧化物一定是酸酐吗? 举例说明。
一元碱 可溶性碱 强碱 二元碱 不溶性碱 多元碱 弱碱 3、碱 c 通性 a 定义 b 分类 Lx-p14 Lx-p14 不溶性碱受热分解,其对应的氧化物不能与水反应. 可溶性碱受热不分解,其对应的氧化物能与水反应
含氧酸盐 无氧酸盐 正盐 可溶性盐 酸式盐 不溶性盐 碱式盐 复盐 4、盐 a 定义 b 分类 c 性质 Lx-p14 d 电离方程式
再见! 邬红
你能记住常见的一些盐和碱的溶解性吗? 你能记住常见的一些盐和碱的溶解性吗?
3、写出下列阴阳离子所形成的化合物的 化学式并注明溶解性 K+ Na+ NH4+ Mg2+ Al3+ Zn2+ Fe2+ Fe3+ Cu2+ Ag+ NO3- OH- Cl- SO42- CO3 2-
Al2O3+6HCl→ 2AlCl3+3H2O Al(OH)3 + 3HCl → AlCl3 +3H2O Al2O3+ 2NaOH → 2NaAlO2 + H2O Al(OH)3 + NaOH → NaAlO2 +2 H2O H 3 AlO3 + NaOH → NaAlO2 +2 H2O HAlO2 + H2O
NaHCO3+HCl NaCl +CO2 +H2O NaHCO3+NaOH Na2CO3+H2O Ca(HCO3) 2 +HCl NaCl + H2O + CO2 Ca(HCO3) 2 + Ca(OH)2 CaCO3+H2O 2NaHCO3 + Ca(OH)2 CaCO3 +Na2CO3 + 2H2O NH4HCO3+HCl NaCl +CO2+H2O 2NH4HCO3+2NaOH (少量) (NH4 ) 2CO3 +Na2CO3 +2H2O
Al2O3+6HCl→2AlCl3+3H2O Al2O3+ 2NaOH → 2NaAlO2 + H2O Fe2O3+6HCl→2FeCl3+3H2O Fe2O3+NaOH→ SiO2+2NaOH→Na2SiO3+H2O SiO2+HCl→
KAl(SO4)2·12H2O 或K2SO4·Al2(SO4)3·24H2O 明矾石(明矾) 十二水合硫酸铝钾 二十四水合硫酸铝钾 光卤石 KCl·MgCl2·6H2O