实验现象:铜片上没有 气泡产生,而 锌片上有气泡产生。
2e -. 实验现象:铜片上没有 气泡产生,而 锌片上有气泡产生。. Zn + 2H + = Zn 2+ + H 2 ↑. 一、原电池 1、定义:这种将化学能转变为电能的装置叫做原电池。. 实验现象: 电流计指针发生偏转, Cu 片上有气泡产生. e -. e -. e -. e -. H +. H +. H +. H +. H +. H +. Zn 2+. Zn 2+. H 2. H 2. SO 4 2-. SO 4 2-. SO 4 2-. 2 、工作原理. 利用发生的氧化还原反应中电子的转移而形成电流。. 3 、电极及电极反应.

实验现象:铜片上没有 气泡产生,而 锌片上有气泡产生。
E N D
Presentation Transcript
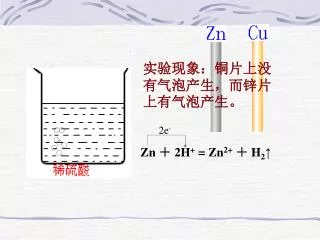
2e- 实验现象:铜片上没有气泡产生,而锌片上有气泡产生。 Zn + 2H+ = Zn2++ H2↑
一、原电池 1、定义:这种将化学能转变为电能的装置叫做原电池。 实验现象:电流计指针发生偏转,Cu片上有气泡产生
e- e- e- e- H+ H+ H+ H+ H+ H+ Zn2+ Zn2+ H2 H2 SO42- SO42- SO42- 2、工作原理 利用发生的氧化还原反应中电子的转移而形成电流。 3、电极及电极反应 Cu Zn 负极:电子流出的极。 锌片:Zn—2e-=Zn2+ (氧化反应) 正极:电子流入的极。 (还原反应) 铜片:2H++2e- = H2↑ 总反应:Zn + 2H+ = Zn2++ H2↑
实验探究形成原电池的条件 (可以) (可以) (可以) 形成条件一: 活泼性不同的两个电极 负极:较活泼的金属 正极:较不活泼的金属、非金属 (不可以) 第一组实验
实验探究形成原电池的条件 (可以) (不可以) 形成条件二:电极需插进电解质溶液中; 第二组实验
实验探究形成原电池的条件 (不可以) (可以) 形成条件三:必须形成闭合回路 第三组实验
实验探究形成原电池的条件 ZnSO4溶液 (可以) (不可以) 形成条件四:自发进行的氧化还原反应。 第四组实验
二、形成原电池的条件: 1.两个电极(活泼性不同); 负极:较活泼金属 正极:较不活泼金属、石墨等 2.电极需插进电解质溶液中; 3.必须形成闭合回路; 4.自发进行的氧化还原反应。
一、原电池 1、定义:这种将化学能转变为电能的装置叫做原电池。 小 结 2、工作原理:利用发生的氧化还原反应中电子的转移而形成电流。 3、电极及电极反应 负极:电子流出的极。 正极:电子流入的极。 你记住了吗? 4、形成条件: ①有两种活泼性不同的电极 ②材料均插入电解质溶液中 ③两极相连形成闭合电路 ④进行的氧化还原反应
思考题: 请根据反应 Fe + 2Fe 3+ = 3Fe 2+ 设计一个原电池,画出装置图 预习:1、本节 “二、化学电源” 2、“三、 金属的电化学腐蚀