Composti chimici
310 likes | 988 Views
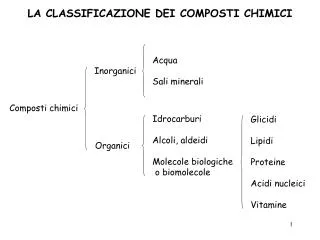
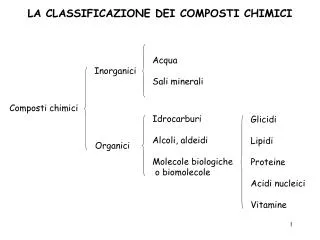
Acqua Sali minerali. Inorganici . Idrocarburi Alcoli, aldeidi Molecole biologiche o biomolecole. Glicidi Lipidi Proteine Acidi nucleici Vitamine. Organici. LA CLASSIFICAZIONE DEI COMPOSTI CHIMICI. Composti chimici . I COMPOSTI ORGANICI. Contengono atomi di carbonio

Composti chimici
E N D
Presentation Transcript
Acqua Sali minerali Inorganici Idrocarburi Alcoli, aldeidi Molecole biologiche o biomolecole Glicidi Lipidi Proteine Acidi nucleici Vitamine Organici LA CLASSIFICAZIONE DEI COMPOSTI CHIMICI Composti chimici
I COMPOSTI ORGANICI Contengono atomi di carbonio Costituiscono gli organismi viventi
LE MOLECOLE BIOLOGICHE O BIOMOLECOLE Costituiscono le strutture presenti negli organismi viventi
Organismi autotrofi(Es. piante): sintetizzano zuccheri (glucosio) a partire da componenti inorganici quali acqua e CO2 mediante il processo di fotosintesi clorofilliana. Organismi eterotrofi (Es. animali): soddisfano il fabbisogno energetico nutrendosi di alimenti che contengono zuccheri. Ecco alcuni esempi: frutta e miele -> fruttosio; glucosio barbabietola da zucchero, zucchero di canna -> saccarosio latte e latticini -> lattosio cereali (pane, pasta, riso), tuberi (patate) e legumi -> amido carne e pesce -> glicogeno GLICIDI o ZUCCHERI o CARBOIDRATI Caratteristiche: Sono composti chimici costituiti da carbonio, idrogeno e ossigeno. Sono molto abbondanti in natura. Hanno sapore dolce. Funzioni: Strutturale: costituiscono strutture essenziali per gli organismi viventi (funzione di sostegno, soprattutto nei vegetali cellulosa) Energetica: forniscono energia per svolgere tutte le funzioni dell'organismo Protezione: costituiscono l’esoscheletro degli invertebrati (chitina)
Ribosio Desossiribosio 5C Componenti degli acidi nucleici Monosaccaridi (formati da 1 molecola di zucchero) Glucosio principale fonte di energia Fruttosio si trova nella frutta Galattosio 6C Disaccaridi (formati da 2 molecole di zucchero) Glucosio + fruttosio Saccarosio(comune zucchero da cucina) Glucosio + glucosio Maltosio (deriva da digestione dell’amido) Glucosio + galattosio Lattosio (in latte e latticini) Amido riserva energetica nei vegetali (cereali, tuberi, legumi) si accumula in amiloplasti nella cellula vegetale si trova nei semi e nelle radici Glicogeno riserva energetica negli animali si accumula in muscoli e fegato Cellulosa funzione di sostegno nei vegetali si trova nella parete cellulare delle cellule vegetali può essere digerita solo dagli erbivori è il composto organico più abbondante sulla Terra Polisaccaridi (formati da più di 20 molecole di glucosio) I diversi tipi di glicidi
Reazione di condensazione Glucosio Fruttosio O OH HO H2O Saccarosio Reazione di condensazione Glucosio Glucosio O OH HO H2O Maltosio Reazione di condensazione Glucosio Galattosio OH O HO H2O Lattosio Come si formano i disaccaridi?
Monomeri di glucosio Granuli di amido in cellule di tubero di patata Amido Granuli di glicogeno nel tessuto muscolare Glicogeno Fibre di cellulosa nella parete di una cellula vegetale Cellulosa Molecole di cellulosa I polisaccaridi di interesse biologico 0 • L’amido e il glicogeno immagazzinano zuccheri di riserva • La cellulosa si trova nelle pareti delle cellule vegetali
LIPIDI Caratteristiche: sono costituiti da lunghe catene di atomi di carbonio, idrogeno e ossigeno sono comunemente chiamati grassi sono untuosi al tatto sono insolubili in acqua (idrofobi = “paura dell’acqua”) Funzioni: riserva energetica (molecole ad alto contenuto energetico; si accumulano nel tessuto adiposo, ad esempio nel derma) protezione meccanica per alcuni organi (cuore, fegato, reni....) isolante termico (es. grasso animale) impermeabilizzante (es. cere sulle penne degli uccelli) funzione strutturale (nelle membrane cellulari fosfolipidi) precursori di importanti molecole biologiche (ormoni, vitamine)
Ac. oleico I trigliceridi (detti anche grassi) Sono costituiti da una molecola di glicerolo + 3 catene di acidi grassi Sono rappresentati dai comuni grassi ed olii. Rappresentano una fonte energetica superiore rispetto ai carboidrati Si accumulano nel tessuto adiposo (grasso sottocuteneo). Svolgono anche la funzione di isolante termico. Grassi di origine vegetale liquidi a temperatura ambiente (es. olio di oliva, olio di semi) Grassi di origine animale solidi a temperatura ambiente (es. burro, lardo, grasso animale) Acido butirrico
I fosfolipidi Prodotti nel fegato. Costituiti da: testa idrofila (fosfato, glicerolo) code idrofobe (2 catene degli acidi grassi) Principali costituenti delle membrane plasmatiche cellulari (doppio strato lipidico) insieme alle proteine di membrana
Il colesterolo e gli steroidi • Il colesterolo svolge funzioni essenziali al metabolismo: • costituente delle membrane cellulari delle cellule animali • precursore della vitamina D (importante per la crescita ossea e dei denti) • composto di partenza per la sintesi degli acidi biliari (prodotti da fegato) Può essere sintetizzato dalle cellule (origine endogena) o introdotto con la l’alimentazione (origine esogena) • costituisce gli ormoni sessuali prodotti dalle ghiandole surrenali (testosterone, aldosterone, estradiolo) ed altri ormoni steroidei (es. cortisone)
Il colesterolo in eccesso nel sangue si accumula sulle pareti interne delle arterie provocando la formazione di placche che causano arteriosclerosi. I livelli di colesterolo nel sangue vanno tenuti sotto controllo: perchè? Il colesterolo in eccesso nel fegato si accumula dando origine ai calcoli biliari
1) Essendo insolubili in acqua, le cere svolgono un’importante funzione di rivestimento protettivo ed impermeabilizzante Le penne degli uccelli La cuticola sulle foglie 3) Le api le usano per costruire le pareti degli alveari 2) Conferiscono lucentezza ai frutti (mele, pere, ciliegie) Le cere
Catene lineari (polimeri) costituiti da una sequenza di nucleotidi. I nucleotidi sono le unità fondamentali degli acidi nucleici e sono costituiti da: 1) zucchero a 5 atomi C (ribosio o desossiribosio) 2) gruppo fosfato 3) base azotata Le basi azotate sono 4: adenina (A) guanina (G) timina (T) uracile (U) citosina (C) purine pirimidine ACIDI NUCLEICI (DNA e RNA)
Struttura del DNA Deoxyribonucleic Acid (acido deossiribonucleico). La struttura del DNA fu scoperta da Watson e Crick che ricevettero il Premio Nobel nel 1953. E’ importante per la trasmissione ereditaria dei caratteri tra genitori e figli. E’ una doppia elica formata da 2 catene polinucleotidiche, cioè composte da una successione di nucleotidi, tenute insieme da legami idrogeno. I nucleotidi sono legati tra loro tramite un legame fosfodiesterico tra il fosfato di un nucleotide ed il gruppo -OH del nucleotide successivo. Le sequenze due filamenti sono complementari: - ad una A su un filamento corrisponde sempre e solo una T sul filamento complementare e viceversa; 2 legami idrogeno. - ad una C su un filamento corrisponde sempre e solo una G sul filamento complementare e viceversa; 3 legami idrogeno.
1) Replicazione o sintesi del DNA La doppia elica di DNA è “srotolata” da un’elicasi e ognuno dei due filamenti funge da stampo per la sintesi di un filamento complementare. La DNA polimerasi “legge” la sequenza del filamento stampo e ne sintetizza uno complementare impiegando i nucleotidi con base azotata complementare (per es. se trova A sul filamento “stampo”, incorpora T nel filamento “complementare”). Alla fine si ottengono 2 molecole di DNA identiche a quella originale (parentale). E’ un processo semiconservativo: ognuna delle 2 molecole ottenute è formata da un filamento parentale ed un neosintetizzato.
2) Trascrizione e traduzione del DNA Dogma centrale della biologia molecolare: DNA RNA proteina trascrizione traduzione L’informazione genetica per la sintesi proteica è conservata nel DNA sotto forma di un codice (il codice genetico) in cui la sequenza delle basi determina la sequenza degli aminoacidi nella proteina codificata. Si parla quindi di traduzione del codice genetico.
2a) Trascrizione Nel processo di trascrizione, la RNA polimerasi II usa uno dei 2 filamenti di DNA come stampo per la sintesi di RNA messaggero (mRNA). Nel mRNA la timina è sostituita dall’uracile. Il processo di trascrizione avviene nel nucleo. 2b) Traduzione mRNA viene trasferito nel citoplasma nel reticolo endoplasmatico rugoso in corrispondenza di strutture specializzate dette ribosomi. La sequenza di mRNA viene decodificata o “tradotta”. Ogni tripletta di nucleotidi (codone) è riconosciuta da un tRNA che possiede una tripletta complementare (anticodone) ed un aminoacido (AA). La concatenazione di AA dà origine ad una catena polipeptidica.
PROTEINE Caratteristiche: sono catene (polimeri) di amminoacidi sono il più abbondante materiale biologico negli organismi animali sono essenziali per la struttura e le funzioni degli esseri viventi Le informazioni per la costruzione delle proteine sono contenute nei geni, cioè nelle sequenze di DNA Funzioni: Strutturale Es. tubulina e actina sono proteine del citscheletro cheratina forma i capelli collagene componente di pelle, tendini, legamenti proteine della seta ragnatela Contrazione Es. actina e miosina contrazione muscolare Riserva ovalbumina, nell’uovo, ha funzione di riserva per l’embrione Recettoriale recepiscono i segnali inviati dalle cellule Enzimatica Es. enzimi digestivi facilitano la digestione degli alimenti Trasporto Es. emoglobina trasporta ossigeno ed anidride carbonica nei globuli rossi del sangue Segnale di comunicazione tra le cellule ormoni, fattori di crescita Difesa immunitaria Es. anticorpi combattono le infezioni
Gli amminoacidi e la formazione del legame peptidico Un aminoacido è un composto chimico caratterizzato da un gruppo amminico (NH2), un gruppo carbossilico (COOH) ed un gruppo R specifico per ogni aminoacido. In natura, esistono 20 amminoacidi diversi. Gli amminoacidi sono tenuti insieme mediante un legame peptidico: esso si forma tra il gruppo carbossilico di un amminoacido ed il gruppo amminico dell’amminoacido successivo accompagnato dalla perdita di una molecola di acqua (H2O).
La struttura delle proteine La forma della proteina è importante per svolgere la sua funzione. Il riscaldamento provoca la perdita della forma (denaturazione) e la perdita della funzione delle proteine. Struttura primaria: sequenza di amminoacidi che forma una catena polipeptidica. Struttura secondaria: catena polipetidica si ripiega a formare struttura ad -elica o struttura a foglietti . Struttura terziaria: catena polipetidica può essere lineare (proteina fibrosa) o avvolgersi su se stessa assumendo una forma quasi sferica (proteina globulare) Struttura quaternaria: associazione di più catene polipetidiche. Es. emoglobina (proteina presente nei globuli rossi, con funzione di trasporto dell’ossigeno nel sangue)
Le informazioni per la sintesi delle proteine sono contenute nel DNA DNA trascrizione in mRNA traslocazione del mRNA nel citoplasma traduzione nei ribosomi presenti nel reticolo endoplasmatico rugoso Sintesi delle proteine
VITAMINE Le vitamine sono un insieme molto eterogeneo di sostanze chimiche. Sono assunte attraverso l’alimentazione. Sono divise in 2 gruppi: • Vitamine che devono essere assunte quotidianamente (Complesso vit B; Vit C) • Vitamine che possono accumularsi (nel fegato) (vit A, vit K, vit D, vit H) 1) Vitamine A: es retinolo -> svolge importante ruolo nella vista 2) Vitamine B 3) Vitamine C: es. acido ascorbico -> partecipa a numerose reazioni metaboliche ( biosintesi di collagene, di alcuni aminoacidi e ormoni), è anti ossidante, interviene in reazioni allergiche, neutralizza i radicali liberi 4) Vitamina D: regola metabolismo del calcio ed il processo di mineralizzazione ossea 5) Vitamine H: es. biotina importante nella sintesi di glucosio e acidi grassi 6) Vitamina K: importante nella coagulazione del sangue La carenza di vitamine ha sintomi specifici a seconda del tipo di vitamina e può causare diversi disturbi o malattie.
I SALI MINERALI L’acqua, nel processo di erosione, scioglie i minerali di cui sono costituite le rocce che si trovano, ad esempio, nell’alveo dei fiumi. I sali minerali disciolti in acqua, rappresentano il residuo fisso che si trova indicato sulle etichette delle bottiglie di acqua minerali. Quando beviamo l’acqua, introduciamo nel nostro corpo anche i sali minerali. Alcuni di questi sono molto importanti per il nostro organismo: Il sodio Il potassio Il calcio molto importante per la ossa e per la contrazione muscolare Il ferro si trova in molte proteine; es nell’emoglobina serve per legare l’ossigeno Il magnesio si trova nella clorofilla