§14 羧酸衍生物
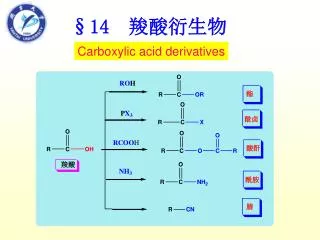
§14 羧酸衍生物. Carboxylic acid derivatives. §14.1 羧酸衍生物的结构和命名. 1 结构. Ester. Acid halide. ( F,Cl,Br,I). Acid anhydride. Amide. Nitrile. 除 腈具有碳氮三键 外, 酯、酰卤、酸酐、酰胺与羧酸一样,都有 羰基, 因羰基所连得 烃氧基、卤素、酰氧基和氨(胺)基 的吸电子能力不同, 故 羰基碳所带正电荷多寡不同 。. 1.2 羧酸衍生物 的结构比较. 结论:. 碳杂键都变短, 酰卤、酸酐变 化不明显。.

§14 羧酸衍生物
E N D
Presentation Transcript
§14 羧酸衍生物 Carboxylic acid derivatives
§14.1 羧酸衍生物的结构和命名 1 结构 Ester Acid halide (F,Cl,Br,I) Acid anhydride Amide Nitrile 除腈具有碳氮三键外,酯、酰卤、酸酐、酰胺与羧酸一样,都有羰基, 因羰基所连得烃氧基、卤素、酰氧基和氨(胺)基的吸电子能力不同, 故羰基碳所带正电荷多寡不同。
1.2 羧酸衍生物 的结构比较 结论: 碳杂键都变短, 酰卤、酸酐变 化不明显。
解释:原因有二:其一,碳的的杂化方式不同(SP2);解释:原因有二:其一,碳的的杂化方式不同(SP2); 其二,羧酸衍生物的偶极结构。 根据键长判断,酰胺的这种偶极结构含量加多,酯次之,酸酐、酰卤最少。
1.3 酰胺的结构特性 实验事实: 温度升高时,该处信号转变成一个6H的单峰。 3H 3H 1H 结论:酰胺中C-N键具有双键的性质(有人将其称为1.5键)。
1.4 腈的结构 腈中碳为SP杂化,碳氮间为三键,与炔键相似。
2 命名 2.1 酰卤的命名: 在命名时可作为酰基的卤化物,在酰基后加卤素的名称即可。 普通命名法: -溴丁酰溴 对氯甲酰苯甲酸 IUPAC 命名法: 2-溴丁酰溴 4-氯甲酰苯甲酸
2.2 酸酐的命名 单酐:在羧酸的名称后加酐字; 混酐:将简单的酸放前面,复杂的酸放后面再加酐字; 环酐:在二元酸的名称后加酐字。 普通命名法: 醋酸酐 乙丙酸酐 丁二酸酐 IUPAC 命名法: 乙酸酐 乙丙酸酐 丁二酸酐
2.3 酯的命名 酯可看作将羧酸的羧基氢原子被烃基取代的产物。命名时把羧酸名称放在前面,烃基的名称放在后面,再加一个酯字。内酯命名时,用内酯二字代替酸字并标明羟基的位置。 普通命名法: 醋酸苯甲酯-甲基--丁内酯 IUPAC 命名法: 乙酸苯甲酯2-甲基-4-丁内酯
O O ( C H ) C H C N H C H C H C H C H C N ( C H ) 3 2 3 2 2 3 2 2 - M e t h y l p r o p a n a m i d e d i m e t h y l p e n t a n a m i d e 2.4 酰胺的命名 命名时把羧酸名称放在前面将相应的酸字改为酰胺即可; N,N- 普通命名法: 异丁酰胺 N,N-二甲基戊酰胺 IUPAC 命名法: 2-甲基丙酰胺 N,N-二甲基戊酰胺
2.5 腈的命名 腈命名时要把CN中的碳原子计算在内,并从此碳原子开始编号;氰基作为取代基时,氰基碳原子不计在内。 普通命名法: -甲基戊腈 -氰基丁酸 己二腈 IUPAC 命名法: 3-甲基戊腈 2-氰基丁酸 己二腈
§14.2 羧酸衍生物的物理性质和光谱性质 1 物理性质 低级的酰氯和酸酐是有刺鼻气味的液体,高级的为固体; 低级的酯具有芳香的气味,可作为香料;十四碳酸以下 的甲酯和乙酯均为液体; 酰胺除甲酰胺外,由于分子内形成氢键,均是固体; 而当酰胺的氮上有取代基时为液体; 羧酸衍生物可溶于有机溶剂; 酰氯和酸酐不溶于水,低级的遇水分解; 酯在水中溶解度很小; 低级酰胺可溶于水。
§14.3 酰基碳上的加成-消去反应 1 通式 离去基团 2 机理
3 影响反应的因素: 反应第一步为亲核加成,羰基碳的 构型由面型转变为体型, 由此可推知:羰基碳的正电性越大,其周围空间位阻越小, 反应越容易进行;第二步为消去反应,即离去基团越易离去, 反应越容易进行。 离去基团的离去能力顺序 羧酸衍生物的羰基活性顺序 More reactive Less reactive
4 羧酸衍生物中羰基碳的反应 氨解 醇解 还原 与金属的反应 水解
§14.4酯的水解和热解 1 碱性水解(皂化)---机理的提出 机理1 -----亲核取代 烷氧断键
机理2 ---亲核取代 酰氧断键
证明方法 ⑴ 动力学研究; ⑵ 同位素跟踪;⑶ 手性醇的构型变化。 动力学研究主要解决反应的级数问题, 即对于分步反应, 那步是速控步骤。同位素跟踪及手性醇的构型是否改变主要 解决是酰氧断键还是烷氧断键的问题。 实验事实 动力学结果: 水解反应速度与酯的浓度、碱的浓度成正比。
同位素追踪结果: 该结果表明:酯的水解为酰氧断键。 手性醇的构型是否转变的实验结果: 如果烷氧断键的话,手性碳应为碳正离子,进而发生消旋化, 而实验结果是:手性醇的旋光纯度与酯的旋光纯度基本相等, 所以,其水解为酰氧断键。
同位素追踪结果: 证明:酰氧断键; 加成消去历程。
2 酯的酸性水解 机理: 如何证明这一机理?
测定未反应酯中同位素丰度减少,证明了经历了四面体构型。测定未反应酯中同位素丰度减少,证明了经历了四面体构型。
3 酯的热解(裂) 讨论:ⅰ机理: 六元环过渡态—顺式消去 ⅱ 在过渡态中,为重叠式构像,据此可推知烯烃的构型;
例: 较稳定 的构象 主要产物
ⅲ当α-c两侧都有β-H时,以空阻小,酸性大的β-H被消除为主要产物.ⅲ当α-c两侧都有β-H时,以空阻小,酸性大的β-H被消除为主要产物. ⅳ 荒原酸酯的消去也是顺式消去。 荒原酸酯
黄(荒)原酸 烷基黄原酸甲酯 烷基黄原酸钠 黄原酸 制备: CH3I ROH + CS2 + NaOH
§14.5乙酰乙酸乙酯和丙二酸二乙酯 在有机合成上的应用 一、乙酰乙酸乙酯 (一)制备 讨论:ⅰ 克莱森(Claisen condensation) 缩合:具有-活泼氢的酯,在碱的作用下,两分子酯相互作用,生成β-羰基酯,同时失去一分子醇的反应,分子内的相应反应称迪克曼Dieckman缩合。
(二)性质 1.互变异构现象
(1)生成的烯醇式稳定的原因 1°形成共轭体系,降低了体系的内能。 2°烯醇结构可形成分子内氢键(形成较稳定的六元环体系) (2)其他含活泼亚甲基化合物的互变异构体中烯醇式的含量。 2.亚甲基活泼氢的性质 (1)酸性 乙酰乙酸乙酯的α-C原子上由于受到两个吸电子基(羰基和酯基) 的作用,α-H很活泼,具有一定的酸性,易与金属钠、乙醇钠作用 形成钠盐。
(2)钠盐的烷基化和酰基化 活泼亚甲基的烷基化(α-烷基化): 讨论:① R最好用1°,2°产量低,不能用3°和乙烯式卤代烃。 ② 二次引入时,第二次引入的R′要比R活泼。 ③ RX也可是卤代酸酯和卤代酮或环氧乙烷。 ④ 用于酮、1,3-; 1,4-; 1,5-二氧化碳架的建造。
3.酮式分解和酸式分解 酮式分解乙酰乙酸乙酯及其取代衍生物与稀碱作用,水解生成 β-羰基酸,受热后脱羧生成甲基酮。故称为酮式分解。 酸式分解乙酰乙酸乙酯及其取代衍生物在浓碱作用下,主要发 生乙酰基的断裂,生成乙酸或取代乙酸,故称为酸式分解。
酮式分解 来源于丙酮的骨架乙酰乙酸乙酯
(三)乙酰乙酸乙酯在有机合成上的应用 用于酮;β-酮酸; 1,3-; 1,4-; 1,5-二氧化碳架; 环状碳骨架的建造。 例1: 以乙酸乙酯为原料合成4-苯基-2-丁酮 【拟合成分析】
合成: 例2: 选用不超过4个碳的合适原料制备 卤代烃应该是:1,4-二溴代丁烷
练习:如何利用乙酰乙酸乙酯合成下列化合物。练习:如何利用乙酰乙酸乙酯合成下列化合物。