第八章 醛、酮、醌
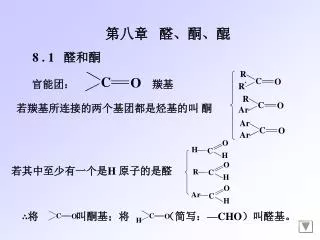
官能团: 羰基. ∴ 将 叫酮基;将 (简写: —CHO )叫醛基。. 第八章 醛、酮、醌. 若羰基所连接的两个基团都是烃基的叫 酮. 8 . 1 醛和酮. 若其中至少有一个是 H 原子的是醛. 8.1.1 分类与命名. 分类 : 根据羰基所连烃基类别分为:. 饱和醛、酮(特别:脂肪族甲基酮) 即:. 脂肪族醛、酮. 醛 酮. 不饱和醛、酮 ( 特别 : α,β 不饱和醛 酮 ) 例: CH 2 =CH—CHO. 芳香族醛、酮.

第八章 醛、酮、醌
E N D
Presentation Transcript
官能团: 羰基 ∴将 叫酮基;将 (简写:—CHO)叫醛基。 第八章 醛、酮、醌 若羰基所连接的两个基团都是烃基的叫 酮 8 . 1 醛和酮 若其中至少有一个是H 原子的是醛
8.1.1 分类与命名 分类:根据羰基所连烃基类别分为: 饱和醛、酮(特别:脂肪族甲基酮) 即: 脂肪族醛、酮 醛 酮 不饱和醛、酮 (特别:α,β不饱和醛 酮) 例:CH2=CH—CHO 芳香族醛、酮 脂环酮(羰基在C 环上)例:
脂肪(链)族醛、酮 系统命名: 例: 主链—选含羰基在内的最长碳链。按C数多少称某醛或酮 。 编号—从醛基所在一端或靠近酮基的一端开始。 支链— 写在前面,酮名称中注明羰基的位置。 4-甲基-2-己烯醛 ( 、不饱和醛) 丁醛 2-甲基丁醛 2-丁酮 4-甲基-3-戊烯-2-酮 ( 、不饱和酮) 4-乙基-2-己酮
芳香族醛、酮的命名,将芳环当作取代基。 苯(基)乙醛 3-苯(基)丙醛 苯乙酮 1-苯基-1-丙酮 二苯甲酮
脂肪族 环 酮的命名 羰基在环内,称为环某酮; 在环外,则将环当作取代基。 环己酮 4-甲基环己酮 例: 1-环己基-2-丙酮 3,3-二甲基环己基甲醛 3 -甲基- 4-(5‘-甲基 - 3’-环己烯基)-2-丁酮
含多个羰基时, 称作二、三、四…酮, 并在名称前注明羰基位置。 例: 2,4-戊二酮 5-丙基-5-己烯-2,4-二酮
8.1.2 物理性质 + - 羰基的结构特点: 8.1.3 化学性质 由于电子效应的影响,使醛、酮在以下几个部位发生化学反应。 ①羰基C原子为官能团中缺电子的部位,∴羰基易接受亲核试剂的进攻而发生亲核加成反应。 - + ②受羰基吸电 子诱导效应影响,使碳上的C-H键易断裂,发生—H的反应。 ③醛的反应 (被氧化剂 氧化、 还原剂还原)。
1、羰基上的亲核加成反应: 定速步骤。影响反应快慢主要因素: ①羰基C 上正电荷密度。正电荷密度越高,反应越易进行。 ②空间位阻的大小。R体积越大,反应越慢。
⑴ 与HCN的加成: 醛、酮与HCN加成,生成 -羟基腈,反应是可逆的。产物进一步水解,可得到比反应物多一个C 原子的-羟基酸。即: 醛、酮反应范围:醛、脂肪族甲基酮、8个碳以下的环酮。 活性:
例如:工业上制造有机玻璃,就是该反应应用。例如:工业上制造有机玻璃,就是该反应应用。 ①甲醛 ②丙酮 ③二苯酮 ④乙醛 ⑤苯乙酮 ⑥苯甲醛 丙酮氰醇 聚甲基丙烯酸甲酯 -甲基丙烯酸甲酯 亲核加成 聚合反应 共热:①脱水 ②水解 ③酯化 练习:写出下列化合物与HCN进行加成反应的难易顺序。 答案:③﹤ ⑤﹤ ② ﹤⑥﹤ ④﹤ ①
⑵ 与NaHSO3加成 (反应范围、活性与 ⑴ 相同) 醛或酮与过量饱和(40%)的NaHSO3 水溶液一起摇动,有白色晶体 -羟基磺酸钠 析出。 机理: 该反应是可逆的,产物溶于水而不溶于NaHSO3饱和溶液,有晶体析出, ∴可用来鉴定、鉴别、分离、提纯 醛、酮类化合物。
⑶ 与格利雅(Grignard)试剂的加成 格氏试剂是含C 的亲核试剂,醛、酮与之加成,其产物经水解,可得到 醇。
⑷ 与醇的加成 几点说明: • 半缩醛(酮) 无论 碱性或酸性介质中均不稳定。 • 缩醛(酮) 碱性介质中稳定,酸性介质中不稳定。 • 缩醛较易形成,缩酮较难。 • 用乙二醇形成环状缩酮 ,可提高缩酮产率。
例如:从3—溴丙醛合成丙烯醛。 ◆ 利用缩醛易被稀酸水解成原来的醛和醇的性质,在有机合成中可以用来保护醛基。 不能采用碱脱HBr的方法,因为稀丙醛在碱性条件下聚合。
再如:4 -己烯醛需还原碳-碳双键,而不还原羰基。 ⑸ 与氨的衍生物 加成 氨的衍生物,如:羟氨、肼、苯肼、2,4-二硝基苯肼、氨基脲等,这些分子中均有含孤电子对的 N,可作为亲核试剂与羰基发生“加成-消除”反应。生成具有—C=N—结构的产物。 例如:
以上试剂 叫 羰基试剂 这些产物均为晶体,具有一定 的熔点,常用于鉴别醛、酮 。 其中,与2,4 -二硝基苯肼反应 生成黄色沉淀,常用于羰基化 合物的定性鉴定。 ↓黄色
⑹ 与水的加成 当羰基C 上正电荷较高时,生成物含量才较高。如: 归纳:羰基上亲核加成反应,亲核试剂提供一对电子的与羰基 C 原子成键(定速步骤),试剂中其余部分与 O 成键。
2、 -H的反应 —H 表现出很强的活性。∵ ① 诱导效应 ② P- 共轭 ∴该离子稳定。
⑴ 羟醛缩合反应 在稀碱作用下,含-H 的醛可发生缩合反应。(酮也有此反应,但由于诱导效应和空间位阻,使产物的量很少,∴讨论没必要。) ∵产物中既有羟基,又有醛基,∴称为羟醛缩合反应。 思考:下面反应有几种产物。
★虽然不含-H 的醛不发生同分子间的羟醛缩合,但它们的羰基可与另外含-H 的醛发生羟醛缩合。 例如: 3-苯基-3-羟基丙醛 肉桂醛 注意:羟醛缩合反应是增长C 链的一种重要方法,在有机合 成中应用很广。 练习:
⑵ 卤代反应 卤仿反应:在碱溶液中, -碳为甲基,则三个H 都被卤素取代,生成的产物,很容易被碱进一步分解。(由于3个卤素的诱导作用) 醛、酮中的-H 容易被卤素取代,生成-H卤代醛、酮。 卤仿 NaOX 产物之一为卤仿,∴称为 卤仿反应。
注意: 不与NaIO作用,∵属于叔醇。 碘仿反应:若用次碘酸钠(I2+NaOH)溶液作反应试剂,则产物中有特殊气味的黄色固体 碘仿—CHI3,现象明显。 将此反应称为 碘仿反应。 ∴实验室常用碘仿反应鉴别具有: 例如:
3、 还原反应 ⑴ 催化加氢 醛、酮可发生程度不同的还原反应,被还原为醇或亚甲基。 • 催化氢化可还原羰基,同时也还原分子中的碳碳双、叁键。 例如: 巴豆醛(2-丁烯醛)
⑵ 被NaBH4 和 LiAlH4还原 硼氢化钠(NaBH4 ) :是缓和还原剂,只还原羰基; 四氢铝锂(LiAlH4 ) :很强还原剂,还原羰基、羧基及其衍生物、卤代烃、腈类。 但它们都不还原碳碳双键、叁键。 例如:
⑶ 克莱门森(Clemensen)还原法 醛、酮与锌/汞齐和浓HCl 一起加热,羰基还原成亚甲基。 ? 思考:
⑷ 沃尔夫—基希纳(Woif-kishner)—黄鸣龙还原法 将羰基还原为亚甲基。该法是先使醛、酮与肼反应生成腙,然后将腙分解成产物。 4、氧化反应 醛、酮主要区别是对氧化剂的敏感性。醛很容易被氧化为相应的羧酸;酮则不易被氧化。所以选择一较弱的氧化剂来区别醛和酮。
常用的较弱氧化剂是: 托伦(Tollen)试剂:AgNO3的氨溶液 斐林(Fehling)试剂:CuSO4 + NaOH + 酒石酸钾钠 本尼迪(Benedict)试剂:CuSO4 + Na2CO3 + 柠檬酸钠 注意:上述试剂只能将醛氧化为酸,不能氧化碳碳双、叁键和醇,它们起作用的分别是:Ag+、Cu2+。 例:在碱性条件下:
注意: 托伦试剂氧化: 脂肪醛 甲醛 芳香醛 斐林试剂氧化: 脂肪醛 甲醛 × 本尼地试剂氧化: 脂肪醛 × × 利用这些差异可区分各类醛。 5、歧化 反应 不含-H 的醛,如:HCHO、R3C-CHO、C6H5CHO等,在浓碱下,发生自身氧化还原反应。例: 注意:当 甲醛 + 不含-H 的其它醛,甲醛总被氧化为甲酸,而另一醛则被还原为醇。
答案: 练习: 某醇分子式为C5H12O,试推断满足下列条件的结构式。 a .它的氧化产物不发生碘仿反应,也不与斐林试剂反应; b .它被氧化后能与 2,4 -二硝基苯肼和 NaOI 反应。
练习: • 分子式为C7H12O的酮 (A),与甲基溴化镁反应,生成分子式为C8H16O的醇 (B),(B)脱水生成分子式为C8H14的两种烯烃 (C)和 (D)。(C) 经臭氧化再还原水解可得 (A),(D)经臭氧化还原再水解得 (E),分子式为C8H14O2,(E)能被费林试剂氧化为 (F),分子式为C8H14O3,用溴的NaOH溶液处理(F),生成3 -甲基己二酸。试写出 (A)、(B)、(C)、(D)、(E)、(F)的结构式及简要推导过程。
8.1.4 醛、酮的代表化合物 1、甲醛 2、丙酮 3、苯甲醛 4、三氯乙醛
结构特征:分子中具有 或 结构的物质叫 醌。 8.2 醌 8.2.1 醌的结构与命名 命名: 邻苯醌(1,2-苯醌) 2,5-二甲基-1,4苯醌 对苯醌(1,4-苯醌) -萘醌(1,4 -萘醌) -萘醌(1,2-萘醌) 蒽醌(9,10-蒽醌)
8.2.2 醌的性质 物理性质:结晶固体,有颜色。为黄色(对苯醌)、 红色(邻苯醌)。 化学性质:从结构上看,苯醌分子中既有羰基,又有碳 碳双键,且羰基和碳碳双键之间形成共轭体 系。∴醌具有:羰基的性质(亲核加成)、 C=C的性质(亲电加成)、羰基与双键共同 参与性质(1,4-加成)。 1、羰基加成 对苯醌二肟 对苯醌一肟
2、双键加成 四溴化醌 二溴化醌 3、 1,4 加成 2-氯-1,4 -苯二酚 4、还原反应
将对苯醌和对苯二酚的溶液混合,混合液呈暗棕色,并析出暗绿色晶体。这种晶体叫 醌氢醌。 8.2.3 醌的衍生物 1、自然界分布较广的醌类是天然色素。 2、维生素K:有K1 、K2、K3三种。 3、辅酶Q 。 总结本章: