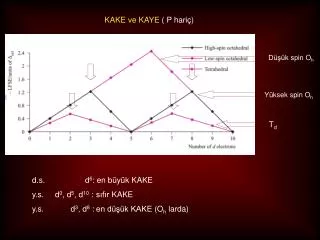
KAK E ve KAYE ( P hariç )
380 likes | 998 Views
Düşük spin O h. Yüksek spin O h. T d. KAK E ve KAYE ( P hariç ). d. s . d 6 : en büyük KAK E y.s. d 0 , d 5 , d 10 : sıfır KAKE y. s . d 3 , d 8 : en düşük KAK E (O h larda). M n+ (g) + n X - (g) MX n(s). KAT açıkladığı kavramlar.

KAK E ve KAYE ( P hariç )
E N D
Presentation Transcript
Düşük spin Oh Yüksek spin Oh Td KAKE ve KAYE ( P hariç) d.s.d6: en büyükKAKE y.s. d0, d5, d10 : sıfırKAKE y.s.d3, d8 : en düşük KAKE (Oh larda)
Mn+(g) + n X-(g) MXn(s) KAT açıkladığı kavramlar 1. Örgü Enerjisi ( Born Haber çevriminden) MCl2 ( 1. periyot için) : y.s, Oh MCl2 Ca(II) Ti(II) V(II) Cr(II)….etc Örgü Enerjisi:Gaz halindeki anyon ve katyonlardan kristal oluşumu sırasında açığa çıkan enerjidir. Örgü enerjisindeki düzensizliklerKAKE den kaynaklanır.
2. Hidrasyon Entalpisi değişimi Hhid z/r M2+ M3+ M+2hidrasyon entalpisi : M2+(g) + 6 H2O [M(OH2)6]2+(aq)
Ca2+ Zn2+ Sc3+ Ga3+ 3. İyon Yarıçapı Değişimi high spin low spin high spin low spin düşük spin: t2g6kadar yavaşça azalır, t2g6 eg1 den sonra artar yüksek spin: t2g3kadar yavaşça azalır, t2g3 eg1den sonra artar
4. İyonlaşma Enerjisi, birinci periyotgeçiş metal iyonları, yüksek spin, Oh 3rd I.E. 2nd I.E. 1st I.E. d6ve d5de azalma
[M(H2O)6]2+ + [EDTA]4- [M(EDTA)]2- +6H2O En fazlaKAKE İlave kararlılık Jahn-Teller etkisinden kaynaklanır Irving-Williams serisi Denge durumu KAKE nin farkına dayanır d5 d6 d7 d8 d9 d10 Mn2+ < Fe2+ < Co2+ < Ni2+ < Cu2+ > Zn2+ I1 ve I2 toplamları
5. dnfonksiyonu olarak Eodeğişimi [Co(en)3]+3 + e→ [Co(en)3]+2 E = - 0.26 eV Aşağıdaki elektrot potansiyellerindeki değişimi KAKE kavramı ile açıklayınız. [Co(H2O)6]+3 + è→ [Co(H2O)6]+2 E = 1.84 eV - 0.4 Δo - 0.8 Δo [Co(NH3)6]-3 + è → [Co(NH3)6]-4 E = 0.10 eV -2.4Δo -1.8Δo
Elektronların orbitaldeki hareketi Elektronların spini (etkisi çok önemlidir) • Soru: Manyetik alanın kaynağı nedir? • Cevap:Hareket halindeki elektrik yükü • Örneğin bir sindiri çevreleyenteldeki akım mıknatısa benzer bir alan oluşturur.
paramanyetizma ferromanyetizma antiferromanyetizma ferrimanyetizma
Manyetik maddeler Maddeler uygulanan manyetik alana karşı davanışlarına göre sınıflandırılabilir Diyamanyetik maddeler, Bi, Hg, Ag, Pb, elmas, NaCl, Cu, H2O, N2 (g) Manyetik momente sahip değildirler,manyetik alan tarafından itilirler. Paramanyetik maddeler, Al, Pt, U, Na, O2 (g) Manyetik momente sahiptirler, alan tarafından zayıfça çekilirler. Eşleşmemiş elektronlara sahiptirler. Alan kalktığında manyetizmaları yok olur. Ferromanyetik maddeler, Fe, Ni, Co , çelik Manyetik momente sahiptirler, alan tarafından kuvvetle çekilirler. Curie noktası altında kalıcı manyetik özelliğe sahiptirler, yani, uygulanan manyetik alan kalktığında manyetik özelliklerini korurlar. Antiferromanyetik maddeler Net manyetik momentleri sıfırdır. Ferrimanyetik maddeler, magnetit (Fe3O4) Net manyetik momentleri sıfır değildir.
Manyetik moment Her bir elektron manyetik momente sahiptir spin açısal momentum orbital açısal momentum Kompleksin manyetik momenti =meff
mS = n (n + 2) Spin manyetik moment, mS " meffde spin orbital katkısı orbital açısal momentum katkısına göre daha baskındır " n = eşleşmemiş elektron sayısı mS = 2 S (S + 1) S = toplam spin kuantum sayısı = n / 2
mS = n (n + 2) eg x2-y2 z2 t2g yz xz xy n = 3 mS = 3 (3 + 2) = 3.87 BM t2 yz xz xy e x2-y2 z2 n = 2 mS = 2 (2 + 2) = 2.83 BM x2-y2 xy z2 n = 0 mS = 0 (0 + 2) = 0 BM yz xz Spin manyetik moment, mS n = eşleşmemiş elektron sayısı Aşağıdakilerin spin manyetik momentlerinedir …..? [Co(OH2)6]2+ Ohy.s. d7 3 u.p.e- [NiCl4]2- Td d8 2 e.e [Ni(CN)4]2-kare düzlem d8
μeff : Etkin manyetik moment m :Molar manyetik duyarlık (denel yöntemlerle tayin edilir) meff = 2.83 m T BM sıcaklık jiromanyetik oran meffbirimi : Bohr Magneton (B.M.)
Manyetik duyarlık tayiniGouy Terazisi Diyamanyetikmaddeler manyetik alan tarafından itilir. Paramanyetik maddeler manyetik alan tarafından çekilir.
M : magnetic polarization of the matter H:magnetic field Χ : magnetic susceptibility (proportionality constant )
Paramanyetik maddelerde, sıcaklık arttıkça χdeğeri değişmez veya azalır. Ferromanyetik ve antiferromanyetik maddeler ısıtıldıklarında manyetik özelliklerini kaybederek paramanyetik maddelere dönüşürler. Curie sıcaklığı (Tc) : Ferromanyetizma paramanyetizma Néel sıcaklığı (TN) Ferromanyetizma paramanyetizma Lantanitler, sıcaklık azaldıkça, paramanyetikten antiferromanyetiğe sonra ferromanyetiğe geçer.
Geçiş metalleri genellikle renkli bileşikler oluştururlar renk şunlara bağlıdır….geçiş metal cinsi metalin yükseltgenme sayısı ligant cinsi kompleksin koordinasyon sayısı d10 (dolu) Cu+,Ag+ Zn2+renksizdir d0 (boş) Sc3+, Ti4+ (TiO2, beyaz) yük aktarım geçişleri yoksa d0 (boş) MnO4- (koyu mor) Yük aktarım geçişi var
Geçiş Metal Kompleksleri eg eg [Ti(OH2)6]3+ hn Do t2g t2g Soğurma spektrumu: lmax = 510 nm 490-580 nm beyazışık 400-800 nm Mavi: 400-490 nm Sarı-yeşil: 490-580 nm Kırmızı: 580-800 nm
bakır(II)sülfat çözeltisi Mavi ve yeşilsoğurulmaz Beyaz ışık
Bakır(II) sülfat çözeltisi mavi renklidir, çünkü Kırmızı ve sarı dalgaboyu soğurulur
Nikel(II) sülfat çözeltisi yeşil renklidir, çünkü Mor, mavi ve kırmızı dalga boyları soğurulur
d-d geçişlerinin rengiDbüyüklüğüne bağlıdır eg eg Doct Doct t2g t2g Dküçük düşük enerji kırmızı ışığı soğurur Dbüyük yüksek enerji mavi ışığı soğurur Renk Çemberi Kırmızı ışık soğurulursa kompleks yeşil görünür Mor ışık soğurulursa kompleks sarı görünür dalgaboyu, l (nm)
Dbüyüklüğünün renk üzerine etkisi 1. Belli bir ligant için, renk metal iyonun değerliğine bağlıdır [V(H2O)6]3+ V(III) = d2 iyonu [V(H2O)6]2+ V(II) = d3 iyonu Mor ışık soğurulursa Kompleks sarı görülür Sarı ışık soğurulursa Kompleks mor görülür eg eg Doct Doct t2g t2g Dbüyük Dküçük
Δbüyüklüğünün renk üzerine etkisi 2. Belli bir metal iyonu için, renk ligant türüne bağlıdır [Cr(NH3)6]3+ [Cr(NH3)5Cl]2+ 2+ 3+
Renk ve spektrokimyasal seriler ZayıfAlan Ligandı Yüksek Spin Kompleksi KuvvetliAlan Ligandı Düşük Spin Kompleksi I- < Br- < S2- < SCN- < Cl-< NO3- < F- < OH- < H2O < NCS- < CH3CN < NH3 < en < bpy < phen < NO2- < phosph < CN- < CO küçükD büyükD Kompleks kuvvetli alan ligandına sahipse = büyük delta Işık düşük dalgaboyunda soğurulur = yüksek enerji
Seçim Kuraları Renk şiddeti seçim kurallarına bağlıdır Seçim kurallarına uyan geçişler serbestgeçişler Seçim kurallarına uymayan geçişler yasakgeçişler Laporte SeçimKuralları Spin Seçim Kuralları
Laporte SeçimKuralları Parite de bir değişim olmalıdır s-orbital gerade d-orbital gerade p-orbital ungerade Laporte seçim kuralına göre serbest Laporte seçim kuralına göre yasak p-orbital d-orbital d-orbital d-orbital
Laporte Seçim kurallarına göre d-orbitalleri (g) arasındaki geçişler yasaktır. Sekizyüzlükompleksler Simetri merkezi vardır : t2gve eg orbitalleri Laporte seçim kuralına göre d-d geçişleri yasaktır Molekül titreşimleri seçim kurallarını geçersiz kılar Dörtyüzlü kompleksler Simetri merkezi yoktur : t2ve e orbitalleri Laporte seçim kuralı uygulanmaz Dörtyüzlükompleksler benzei sekizyüzlü komplekslerden daha koyu renklidir
The Spin Seçim Kuralı Spinde bir değişim olmamalıdır serbest yasak