Diels-Alder Reaction
190 likes | 608 Views
Diels-Alder Reaction. 노윤영 이도형 이윤형 이하나. 실 험 목 적. 고리첨가반응 (cycloaddition reaction) 을 통한 six-membered rings 의 구성을 밝혀낸다. Reagents. 3-sulfolene 분자식 C 4 H 6 0 2 S 분자량 118.15 녹는점 65-66℃ 끓는점 끓이면 분해됨 비 중 1.31-1.32 용해도 양 호. Reagents. Maleic anhydride 분자식 C 4 H 2 0 3

Diels-Alder Reaction
E N D
Presentation Transcript
Diels-Alder Reaction 노윤영 이도형 이윤형 이하나
실 험 목 적 • 고리첨가반응(cycloaddition reaction)을 통한 six-membered rings의 구성을 밝혀낸다.
Reagents • 3-sulfolene 분자식 C4H602S 분자량 118.15 녹는점 65-66℃ 끓는점 끓이면 분해됨 비 중 1.31-1.32 용해도 양 호
Reagents • Maleic anhydride 분자식 C4H203 분자량 98.06 녹는점 51-53℃ 끓는점 202 (분해) 비 중 1.218 용해도 가수분해됨
Reagents • O-xylene 분자식 C8H10 분자량 106.17 녹는점 -25℃ 끓는점 144℃ 비 중 0.88 용해도 없음
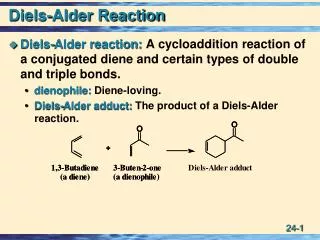
Theory (이론) Diels-Alder reaction의 핵심은 Diene ( conjugated 상태 ) 과 double bond 나 triple bond 을 가진 dienophile이 만나서 cyclohexene이 만들어 지는 것입니다. 이 반응의 경우 워낙 잘 가기 때문에 위에처럼 heating 을 해주지 않아도 RT에서도 높은 수득률을 보여줍니다.
Theory (이론) • 반응 메카니즘은 바로 위에 처럼 간단하게 표현할 수 있습니다. diene 이 전자를 제공하고 있으므로 diene에는 EDG(electron donating group)이 치환되어 있으면 훨씬 반응이 잘 진행될 수 있습니다. 이것은 다시 dienophile의 경우 반대로 전자를 끌어당길 수 있는 EWG이 치환되어 있으면 반응이 잘 갔다는 것을 의미합니다.
Theory (이론) Dienes Dienophiles
Theory (이론) • 여기서 핵심은 endo- 와 exo- 개념이 나왔다는 것인데 위에 그림에서 처럼 dienophile 이 diene 의 ring 아래로 접근해서 형성되는 것을 ( diene under the ring ) 해서 endo라고 합니다 ---> 꼭 기억합시다. • 그에 반해서 diene 이 ring 밖으로 exposed된 상태를 exo-라고 합니다.
Procedure (실험과정) • 1. 2.5g의 3-sulfolene, 1.5g의 maleic anhydride, 1ml의 xylene을 stirring bar와 함께 50ml 플라스크에 넣는다.
Procedure (실험과정) • 2. 1의 혼합물을 안에 있는 고체가 전부 녹을 때까지 stirring하면서 가열한다. 이 때 가열은 heating mantle과 slidacs를 이용한다.
Procedure (실험과정) • 3. 혼합물을 30분동안 reflux 상태에서 가열한다.
Procedure (실험과정) • 4. reflux가 끝난 혼합물을 끓는점 이하로 식혀준 후 10ml의 xylene을 다시 넣고, 다시 모든 고체가 녹을 때까지 가열한다.
Procedure (실험과정) • 5. 4에서 가열한 혼합물을 Erlenmeyer flask에 넣는다. 이 때 혼합물에서 결정이 생긴다면 다시 결정이 녹을 때까지 천천히 가열한다.
Procedure (실험과정) • 6. 혼합물이 흐리게 될 때까지 petroleum ether를 넣는다
Procedure (실험과정) • 7. 나온 결정을 감압여과하여 거르고 오븐에 넣어 말린다.
주 의 사 항 • - 슬라이닥스의 전압은 대략 50V 정도로 한다. • - 2번 과정에서 reflux를 할 때 heating mantle에서 열이 덜 빠져나가게끔 sea sand를 채운다. 열이 빠져나가면 가열하는 시간이 오래 걸리고, 종이 등을 태우면 mantle의 열에 의해 종이가 탈 수 있다. • - 3번 과정에서 혼합물을 reflux conderser에 넣고 가열하면 처음에는 기체가 생성된다. 이 때는 아직 reflux가 이루어진 것이 아니므로 이 기체가 없어지고 액체가 맺히면 그 때부터 reflux가 된 것으로 보고 30분을 측정한다. • - 혼합물을 두 번째 가열할 때 원래는 혼합물이 투명해야 하지만 약간의 불순물이 들어갈 수 있기 때문에 황색을 띌 수도 있다. • - reflux를 위해서는 상당히 높은 온도가 필요하므로 용액 등을 옮길 때 화상에 주의한다.
DATA / RESULT • 3-sulfolene 의 몰수는 2.5/118.15=0.0212몰 sulfolene 1몰을 가열하면 1몰의 butadiene이 얻어지므로1,3-butadinen 몰수 = 0.0212몰 • Maleic anhydride 1.5/98.06=0.01530몰 - 제한 시약 • butadiene과 Maleic anhydride가 1:1로 반응하므로 product의 몰수는 0.01530몰 • 0.01530*152.15=2.328그램이 생성되어야 함. • 수득률 : 1.61/2.328*100=69%