2.4 第四节 液体及玻璃(非晶态)的粘 滞 流 动
2.4 第四节 液体及玻璃(非晶态)的粘 滞 流 动. 晶体中塑性流动强烈地决定于结晶学,即具有一定的滑移系统,与此相比较,液体和玻璃的粘滞形变完全是各向同性的,只决定于作用应力。. F. v 2. A. x. v 1. 流动度 ------ 粘度的倒数 1/ 。 粘度在宽广范围内变动。 例如: 室温下,水和液态金属粘度为 0.01 泊数量级。 液线温度下钠钙硅酸盐玻璃,其值约 1000 泊; 在退火范围的玻璃约为 10 14 泊。. 2.4.1 流动模型. 1. 绝对速率理论. 绝对速率模型:

2.4 第四节 液体及玻璃(非晶态)的粘 滞 流 动
E N D
Presentation Transcript
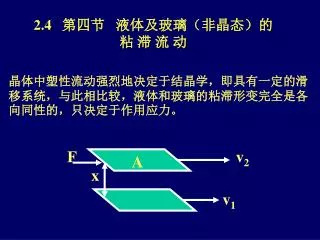
2.4 第四节 液体及玻璃(非晶态)的粘 滞 流 动 晶体中塑性流动强烈地决定于结晶学,即具有一定的滑移系统,与此相比较,液体和玻璃的粘滞形变完全是各向同性的,只决定于作用应力。 F v2 A x v1
流动度------粘度的倒数1/。 粘度在宽广范围内变动。 例如: 室温下,水和液态金属粘度为0.01泊数量级。 液线温度下钠钙硅酸盐玻璃,其值约1000泊; 在退火范围的玻璃约为1014泊。
2.4.1 流动模型 1. 绝对速率理论 绝对速率模型: 把粘滞流动看成是受高能量过渡状态控制的一种速率过程。 绝对速率理论的含义: 液体分子从开始的平衡位置过渡到另一平衡状态。 越过能垒进行传输,该能垒受到作用应力的影响发生偏移。
3 势 能 流动方向 2 E E E 1 /2 液体流动模型与势能曲线 根据绝对速度理论,流动速度为: u=2 0exp(-E/kT)sin( 1 2 3/2kT) 根据牛顿液体定律:= dv/dx= u/ 1
得:=1/u=1/[20exp(-E/kT)sin(1 23/2kT)] 假定: =1 = 2 = 3 则: == exp(E/kT) /[2 0 sin( V0/2kT)] 当外应力很小,气体分子体积很小, V0kT 得: = kT/ 0V0 exp(E/kT)= 0 exp(E/kT) 说明:在外应力很小时,粘度与应力无关,应力较大时,粘度随温度提高而剧烈的下降。
2. 自由体积理论 表达式:=Bexp(KV0/Vf) 其中: Vf=V-V0 Vf------自由体积,由于提高了容许分子运动的空隙, 其值越大粘度越小; V------给定温度下分子的体积,温度越高,其值越大。所以温度升高,自由体积增大,粘度降低; V0 ------分子有效的硬核体积,其值恒定不变。 3. 过剩熵理论 温度下降,液体的熵降低,使形变增加困难。 表达式: =Cexp(D/TS0)
2.4.2 影响粘度的因素 1 . 温度 不同种类的材料,粘度对温度的依赖关系有很大差别。 玻璃粘度随温度变化的特点: 在玻璃转变温度,相当于粘度等于1013泊所对应的温度,玻璃的折射率、比热、热膨胀系数、粘度等物理性质发生突变,在性质与温度曲线上表现为斜率突然改变。
退火点(消除内应力温度):=10 12..5-10 13.5泊 软化点:=10 7.6 泊 工作范围(成型温度):=104-108 泊 粘 度 熔化范围:=50-500泊 钠钙硅系统玻璃温度和粘度的关系曲线 温度
2. 时间 在玻璃转变温度, 玻璃的粘度与时间有关。 lg 在退火点487.70C以下保温一段时间,粘度随时间的变化曲线 15.5 15.0 14.5 14.0 从高温状态冷却到退火点时粘度随时间的变化曲线 0 1000 2000 min
3. 熔体结构、组成 玻璃的粘度与熔体结构密切相关,而熔体结构又决定于玻璃的化学组成和温度,其结构主要由氧硅比决定。 玻璃的粘度几乎总是随网络改变阳离子浓度的增加而下降。 例如:在16000C,熔融石英的粘度因掺2.5mol%K2O,粘度下降约四个数量级。 原因:改性离子减弱了Si—O键。
(1)化学键的强度 在碱硅二元玻璃中,当硅氧O/Si比值很高,已接近岛状结构,其间很大程度上依靠R—O相连接,粘度按Li2O—Na2O—K2O顺序递减,当比值低时,顺序相反。 (2)离子的极化 阳离子的极化力大,对氧离子极化、变形大,减弱硅氧键的作用大,表现为粘度下降。 一般非惰性气体型的氧离子极化力大于惰性气体型的氧离子。 例如:二价铅取代电荷相同、大小相近的二价锶离子,玻璃的粘度下降。过渡金属取代镁,粘度下降。
(3) 结构的对称性 结构不对称,有可能在结构中存在缺陷,粘度下降。 例如:Si—O、 B—O键强相差不大,但石英玻璃的粘度比氧化硼玻璃的粘度大的多。 磷酸盐玻璃中磷氧有单键和双键,即结构不对称性。
(4)配位数N 氧化硼的配位数对粘度的影响比较突出。 16Na2O·xB2O3· (84-x)SiO2玻璃系统粘度随硼含量的变化: 开始加入的硼处于氧四面体,使结构网络聚集紧密,粘度提高,当含量增加到一定值时,硼处于三角体中,使结构疏松,粘度下降。 In2O3(N=6)>Al2O3(N=4) ZrO2(N=8) > TiO2(N=6) > GeO2(N=4)
氧化物对玻璃粘度的影响总结 1. SiO2、Al2O3、 ZrO2 等提高粘度。 2. 碱金属氧化物降低粘度。 3. 碱土金属氧化物对粘度的作用较复杂。一方面类似于碱金属氧化物,能使大型的四面体群解聚,减小粘度,表现在高温。另一方面,其电价较高,离子半径不大,故键力较大,有可能夺取小型四面体群的氧离子,使粘度增大,表现在低温; 4. PbO、 CdO、 Bi2O3、 SnO等降低粘度。 5. Li2O 、ZnO、 B2O3等增加低温粘度,降低高温粘度。