为什么化学反应通常不能进行到底?
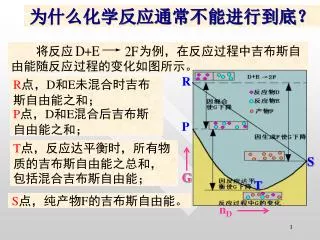
将反应 为例,在反应过程中吉布斯自由能随反应过程的变化如图所示。. R. P. S. G. T. n D. 为什么化学反应通常不能进行到底?. R 点, D 和 E 未混合时吉布斯自由能之和;. P 点, D 和 E 混合后吉布斯自由能之和;. T 点,反应达平衡时,所有物质的吉布斯自由能之总和,包括混合吉布斯自由能;. S 点,纯产物 F 的吉布斯自由能。. 第三章 化学平衡. 学习要点: 平衡位置:变化方向的依据,变化限度的量度。 用热力学方法计算平衡位置; 确定影响平衡位置的因素,对实际反应进行指导。.

为什么化学反应通常不能进行到底?
E N D
Presentation Transcript
将反应 为例,在反应过程中吉布斯自由能随反应过程的变化如图所示。将反应 为例,在反应过程中吉布斯自由能随反应过程的变化如图所示。 R P S G T nD 为什么化学反应通常不能进行到底? R点,D和E未混合时吉布斯自由能之和; P点,D和E混合后吉布斯自由能之和; T点,反应达平衡时,所有物质的吉布斯自由能之总和,包括混合吉布斯自由能; S点,纯产物F的吉布斯自由能。
第三章 化学平衡 学习要点: 平衡位置:变化方向的依据,变化限度的量度。 用热力学方法计算平衡位置; 确定影响平衡位置的因素,对实际反应进行指导。
<0, 自发 =0, 平衡 >0, 不能发生 回顾第二章内容: 化学势判据 设各物质的化学势分别为μA,μB,μY,μZ, 则等温等压条件下,反应系统的吉布斯函数变化为:
混合理气中组分B的标准态化学势。 标准态——T , pθ,纯理想气体B 理想气体化学势
液态或固态物质的标准态化学势。 标准态——T, pθ(p)下纯液体(固体), (饱和蒸气压为p*) 定温下:l(T,p*) g (T,p*) 或 s (T,p*) g (T,p*) p*为纯液(固)体在T下的饱和蒸汽压,为T的函数。 纯液体及纯固体化学势
§3.1 理想气体的化学平衡 一、平衡常数的热力学推导——以理想气体反应为例 设在一极大封闭系统中,有amol A物质,bmol B物质, ymolY物质, zmolZ物质,等温等压条件下,存在如下平衡: aA + bB = yY +zZ 设各物质的化学势分别为μA,μB,μY,μZ,则等温等压条件下,反应系统的吉布斯函数变化为: 反应的平衡条件: 再根据:
整理得: 令: 则:
称为热力学平衡常数,它仅是温度的函数。在数值上等于平衡时的“压力商”,是量纲为1的量。因为它与标准化学势有关,所以又称为标准平衡常数。称为热力学平衡常数,它仅是温度的函数。在数值上等于平衡时的“压力商”,是量纲为1的量。因为它与标准化学势有关,所以又称为标准平衡常数。 令
是平衡位置的标志; 是反应程度的量度。 关于Kθ与ΔrGθm的几点说明: Kθ与ΔrGθm的物理概念不同,所指状态不同; Kθ与ΔrGθm中所选物质的标准态必须一致; 标准平衡常数Kθ为无量纲量,有别于实验K; 标准平衡常数Kθ
二、其他平衡常数的表示方法( Kx、Kc、Kp) 反应达平衡时,用反应物和生成物的实际压力、摩尔分数或浓度代入计算,得到的平衡常数称为经验平衡常数,一般有单位。 以摩尔分数表示:pB=xBp,代入K的表达式得:
显然: 以物质的量浓度表示:pB=cBRT,代入K的表达式: 以分压表示:
§3.2 复相化学平衡 一、复相化学平衡: 系统在任意T、P下,纯凝聚相的化学势为: 而气相的化学势为:
对于复相反应,平衡常数表达式中只包含了气体的相对分压,即平衡常数只与平衡气相的分压有关。对于复相反应,平衡常数表达式中只包含了气体的相对分压,即平衡常数只与平衡气相的分压有关。 得:
二、分解压 对于如下反应——特殊的复相反应,只有一种气体生成物,其余都是纯凝聚相。 2FeO(s)=2Fe(s) + O2(g), Kp=p(O2) CaCO3(s)=CaO(s) +CO2(g), Kp=p(CO2) 定义:T温度下,若纯凝聚相分解时只产生一种气体。当反应达平衡时,该气体的平衡分压,即为该凝聚相物质的分解压。分解压等于外压时的温度称为分解温度。 Kp只是温度的函数,分解压也只与T 相关,与凝聚态物质的数量无关;
分解压大小反映了分解反应的程度,亦或是凝聚态物质的稳定性。分解压愈大,化合物愈易分解,且随 T 升高,分解压增大。 表3.1 某些氧化物在1000K下的分解压 炼钢中可选择Al、Si、Mn作为脱氧剂
§3.3化学反应等温方程式 一、等温方程的推导 理想气体反应
是温度的函数,一定反应,一定温度下为常数,与系统分压无关; 则与分压有关。 (2) 表征给定系统中所发生等温反应的不可逆程度,我们可以通过选择反应条件(温度、组成、压力),来改变二者相对大小使反应朝我们希望的方向进行。 范特荷夫等温方程
自发 平衡 的讨论 二、等温方程式 方程表明: ⑴ Jθ/ Kθ=1时, ΔrGm=0,反应系统处于平衡态; ⑵ Jθ/ Kθ≠1时, ΔrGm≠ 0,反应系统偏离平衡态; ⑶ 改变系统的 Jθ值,系统偏离平衡态,将引起平衡移动: 当J<Kθ,ΔrGm<0,反应正向自发; 当J>Kθ,ΔrGm>0,反应逆向自发;
由 可知,只要知道了 ,就可以求出 标准摩尔生成吉布斯函数 在指定温度T下,由各自处于标准状态下的指定单质变为处于标准状态下1mol纯物质B的标准吉布斯函数变化。 任一温度下,标准态下的指定单质其 为零。 §3.4 标准平衡常数的热力学计算 一、标准摩尔生成吉布斯函数法
例1:有人认为,汽车排气管中排出的空气污染物质NO可以用莫涅尔monel催化剂(莫涅尔催化剂是一种镍铜合金),使它同也是汽车中排出的CO进行反应来消除例1:有人认为,汽车排气管中排出的空气污染物质NO可以用莫涅尔monel催化剂(莫涅尔催化剂是一种镍铜合金),使它同也是汽车中排出的CO进行反应来消除 NO(g)+CO(g)→CO2(g)+N2(g) 这一反应从热力学上来看是可行的吗?下一反应 CO(g)+H2O(g)→CO2(g)+ H2(g) 会把CO消耗掉,从而使NO得以自由排出,那么,它的干扰是否应该加以考虑呢?
对于反应:NO(g)+CO(g)→CO2(g)+N2(g) 对于反应:CO(g)+H2O(g)→CO2(g)+ H2(g) 可见,两个反应在热力学上都是可行的。
例如,求 的平衡常数 二、标准摩尔熵法 三、组合法 (1) - (2) 得(3)
§3.5标准平衡常数与温度的关系 ——范特荷夫等压方程 由热力学重要关系——G-H方程: (3-21) 一、等压方程的推导 ∴改变温度将引起 Kθ的改变,即平衡位置的改变。 ——化学反应等压方程式(Van’t Hoff等压方程式)。
不论 还是 ,温度越高, 随T的变化越缓慢 二、定性讨论: 所以ΔrHθm的符号将决定 Kθ 随 T 变化的方向。 • ΔrHθm的大小将决定 Kθ随 T 变化的程度, • 即| ΔrHθm|愈大, Kθ受T 的影响愈大。
(3-24) lnKθ I/T 三、定量计算: • 在温度变化范围不大时,设反应焓变为常数。 • 对上式积分:
(3-23) 应用 (a)已知ΔH ,T1 ,K1,T2计算K2 (b) 已知T1 ,K1,T2 ,K2计算ΔH • T变化范围大或需精确计算时,需代入ΔrHθm(T)关系——(Kichoff)定律
若 反应正向进行 (1)对吸热反应 温度升高,则Kθ值增大; 若 反应逆向进行 (2)对放热反应 温度升高,则Kθ值减小; §3-6 各种因素对平衡的影响 一、温度的影响 判断反应进行方向 问题:若二者同号时,如何判断,温度对反应进行方向有何影响?表3-2(自学)
二、浓度的影响 改变反应物或产物的浓度(或分压),则J 值变化,平衡移动。 三、压力的影响
若 p增大时,平衡向正方向移动 <0, 若 p增大时,平衡向逆方向移动 若 , p不影响平衡 >0,
四、惰性气体的影响 1.等温等压下加入或移走惰性气体,组分的分压变化,影响化学平衡。 加入惰性气体,则p减小,即增加惰性组分,相当于减小系统压力的作用. 例: N2+3H2=2NH3 νB<0, 若增加惰性组分,减小压力向体积增大的方向进行,对合成氨不利.
2.等温等容下的化学反应,改变气体的量不会改变分压,不影响化学平衡。2.等温等容下的化学反应,改变气体的量不会改变分压,不影响化学平衡。 等温等容时,改变惰性气体的量不会改变 pi,因此不会使平衡移动。
§3-7 平衡组成的计算 例2 甲烷是钢铁表面进行渗碳处理时最好的渗碳剂之一(氨则是渗氮剂)。其高温反应为: CH4(g)=C(石墨)+2H2(g) ⑴ 求500℃时反应的标准平衡常数; ⑵ 求500℃平衡时CH4的分解百分率。设其总压力为101.325和50.66kPa,且设体系中无局外气体。 ⑶ 500℃,101.325kPa总压下,分解前的甲烷中含有50%惰性气体,求CH4的分解百分率。
比较 解: (1)在500℃时 定性讨论
总压降低,分解百分率增加; 当p=101.325kPa时,得=0.309,当p=50.66kPa时,得=0.417。 即降低总压有利于CH4生成 定性讨论
总压降低,分解百分率增加; P=101.325kPa时, =0.392,即加入惰性气体,CH4分解率增加。 定性讨论 加入惰性气体,分解百分率增加。
M N -5 lg[Cr+3] N’ M’ -7 C 6 8 10 pH 例3 Cr3+在水中存在如下平衡: 问:如何控制水溶液的pH值,方能使排放水中残留的总Cr含量不大于0.5mg/L(环保排放标准)? 解: pH=5.7~9.6:排放标准 pH=5.8~8.6:饮用标准 pH =6.7时: [Cr3+总]≈ 2×10-8mol/L (或1×10-3mg/L) 为最佳排放条件。
自学: §3-8 总结: 1、平衡位置:变化方向的依据,变化限度的量度。 2、用热力学方法计算平衡位置; 3、确定影响平衡位置的因素,对实际反应进行指导。 本章习题:P102~103, 3-1、3-2、3-6
1.有理想气体反应:A(g)+2B(g)=C(g)达到平衡。当温度不变时,增大压力则反应平衡常数Kθ()(填增大、减小或不变),平衡将( )移动(填向左、向右或不) 2. 从范特荷夫方程可看出,对于放热反应,升高温度,平衡常数Kθ( ) (填增大、减小或不变),平衡向( )方向移动。(填反应物或产物) 3.已知2NO(g)+O2(g)=2NO2(g)为放热反应。反应达到平衡后,欲使平衡向右移动,应采取的措施是( ) A.降温和减压 B.降温和增压 C.升温和减压 D.升温和增压
4.理想气体化学反应平衡时( νB ≠0),加入惰性气体,平衡不发生移动的条件是( ) A. 恒温恒压 B. 恒温恒容 C. 任意 D. 绝热恒压 5.在恒温恒压不做非体积功的情况下,下列哪一个过程肯定可以自发进行 ( ) (A) ΔH>0,且ΔS>0 (B) ΔH<0,且ΔS>0 (C) ΔH>0,且ΔS<0 (D) ΔH<0,且ΔS<0
3-6. 将含水蒸气和氢气的体积分数分别为0.97和0.03的气体混合物加热到1000K,这个平衡气体混合物能否与镍反应生成氧化物?已知, 解:(1)-(2)=(3) (3)