情景六 粗铅精炼
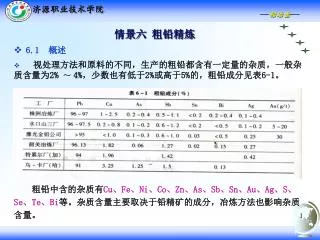
情景六 粗铅精炼. 6.1 概述 视处理方法和原料的不同,生产的粗铅都含有一定量的杂质,一般杂质含量为 2% ~ 4% ,少数也有低于 2% 或高于 5% 的,粗铅成分见表 6-1 。. 粗铅中含的杂质有 Cu 、 Fe 、 Ni 、 Co 、 Zn 、 As 、 Sb 、 Sn 、 Au 、 Ag 、 S 、 Se 、 Te 、 Bi 等。杂质含量主要取决于铅精矿的成分,冶炼方法也影响杂质含量。. 铅需要经过精炼才能被广泛地使用。 精炼的目的一是除去杂质;二是回收贵金属,尤其是银。 我国现行的精铅国家标准: GB/T469-1995:.

情景六 粗铅精炼
E N D
Presentation Transcript
情景六 粗铅精炼 • 6.1 概述 • 视处理方法和原料的不同,生产的粗铅都含有一定量的杂质,一般杂质含量为2% ~4%,少数也有低于2%或高于5%的,粗铅成分见表6-1。 粗铅中含的杂质有Cu、Fe、Ni、Co、Zn、As、Sb、Sn、Au、Ag、S、Se、Te、Bi等。杂质含量主要取决于铅精矿的成分,冶炼方法也影响杂质含量。
铅需要经过精炼才能被广泛地使用。 精炼的目的一是除去杂质;二是回收贵金属,尤其是银。 我国现行的精铅国家标准:GB/T469-1995:
粗铅精炼的原料有三类: • 第一类是铅熔炼或铅锌冶炼产出的粗铅,俗称矿产粗铅(简称矿铅); • 第二类是再生铅; • 第三类是锡冶炼副产粗铅。 • 粗铅的精炼方法有火法和电解法两种。 目前世界上采用火法精炼的厂家较多,约占世界精铅产量的70%,只有加拿大、秘鲁、日本和我国的一些炼铅厂采用电解精炼。
火法精炼是利用杂质金属与主金属(铅)在高温熔体中物理性质或化学性质方面的差异,形成与熔融主金属不同的新相(如精炼渣),并将杂质富集于其中,从而达到精炼的目的。火法精炼是利用杂质金属与主金属(铅)在高温熔体中物理性质或化学性质方面的差异,形成与熔融主金属不同的新相(如精炼渣),并将杂质富集于其中,从而达到精炼的目的。 • 例如: • 铜在粗铅中的溶解度随温度降低而减小,因而可采用熔析除铜; • 铜对硫的亲和力大于铅,因而有加硫除铜; • 砷、锑、锡等杂质对氧的亲和力大于铅,因而有氧化(或氧化加碱)精炼和碱性精炼除砷、锑、锡; • 在含杂质金属的粗铅中添加第三种甚至更多种金属,它们与杂质金属形成金属间化合物(合金)的亲和力大于铅,因而有加锌除银、加钙镁除铋等方法。
火法精炼的优点是设备简单、投资少、占地面积小,并可以按粗铅成分和市场需求采用不同的工序。从而产出多种牌号的精铅。含铋和贵金属少的粗铅最宜采用火法精炼。火法精炼的优点是设备简单、投资少、占地面积小,并可以按粗铅成分和市场需求采用不同的工序。从而产出多种牌号的精铅。含铋和贵金属少的粗铅最宜采用火法精炼。 火法精炼的缺点是铅直收率低,劳动条件差,工序繁杂,中间产品处理量大。 粗铅火法精炼的典型流程
铅的电解精炼技术的优点:产品质量高,生产过程稳定,操作条件好。缺点:生产周期长,占用资金大,投资大,生产成本略高。 铅的电解精炼技术的优点:产品质量高,生产过程稳定,操作条件好。缺点:生产周期长,占用资金大,投资大,生产成本略高。 铅电解精炼的一般工艺流程如图所示:
6.2粗铅火法精炼 1、除铜 粗铅精炼除铜有熔析和加硫两种方法:初步脱铜用熔析法,深度脱铜用加硫法。 (1)熔析法除铜 熔析除铜的原理是: 基于在低温下铜及其某些(As、Sb、Sn、S等)化合物在铅水中的溶解度变小。 见Cu-Pb二元系相图 粗铅熔析可使含铜量降至wCu=0.02%~0.03%,比Pb-Cu共晶成分含铜wCu=0.06%还低。
(2)加硫法除铜 熔析除铜可将铅含铜降至0.1%左右。如果进行电解精炼,熔析后的粗铅即可铸成阳极。如果继续进行火法精炼,熔析除铜后的粗铅还需采用加硫的方法进一步脱铜,直至铅含铜降至wCu=0.001%~0.003%。 加硫除铜多用硫磺作硫化剂,也可用黄铁矿或高品位铅精矿。 当用硫磺作硫化剂时,虽然铅首先按式: 被硫化,但是由于硫对铜的亲和力比对铅大,故按式: 形成Cu2S。 2 [Pb] +S2= 2[PbS] [PbS]+2[Cu]=[Pb]+ (Cu2S)
由于Cu2S不溶于铅,且铅的浓度可视为不变。上式可变为:由于Cu2S不溶于铅,且铅的浓度可视为不变。上式可变为: 由此可见,粗铅加硫除铜过程中,铅水对PbS的溶解度越大,则残存的铜浓度便越小。对330一350℃温度下PbS饱和(WPbS =0.7%一0.8%)的铅水,理论上残存的最小含铜量仅有百万分之几,但实际上只降到0.001%~0.002%。
除 铜 工 艺
在进行除铜作业时,首先将粗铅装入锅内加热熔化,粗铅质量好时加热到500℃就可用捞渣机捞渣。捞完渣后就淋水降温,分2 ~3次淋水,每加一次水撇一次稀渣,最后把铅液降至330 ℃左右,撇净稀渣并打净锅帮后,搅拌加入硫磺粉进一步除铜。当粗铅质量不高,特别是含铜高时,浮渣量较大,为了降低渣率和渣含铅,要把铅液温度加热到650 ~700 ℃,并用压渣坨压渣,以提高渣温度,降低渣含铅。压渣后捞渣,容量为50t的锅产渣量4~8t。
装锅时,先装前锅稀渣,再装粗铅及其他含铅物料;若处理残极,则不得混入稀渣。装锅时应装紧密,以便快速熔化。压渣要压2 ~3次,压渣要均匀,压好后即可捞渣,同时压火降温。每次捞渣时,捞渣机要在铅液上停留至不再有铅液往下滴方可离开,以减少浮渣含铅。捞出的渣倒入渣盘集中,然后再送往指定地点,待作浮渣处理回收铜备用。 • 捞完渣后,锅中铅液面较低且温度较高,为了降温和提高铅液面需二次装入粗铅即续锅,续满并熔化后捞二次渣。当铅液温度降至500℃以下,可按前述淋水降温熔析,并加硫除铜。加完硫磺后逐渐升温到450 ~480 ℃,反应30~60min,捞出硫化渣后返回下一锅;铅液则待下一步除砷、锑、锡作业,后续过程如不采用火法精练,此时的铅液直接浇铸成阳极板送电解精炼。
⑶ 铜浮渣的处理 所谓“浮渣”,一般都是指火法精炼过程中浮在熔融(主)金属表面上,由精炼过程形成的杂质化合物及机械夹带的主金属液滴(块)所组成的固体物质。 熔析除铜产出的浮渣一般含Cu 10%-20%,Pb 60%-80%。
各炼铅厂均用苏打—铁屑法专门处理铜浮渣。其优点是铅回收率高,达到95 ~98%;铅锍含铅低,铜铅比高,可达4 ~8,铜回收率可过85 ~90%。处理浮渣的炉料配比列于表6-5。
配入苏打是为了降低炉渣和硫的熔点,形成钠锍,降低渣含铅并使砷、锑形成砷酸钠、锑酸钠造渣,脱除部分砷、锑.反应如下:配入苏打是为了降低炉渣和硫的熔点,形成钠锍,降低渣含铅并使砷、锑形成砷酸钠、锑酸钠造渣,脱除部分砷、锑.反应如下: 配入焦炭足为了维持炉内有一定的还原气氛,防止硫化物氧化,以保证造硫有足够的硫,并有还原Pb0的作用。配入Pb0 可使部分砷挥发,减少黄渣的生成,提高铅回收率加Pb0。
铁屑是不配入炉料中的,一般是在放渣后分批加入铁屑,并搅拌,使其与硫充分反应,降低硫中含铅量,加入量以加入的铁屑不再发生作用为止,其化学反应式为:铁屑是不配入炉料中的,一般是在放渣后分批加入铁屑,并搅拌,使其与硫充分反应,降低硫中含铅量,加入量以加入的铁屑不再发生作用为止,其化学反应式为: PbS十Fe=Pb十FeS 国内铅厂处理铅浮渣大多用反射炉。浮渣反射炉燃料可用块煤或粉煤。 熔炼作业包括加料、升温熔化、放渣、加铁屑转换、沉淀分离、放锍、加部分料降温、出铅,整个作业时间为14 ~20h,加料前,将浮渣与试剂按确定的比例配料混合,待炉膛加热到1000 ℃以上时,将炉料加入炉内,在熔化期间保持炉温1100 ~1200 ℃,待炉料熔化后,搅拌一次,并提高炉温达1200 ~1300 ℃,静止30 ~40min后,开始放渣。
放渣放锍均要掌握“宽口、薄溜、勤取样”的原则,尽量避免开溜过深而带出锍或铅液。高温放渣的目的在于降低炉渣的粘度,降低炉渣中的含铅量及含铜量。放完渣后,向炉内分批加入铁屑,并搅拌,以使炉料和铁屑充分反应,并升高温度,沉淀30 ~40min,使锍和粗铅进一步分离后再放锍。开始放锍时,溜口开得深一些,使其流动得快,并将炉内残存的粘渣带出,同时,要勤取样观察,一旦发现有铅带出,立即堵溜停放,准备放铅。有的工厂将渣与锍在一次放出,送鼓风炉进一步富集铜,分离铅。 • 炉子烟气经降温后用布袋收尘,烟尘率为3%~5%。粗铅中的铟在熔析除铜过程中大部分进入浮渣,浮渣处理时它主要进入烟尘,该烟尘作为铅厂回收铟的原料。
(4)连续脱铜 有的工厂采用连续除铜作业。 粗铅连续脱铜也是用熔析除铜的原理。首先形成冰铜: 配料中还加入铁屑、苏打和焦炭。铁屑能与PbS发生沉淀反应Fe+PbS=Pb+FeS,从而降低冰铜中的含铅量。苏打则与PbS进行反应: 既降低冰铜中的含铅量,也降低冰铜的熔点。其余的钠便形成砷酸盐,锑酸盐或硅酸盐入渣。 2Cu十PbS(FeS)=Cu2S十Pb (Fe) 2PbS+2Na2CO3十C=2Pb+2Na2S+3CO2 PbS+Na2CO3十C=Pb+Na2S+CO+CO2 PbS+Na2CO3+CO=Pb+Na2S+2CO2
其操作是在一个较深熔池(1.2 ~1.8m)的炉中进行的。在深熔池中,熔体自上而下温度逐步降低,形成一定的温度梯度,粗铅液加入熔池上部,低温铅液自深池底部虹吸放出,铅液自上而下运动,温度逐步降低,底层温度控制在400 ~450 ℃。随着温度的降低,铅中溶解的铜自下而上移动,浮到熔池上层被加入的硫化剂(一般为PbS)硫化形成铜锍,依据其聚积量的多少,定期放出炉渣和锍。放锍前加入铁屑,以降低锍中含铅量。粗铅液则根据鼓风炉的生产和铅包大小,不断地加入炉内。自底部放出的含铜低的低温铅液则视下道 工序的需要定期放出。须保持炉内铅液液面大致稳定,可在300mm范围内波动。因此,可以认为粗铅连续脱铜炉是把处理铜浮渣的反射炉置于熔铅锅上方的联合冶金装置。
6.2.3 粗铅精炼除砷、锑、锡 • 除铜后的粗铅还含有Sn、As、Sb、Bi、Ag、Au等杂质。在火法精炼中,这些杂质将分别被除去,而首先是除砷、锑、锡。粗铅精炼除砷、锑、锡的基本原理相同,且可在一个过程中完成。 • 粗铅精炼除砷、锑、锡有氧化精炼和碱性精炼两种方法: • 氧化精炼是借助于空气的氧对杂质的氧化造渣除去; • 碱性精炼则是利用硝酸钠(NaNO3 )做氧化剂将杂质氧化造渣除去。分离As、Sb、Sn后的粗铅开始变软,所以将除As、Sb、Sn的粗铅精炼称为软化精炼,精炼后的铅称为软铅。
氧化精炼虽然设备简单,操作容易,投资少;但其缺点是铅的损失大,直接回收率低,作业时间长,劳动条件差,燃料消耗高,精炼后残锑高,故很少采用。氧化精炼虽然设备简单,操作容易,投资少;但其缺点是铅的损失大,直接回收率低,作业时间长,劳动条件差,燃料消耗高,精炼后残锑高,故很少采用。 • 碱性精炼的主要优点是作业可在较低温度下进行,金属损失小,燃料消耗少,操作条件好,终点产品含砷、锑、锡比较低,试剂NaOH和NaCl可部分再生;缺点是过程所产生的各种碱渣处理比较麻烦,试剂消耗大。目前大多数精炼厂采用碱性精炼除砷、锑、锡。
碱性精炼 • 广而言之,所谓碱性精炼是加碱于熔融粗金属中,使氧化后的杂质与碱结合成盐而除去的火法精炼方法。 • 粗铅碱性精炼的实质是使粗铅中杂质氧化并与碱造渣而与铅分离,但该过程可以在比氧化精炼较低温度(400~450℃)下进行,且氧化剂主要不是空气而是硝石(NaNO3) • 其原理是利用杂质元素As、Sb、Sn对氧的亲和力大于主金属铅,从而优先将As、Sb、Sn氧化为高价氧化物,然后它们再与NaOH形成相应的钠盐从而与铅分离,其反应速度快,进行得完全, As、Sb、Sn等杂质在铅中的残留量都比较低。 • 往粗铅中加入硝石后,硝酸钠熔于熔体中,在450℃的高温下分解析出O2: • 2NaNO3==Na2O+N2↑+2.5O2 ↑
硝石分解析出的O2(实际上是以活性大的原子氧[O]释出)使杂质氧化并形成相应的钠盐,如砷酸钠、锡酸钠和锑酸钠,故其反应式分别为:硝石分解析出的O2(实际上是以活性大的原子氧[O]释出)使杂质氧化并形成相应的钠盐,如砷酸钠、锡酸钠和锑酸钠,故其反应式分别为: 2As+4NaOH+2NaNO3==2Na3AsO4+N2↑+2H2O 2Sn+6NaOH+4NaNO3==5Na2SnO3+N2↑+3H2O 2Sb+4NaOH+2NaNO3==2Na3SbO4+N2↑+2H2O 一些铅也被氧化生成铅酸钠(Na2PbO2),但其中的Pb最后又会被Sn、Sb、As置换出来: 5Pb+2NaNO3==Na2O+5PbO+N2 ↑ PbO+Na2O== Na2PbO2 Sn+2Na2PbO2+H2O==Na2SnO3+2NaOH+2Pb 2As+5Na2PbO2+2H2O ==2Na3AsO4+4NaOH+5Pb 2Sb+5Na2PbO2+2H2O ==2Na3SbO4+4NaOH+5Pb
由于上述反应,最终进入碱性精炼渣中的铅较少。此外过程中还要加入食盐,虽然它不起化学反应,但是提高了NaOH对杂质盐的吸收能力,所以能降低炉渣的熔点和粘度,减少NaNO3的消耗。每除去1kgSn、As、Sb消耗的各种试剂量列于表6-8。由于上述反应,最终进入碱性精炼渣中的铅较少。此外过程中还要加入食盐,虽然它不起化学反应,但是提高了NaOH对杂质盐的吸收能力,所以能降低炉渣的熔点和粘度,减少NaNO3的消耗。每除去1kgSn、As、Sb消耗的各种试剂量列于表6-8。
碱性精炼的装置是在精炼锅上放置一个反应器,如图6-7。试剂从上部加入反应器,铅液离心泵将锅中的铅液扬至反应器与试剂反应,反应后从筒下部流回锅中,如此反复循环,反应器中还可装上搅拌机,使铅液与试剂有更良好的接触,以加快反应。当渣子变粘稠,铅试样发亮蓝色,说明过程已到终点,关闭反应器底部的阀门,吊出反应器,缷出渣子,最后将铅液扬至除银锅进行加锌除银作业。反应时间决定于粗铅中杂质含量,通常每除去1t锑需10h,1t砷或锡则需17h。碱性精炼的装置是在精炼锅上放置一个反应器,如图6-7。试剂从上部加入反应器,铅液离心泵将锅中的铅液扬至反应器与试剂反应,反应后从筒下部流回锅中,如此反复循环,反应器中还可装上搅拌机,使铅液与试剂有更良好的接触,以加快反应。当渣子变粘稠,铅试样发亮蓝色,说明过程已到终点,关闭反应器底部的阀门,吊出反应器,缷出渣子,最后将铅液扬至除银锅进行加锌除银作业。反应时间决定于粗铅中杂质含量,通常每除去1t锑需10h,1t砷或锡则需17h。 • 如果粗铅含杂质较高,反应可分两段进行。第一段主要产出含杂质高的渣子,第二段再加新试剂,以得到优质铅液,渣子则返回第一段使用。 • 粗铅的碱性精炼也实现了连续操作。
6.2.4 铅的提银精炼 目前,铅的提银精炼普通采用加锌法。 其过程的实质便是在适当的温度下将锌加入到含金银的铅水中并不断搅拌,由于锌对金银的亲和力较大。从而相互结合成锌金化台物和锌银化台物。这些化合物熔点高,密度小,稳定且不溶于被锌饱和的铅水,因此以固体银锌壳形态浮至铅水表面,而与铅分离。
加锌除银过程中,铜、铁、镍、钴等也与锌形成高熔点化合物进入银锌壳,增加锌的消耗和降低银锌壳中贵金属的含量,并使银锌壳变成糊状难以与铅进行分离所以,在加锌提银精炼之前,必须将这些杂质先行除去。加锌除银过程中,铜、铁、镍、钴等也与锌形成高熔点化合物进入银锌壳,增加锌的消耗和降低银锌壳中贵金属的含量,并使银锌壳变成糊状难以与铅进行分离所以,在加锌提银精炼之前,必须将这些杂质先行除去。 溶解于粗铅中的锌,与粗铅中的银发生如下反应: 2Ag+3Zn==Ag2Zn3 2Ag+5Zn==Ag2Zn5 因Ag2Zn3和Ag2Zn5熔点高,分别为665℃和636 ℃,它们在铅液中的溶解度很小,所以可以认为它们在铅液中的浓度已达到饱和浓度,故可视其浓度[Ag2Zn3][Ag2Zn5]数值为常数,因此上面反应式的平衡常数可写成: K1=[Ag]2[Zn]3 K2=[Ag]2[Zn]5 可见,要使银最少,则锌的浓度应达最大,即达其饱和值,升高温度可提高锌在铅水中的溶解度,但温度过高,锌则被空气氧化而造成消耗量增加,所以作业温度选择在450~550℃范围内。
除金的原理与除银相似。因金对锌的亲和力大于银,故首先Au-Zn化合物进入富渣中。除金的原理与除银相似。因金对锌的亲和力大于银,故首先Au-Zn化合物进入富渣中。 • 加锌除银操作程序是间断在在精炼锅中进行。作业周期包括加含银铅、加入返料贫银锌壳、加温、搅拌、降温和捞渣(银锌壳)等。其中加锌反应仅20~30min。作业周期主要取决于升温和降温速率。降温速率为10 ~12 ℃/h,每锅需15 ~20h。
富银锌壳的产率为粗铅的1.5% ~2.0%,其成分(%)为:6 ~11Ag, 0.01 ~0.02Au, 25 ~30Zn, 60 ~70Pb。 除银后的铅含Ag3 ~10g/t,Au微量,Zn0.6% ~0.7%。对于含银为1 ~2kg/t的粗铅,除银耗锌量为8 ~15kg/t铅。 加锌提银也可连续作业。1932年,皮里港铅厂首先实现铅的连续加锌提银精炼,故连续除银锅也称皮里港式连续除银锅。 锅形如桶,高6.9m,最大直径3m。首先往锅内注入已除银的铅液作底液,并加入锌液(420 ℃),锌便漂浮在铅液的上面。其后,连续注入待脱银的软化铅(即已除去Sn、As、Sb的铅),因粗铅密度较大而穿过熔融锌层向下移动,铅液被锌液浸染而饱和锌。锅外燃料燃烧加热维持锅内一定的温度梯度,锅上部为630 ℃左右,锅底部约为430 ℃。当铅液从上往下流动时,锌银(金)合金不断从铅液析出,在虹吸管外向上运动,与铅液形成对流。锌液往复运动而富集金银。银锌壳(约15%Ag、150g/t Au、60%Zn、20%Pb)定期从上部捞出,用蒸馏法回收锌并返回,同时产出贵铅送去回收金银。除银后的铅液则沿虹吸管上升被连续抽走。
与间断操作比较,连续精炼除银的优点是: • (1)提高了劳动生产率,操作过程简化。 • (2)精铅含银稳定在1 ~10g/t之间。 • (3)银锌壳的产量少,其中含银高1 ~2倍。 • (4)进入银锌壳的铅要少2 ~3倍。 • 但是连续精炼锅上部的温度高,锌对上部锅壁腐蚀大。
由于粗铅精炼所产的富银锌壳含银高达10%左右,一般火法精炼车间均设银锌壳处理工序。首先蒸馏脱锌,然后进行灰吹除铅,回收金银。蒸馏原理是由于锌的沸点为907℃,银为1935 ℃,铅为1527 ℃,在熔析除去夹带的金属铅后进行蒸馏加收锌,锌蒸气冷凝后得到的液体锌返回除银作业使用,余下的蒸馏渣含锌仅0.5%~1.0%,主要成分是银和铅,称为贵铅。将贵铅进行灰吹除铅,即在分银炉中氧化除去其中的铅和少量铜、铋、锑等杂质,产出金银合金铸成银阳极,再进行粗银电解精炼,分别回收金和银。
铅的脱锌精炼 加锌提银后的铅中常残留有wZn=0.5%~0.6%,必须进一步精炼除去。铅的脱锌精炼有氧化法、氯化法、碱法和真空法。 (1)氧化法 氧化法是基于锌比铅更容易氧化,向铅液中鼓入空气,锌氧化生成不溶于铅的氧化锌而被除去。这是个老方法,因作业时间长、回收率低、劳动条件不好而很少采用。 (2)氯化法 氯化法是向铅液中通入氯气,将锌变成ZnCl2除去,其缺点是有过量未反应的氯逸出,给污染治理带来许多麻烦,还不能把锌除至要求的程度,仍要加NaOH除去残留的锌。
(3) 碱法脱锌 • 碱法脱锌的原理与碱法除砷、锑、锡大致相同,也采用NaOH和NaCl做反应剂,但无需用NaNO3做氧化剂,锌的氧化剂为空气中的氧。其反应为: • 每吨锌消耗NaOH1t,NaCl 0.75t,过程不需加热即可维持450℃,每除去1t锌约需12h,产出的Na2ZnO2浮渣经水浸蒸发结晶得到NaOH与NaCl可返回再用,锌以ZnO形式回收。 • 缺点:碱的回收再生作业比较麻烦且费用高 Zn+0.5O2=ZnO Zn+PbO=ZnO十Pb ZnO+2NaOH=Na2ZnO2+H2O
上述各种方法的除锌的共同缺点是锌以化合物形态进入精炼渣,不能以金属态的冷凝锌回收再返回除银工序。 (4) 真空蒸馏法脱锌(物理方法) 真空法脱锌是基于锌比铅更容易挥发的原理使铅与锌分离。 铅和锌的蒸汽压只决定于温度和合金成分,而与系统的残压无关。残压只影响蒸发速度。蒸发速度还与蒸发表面有关,所以力求薄层蒸发,并在搅拌和喷雾情况下进行。 优点是回收的锌可返回除银工序,且效率高,成本低。 澳大利亚皮里港铅厂的连续真空脱锌设备如图6-11。
6.2.6 铅的脱铋精炼 粗铅火法精炼除铋比较困难,当粗铅含铋较高时,采用电解法比较适宜。火法精炼通用的是加钙、镁、锑法,还有加钾、镁、锑法。 加钙镁除铋是基于钙镁与铅水中的铋能形成较为难熔的化合物。这些化合物不溶于铅水中,从而以硬壳状的铋质浮渣浮至铅面而被除去。 铋与钙能形成Bi2Ca3(熔点928℃)和Bi3Ca(507℃分解)两种化合物;而Bi-Mg系有一种化合物Bi2Mg3,熔点823℃。 加钙,钙以wCa=2%~5%的铅钙合金加入,它与铋进行下列反应: Pb3Ca+3Bi=Bi3Ca+3Pb 加镁时,反应为: 3Mg+2Bi=Mg3Bi2
同时加入钙和镁时,除铋将更彻底,此时的反应为:同时加入钙和镁时,除铋将更彻底,此时的反应为: Ca+2Mg+2Bi=CaMg2Bi2 钙、镁与铋形成的化除铋合物虽密度比铅小,但由于他们呈微细颗粒悬浮于铅液中,不易除去,影响结果。若加入适量的锑,由于锑和钙、镁分别形成易上浮的Sb2Ca3、Sb2Mg3和Mg2CaSb2颗粒,能将悬浮的微粒Mg2CaBi2夹带至表面被除去。
除铋作业在精炼锅中进行,作业时间依容量而定,150t锅作业周期8 ~10h,260t锅则为12h。过程温度控制在350℃左右,加钙镁时360 ℃ ,捞铋渣时330 ~340 ℃ 。 • 如果将铋的含量除到0.02%时,钙和镁的消耗可按下式计算: • QCa=CBi+0.57 • QMg=2CBi+0.7 • 式中QCa、QMg 精炼1t铅所消耗的钙、镁千克数; • CBi 粗铅中含铋量(%)。 • 一般锑的消耗为铋含量的30倍。
粗铅除铋后,粗铅中的Cu,As,Sn,Sb,Ag,Zn,Bi等杂质含量能达到产品标准要求,可能还残留些加入的试剂如Ca,Mg,Sb,K,Na等。为了确保产品质量要求,铸锭之前进行最终精炼,即在原精炼锅中加入铅量0.3%左右的NaOH和0.2%左右的NaNO3,搅拌2~4h进行碱性精炼,捞完渣后,即可浇注成精铅锭。粗铅除铋后,粗铅中的Cu,As,Sn,Sb,Ag,Zn,Bi等杂质含量能达到产品标准要求,可能还残留些加入的试剂如Ca,Mg,Sb,K,Na等。为了确保产品质量要求,铸锭之前进行最终精炼,即在原精炼锅中加入铅量0.3%左右的NaOH和0.2%左右的NaNO3,搅拌2~4h进行碱性精炼,捞完渣后,即可浇注成精铅锭。
6.3 粗铅的电解精炼 6.3.1 概述 我国炼铅厂的粗铅精炼大都采用粗铅火法精炼(除铜)-电解精炼的联合工艺流程。它的火法精炼部分只是除铜,也有工厂还除锡,得到的是初步除铜(锡)粗铅,被浇铸成阳极板送去电解。初步火法精炼产出的粗铅一般含98 ~98.5%Pb、1.5% ~2.0%的杂质。
由于铅的电化当量比较大,标准电极电位又较负,给粗铅电解精炼创造了有利的条件。由于铅的电化当量比较大,标准电极电位又较负,给粗铅电解精炼创造了有利的条件。 • 电解精炼是利用阳极中不同元素的阳极溶解或在阴极析出难易程度的差异来提纯金属的,其基本原理是以电化学基础理论为依据。
阴极板是利用析出铅(纯铅)熔化制作的始极片(阴极),按一定的间距装入盛有电解液的电解槽中,电解液由硅氟酸和硅氟酸铅的水溶液组成。将电解槽接通直流电,铅自阳极溶解进入电解液,并在阴极放电析出。粗铅电解的电化学体系如图所示。阴极板是利用析出铅(纯铅)熔化制作的始极片(阴极),按一定的间距装入盛有电解液的电解槽中,电解液由硅氟酸和硅氟酸铅的水溶液组成。将电解槽接通直流电,铅自阳极溶解进入电解液,并在阴极放电析出。粗铅电解的电化学体系如图所示。
在电解精炼体系中,当外电源的直流电流通过电解槽时,在电极上发生电化反应,其电解反应为原电池反应的逆过程,也就是将电能转变成化学能的过程。为了讨论问题一致,总是规定在电解精炼体系中,当外电源的直流电流通过电解槽时,在电极上发生电化反应,其电解反应为原电池反应的逆过程,也就是将电能转变成化学能的过程。为了讨论问题一致,总是规定 • 电解槽中从外电路输入电子(e-)的电极为阴极,在此电极上进行还原反应; • 向外电路输出电子的电极为阳极,在该电极上进行氧化反应。 • 在两极通以直流电后,溶液中的铅离子(Pb2+)便移向阴极,获得电子后就成为铅原子沉积在阴极上,产出纯度很高的电解铅电析出铅;在阳极方面,由于电源不断地从它上面把电子取走,结果阳极方面原子因为失去电子成为离子。当硅氟酸离子(SiF62-)移向阳极与这些Pb2+离子接触时,便形成PbSiF6, Pb2+离子就陆续从阳极脱离,进入溶液。由此可见,整个电解精炼过程包括阴极反应和阳极反应,总反应为: • Pb(含杂质)→ Pb(纯)
在电解精炼过程中,阳极中所含电位比铅负的金属如锌、铁、镉、钴、镍等,与铅一道自阳极溶出,但一般不在阴极析出;在电解精炼过程中,阳极中所含电位比铅负的金属如锌、铁、镉、钴、镍等,与铅一道自阳极溶出,但一般不在阴极析出; • 电位比铅正的金属如锑、铋、铜、金、等,几乎都不进入电解液,而留在阳极泥中; • 电位与铅接近的锡,电解时与铅一道溶解并大部分在阴极上析出,须用电解法以外的方法除去。 • 综上可见,电解精炼是利用阳极中不同元素的阳极溶解或在阴极析出难易程度的差异来提纯金属的,其基本原理是以电化学基础理论为依据。
6.3.2 电解冶金的电化学依据 所谓电解,是指在一定外加电压下,将直流电流通过电解池,在两极分别发生氧化反应和还原反应的电化学过程。 6.3.2.1 电极和电极反应 电解池是由两个金属导体分别插入电解质溶液构成。电极的概念应当是指“金属/溶液”体系,即包括金属及其相邻的电解液界面两部分组成;但从工程角度,习惯上把“金属/溶液”体系中的金属部分称为电极。 连接直流电源正极的不纯金属称为阳极 连接直流电源负极的纯金属称为阴极。 接通直流电源并逐渐增加两极间直流电压,则有电流通过电解池并逐渐增大。