Elettrochimica
550 likes | 1.34k Views
Elettrochimica. Elettrochimica è lo studio delle reazioni chimiche che producono effetti elettrici E dell’opposto, cioè dei fenomeni chimici che sono causati dall’azione della corrente o del voltaggio. Redox Reactions. Reduction. Oxidation. Oxidation : Gain of oxygen Loss of electrons.

Elettrochimica
E N D
Presentation Transcript
Elettrochimica Elettrochimica è lo studio delle reazioni chimiche che producono effetti elettrici E dell’opposto, cioè dei fenomeni chimici che sono causati dall’azione della corrente o del voltaggio
Redox Reactions. Reduction Oxidation
Oxidation: • Gain of oxygen • Loss of electrons • Reduction: • Loss of oxygen • Gain of electrons Increase in oxidation number Decrease in oxidation number
Reazioni Redox Ossidazione • Perdita di elettroni Riduzione • Acquisto di elettroni agente ossidante • sostanza che, riducendosi, causa ossidazione agente riducente • sostanza che, ossidandosi, causa riduzione
Zn + Cu2+SO42- Zn2+SO42- + Cu n.o. 0 +2 +2 0 RED1 OX2 OX1 RED2 Zn2+/Zn = coppia coniugata redox 1 Cu2+/Cu = coppia coniugata redox 2 LE REAZIONI DI OSSIDORIDUZIONE SONO RICONDUCIBILI ALL’INTERAZIONE TRA DUE COPPIE OSSIDORIDUTTIVE CHE SCAMBIANO ELETTRONI. SIMILITUDINE CON REAZIONI ACIDO BASE (DUE COPPIE CONIUGATE ACIDO/BASE) Semireazione di ossidazione Zn(s) Zn+2(aq) + 2 e- Semireazione di riduzione Cu+2(aq) + 2 e- Cu(s)
Cella voltaica o galvanicaUna reazione chimica modificata per generare corrente Celle e Reazioni di Cella Cella di Daniel Zn(s) + Cu+2(aq) Zn+2(aq) + Cu(s) Semireazione di ossidazione anodo Zn(s) Zn+2(aq) + 2 e- Semireazione di riduzione catodo Cu+2(aq) + 2 e- Cu(s)
Cella di Daniel Un elettrodo di rame immerso in una soluzione di solfato di rame (II) Un elettrodo di zinco immerso in una soluzione di solfato di zinco ZnZn+2+2 e- Cu+2+2 e-Cu
Galvanic Cell: cariche elettriche ZnZn+2 Cu+2Cu Il ponte salino o disco poroso permette la migrazione degli ioni così che la soluzioni rimangono neutre :
Galvanic Cells: gli elettroni ZnZn+2+2 e- Cu+2+2 e-Cu Anodo: ossidazione Carica (+) Catodo: riduzione Carica (-)
Potenziale di cella Gli elettroni sono spinti dalla reazione di ossidazione ed accettati dalla reazione di riduzione. Questo genera corrente elettrica: potenziale di cella, o forza elettromotrice. Misurato in Volt Esso è positivo e misurabile sperimentalmente Misurato come la differenza di potenziale tra gli elettrodi di una cella elettrochimica Se misurato in condizione standard ( concentrazione, pressione, temperatura) si ottiene la E°, il potenziale standard della cella.
“regole” delle celle elettrochimiche • All’anodo gli elettroni sono prodotti dall’ossidazione. • Al catodo gli elettroni sono reagenti per la riduzione. • Gli elettroni si muovono nei cavi allontanandosi dall’anodo • Gli anioni tornano verso il (–) per caricare l’ anodo.
Potenziale di cella standard E°, la differenza di potenziale, in volts, tra gli elettrodi di una cella elettrochimica in condizioni standard (25oC, concentrazione degli ioni = 1 M, ed i gas alla pressione di 1 atm)
Elettrodo standard ad idrogeno consiste in un elettrodo di platino coperto da una polvere sottile di platino intono a cui gorgoglia H2(g). Il suo potenziale è definito come 0 volts. Semicella a Idrogeno H2(g) = 2 H+(aq) + 2 e- reazione reversibile 2H+(aq, 1M) + 2e- H2(g, 1 atm) E = 0 V
Potenziale di elettrodo E’ utile considerare il potenziale di cella come la somma dei due potenziali di elettrodo: E° = E°(catodo) + E°(anodo) Per fare ciò si è definito come potenziale 0 quello dell’elettrodo H 2H+ (aq) + 2e- H2(g) + E° = 0.00 Per misurare il potenziale di un elettrodo (es. Zn) basta calcolare il potenziale della cella Zn//H
Gli elettrodi della pila Daniell Lo Zn riduce H+ H2 riduce il Cu2+ Quindi Zn riduce Cu2+
Calcolo potenziale di cella Il potenziale dell’elettrodo a Zn è potenziale di ossidazione = + 0.76 V Il potenziale della reazione opposta è di riduzione = -0.76 V
E° standard Cl2 ha tendenza a ridursi > di Cr3+
Potenziali di elettrodo Per convenzione vengono sempre espressi come potenziali standard di riduzione Ox red
Serie elettrochimica I potenziali standard di riduzione ordinano le sostanze in base alla loro tendenza a ridursi. Esprimono l’energia libera della semireazione in Volt Indicano anche il potere riducente o ossidante. Valori negativi sono associati ad alti poteri riducenti della forma ridotta (es. Zn) Valori positivi ad alto potere ossidante della forma ossidata (es. Cu2+) La serie elettrochimica è in ordine decrescente di potere ossidante
Esempio se si vuole la riduzione di mercurio(II) in una cella voltaica, e la semireazione è: Quale reazione può essere usata all’anodo (ossidazione)? A, B
Diagramma di Cella rappresentazione schematica di una cella elettrochimica che mostra la due semicelle connesse da un ponte salino e equivalente, come Zn(s)/ZnSO4(aq)//CuSO4(aq)/Cu(s) Zn(s)/Zn++//Cu++/Cu(s) anodo catodo Ox Red
Reazioni di spostamento di Metalli • I solidi dei metalli più reattivi spostano gli ioni di metalli meno reattivi • La reattività relativa è basata sui potenziali delle semireazioni • I metalli con potenziali molto diversi reagiscono più vigorosamente
esempio Ag+ + e- Ag E°= 0.80 V Cu2+ + 2e- Cu E°= 0.34 V Ag reagirà con Cu2+? yes, no Cu reagirà con Ag+? yes, no
Energia libera di Gibbs e Potenziale di Cella Se la cella genera corrente (E) essa è spontanea (-DG) DG = - nFE dove n => numero di elettroni scambiati F => constante di Faraday* E => potenziale di cella * F= 96485 Coulomb/mol
Applicazioni delle Celle Electrochimiche Batterie: convertono l’energia chimica in elettricità Celle Primarie • celle elettrochimiche non-reversibili Celle Secondarie • celle elettrochimiche reversibili
Applicazioni delle Celle Electrochimiche Celle Primarie "dry" cell e alkaline cell 1.5 v/cell mercury cell 1.34 v/cell fuel cell 1.23v/cell Celle Secondarie lead-acid (automobile battery) 2 v/cell NiCad 1.25 v/cell
Equazione di Nernst La dipendenza del potenziale dalla concentrazione dei reagenti/prodotti R= costante dei gas, T= temp in K, n= numero di elettroni, F= costante di Faraday E = E0 + RT ln [OX1] nF [RED1] Convertendo il log naturale in decimale e quantificando le costanti, a 25 °C E = E0 + 0.059 log [OX1] n [RED1] E = E0 + 0.0257 ln [OX1] n [RED1] N.B. quando [OX] = [RED] E = Eo
ESEMPIO: Quale è il potenziale di cella per la cella di Daniel quando [Zn+2] = 10 [Cu+2] ?Q = ([Zn+2]/[Cu+2] = (10 [Cu+2])/[Cu+2] = 10Eo = (0.34 V)Cu + (-(-0.76 V))Zn n = 2, (2 gli elettroni scambiati) Ecella = Eocella - (0.0257/n)ln Q così Ecell = (1.10 - (0.0257/2) ln 10) V Ecell = (1.10 - (0.0257/2) 2.303) V Ecell = (1.10 - 0.0296) V = 1.07 V
Celle a concentrazione • una cella il cui potenziale dipende solo da differenze di concentrazione. • Un compartimento contiene una soluzione concentrata, e l’altro una soluzione diluita. • Esempio: 0.025 M Cue 1.50 M Cu2+.
Celle a concentrazione • Le due semi-reazioni sono uguali, quindi Eº è zero .
Misura del pH Meter • Un elettrodo il cui voltaggio cambia col pH • Un elettrodo di riferimento il cui voltaggio non cambia • Un volt meter che converte i millivolts in unità pH. • Un compensatore automatico di temperatura (optionale). reference pH electrode
Fe2+ + 2OH– Fe(OH)2(s) Fe2O3 O2 + 2H2O + 4e– 4OH– Fe2+ cathode anode e– Corrosione e protezione dei metalli Iron
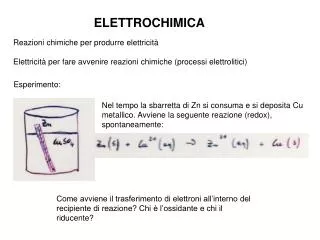
Corrosione, la ruggine Zn Cu Una barretta di ferro messa in un sistema semisolido (agar) che contiene fenoftaleina (Indicatore di pH) Fe (s)à Fe+2 + 2 e- ½ O2(g) + H2O (l) + 2 e-à 2 OH- Fe
Elettrolisi • La disponibilità di elettricità permette di compiere reazioni opposte a quelle delle pile. • Si usa una cella in cui i due elettrodi sono nella stessa soluzione elettrolitica e si applica corrente ai due elettrodi
Refining Elettrolitico del rame Cu(s) + Cu+2(aq) --> Cu+2(aq) + Cu(s) impuro puro anodo catodo
Aspetti quantitativi dell’elettrolisi • 1 coulomb = 1 amp sec • 1 mole e- = 96,500 coulombs N° mol e- =Corrente(C/s)x tempo x1 mol e-/ 96,500 = Amp x sec /96.500
Esempio Quanti grammi di cromo possono essere deposti da una soluzione di Cr+6 in 45 minuti con una currente di 25 amp? (45 min) #g Cr = ------------
Esempio Quanti grammi di cromo possono essere deposti da una soluzione di Cr+6 in 45 minuti con una currente di 25 amp? (45 min)(60 sec) #g Cr = --------------------- (1 min)
Esempio Quanti grammi di cromo possono essere deposti da una soluzione di Cr+6 in 45 minuti con una corrente di 25 amp? (45) (60 sec) (25 amp) #g Cr = --------------------------- (1)
Esempio Quanti grammi di cromo possono essere deposti da una soluzione di Cr+6 in 45 minuti con una currente di 25 amp? definizione del coulomb (45)(60 sec)(25 amp)(1 C) #g Cr = ----------------------------- (1) (1 amp sec)
Esempio Quanti grammi di cromo possono essere deposti da una soluzione di Cr+6 in 45 minuti con una currente di 25 amp? Faraday’s constant (45)(25)(60)(1 C)(1 mol e-) #g Cr = ---------------------------------- (1)(1)(96,500 C)
Esempio Quanti grammi di cromo possono essere deposti da una soluzione di Cr+6 in 45 minuti con una currente di 25 amp? massaatomica (45)(60)(25)(1)(1 mol e-)(52 g Cr) #g Cr = ------------------------------------------- (1)(1)(96,500) (6 mol e-)
Esempio Quanti grammi di cromo possono essere deposti da una soluzione di Cr+6 in 45 minuti con una currente di 25 amp? (45)(60)(25)(1)(1 mol e-)(52 g Cr) #g Cr = ------------------------------------------- (1)(1)(96,500)(6 mol e-) = 58 g Cr