Gold Katalyse
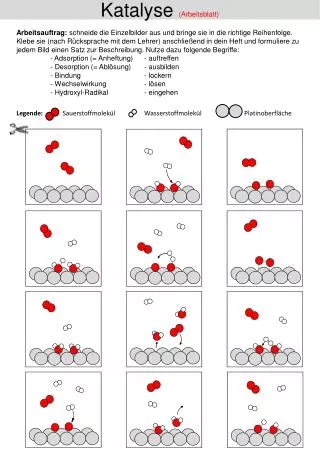
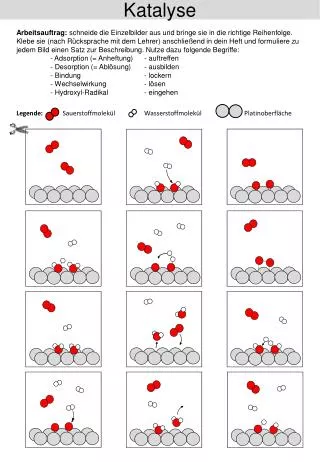
Gold Katalyse. Literatur: Angew. Chem. Int. Ed. 2006 , 45 , 7896-7936. Homogene und Heterogene Hydrogenierung / Dehydrogenierung. Heterogene Hydrogenierung. 1950, Couper und Eley : Gold-Oberflächen katalysieren die Umwandlung von para -Wasserstoff in ortho -Wasserstoff

Gold Katalyse
E N D
Presentation Transcript
Gold Katalyse Literatur: Angew. Chem. Int. Ed.2006, 45, 7896-7936
Heterogene Hydrogenierung • 1950, Couper und Eley: Gold-Oberflächen katalysieren die Umwandlung von para-Wasserstoff in ortho-Wasserstoff • Gold-Oberflächen können H2 aktivieren • 1963, Erkelens, Kemball und Gawly: Erste durch Gold katalysierte Hydro-genierung von Alkenen • Aktivierungsenergie für Hydrogenierung ist höher als für Dehydrogenierung
Heterogene Hydrogenierung • 1973, Bond et al.: Effiziente Hydrogenierung bei niedrigen Temperaturen und geringem Goldanteil • Abhängigkeit vom Trägermaterial
Heterogene Hydrogenierung • Chemoselektive Monohydrogenierung • D2 reagiert viel langsamer als H2 → Brechen der H-H Bindung ist geschwindigkeitsbestimmender Schritt
Heterogene Dehydrogenierung / Isomerisierung • 1928, Clark und Toplet: • 1969, Inami et al.: • 1980, Satchler et al.: Eine Monoschicht Au auf Pt verbessert die Rate der Dehydrogenierung von Cyclohexen bei 100 °C um den Faktor 5
Homogene Hydrogenierung • 2006, Corma: Möglicher Mechanismus der homogenen Hydrogenierung • Oxidationsstufe von Au bleibt unverändert • Heterolytische Spaltung geschwindigkeitsbestimmender Schritt Substitution Insertion Heterolytische Spaltung Addition Heterolyse + Eliminierung
Homogene Hydrogenierung • 1995, Baker et al.: Keine β–Wasserstoff Eliminierung bei Au-Komplexen
Homogene Dehydrogenierung • 1999, Hosomi: Hexaalkyldistannane • 2005, Ito et al.: Dehydrogenierende Silylierung
1.Übersicht ∙ Trägerfixierte Gold-Katalysatoren → Epoxidierung von Alkenen → Oxidation von Alkoholen ∙ Heterogene Gold-Katalysatoren → Effiziente C-H-Aktivierung ∙ Legierungen von heterogenen Goldkatalysatoren mit Pd → direkte Bildung von Wasserstoffperoxid aus den Elementen
2.Epoxidierung ∙ Epoxidierung von Ethen mit Sauerstoff und Ag-Katalysator: Selektivität 90 % ∙ Oxidation von Propen problematisch: Selektivität für Epoxid < 10 % ∙ Lösung: Trägerfixierte Goldkatalysatoren für die Epoxidierung von Propen, H2 als Red ∙ verwendete heterogene Gold-Katalysatoren: - Au/TiOx - Au/TS-1 (Si : Ti von 500 : 1) → aktive Zentren: Gold-Spezies mit Durchmesser < 2nm - Au auf mesoporösen Titansilicat-Trägern → Selektivität > 90% zugunsten von Propenoxid, bei Umsatz von 7%
∙ katalytische Mengen Peroxid initiieren Oxidation von Alkenen mit O2 → sehr hohe Selektivitäten zugunsten des Epoxids für Cyclohexen, Styrol, cis-Stilben und Cycloocten ∙ Selektivität stark abhängig vom Lösungsmittel: am besten für substituierte Benzole ∙ „Grüne“ Chemie: - bestimmte Katalysatoren auch in Abwesenheit von Lösungsmitteln aktiv - niedrige Reaktionstemperaturen Tabelle 1: Oxidation von cis-Cycloocten mit O2 unter lösungsmittelfreien Bedingungen
3. Oxidation von Alkoholen und Aldehyden ∙ bisher: trägerfixierte Pd-Nanopartikel - oxidieren Glucose → Gluconsäure Glycerin → Glycerinsäure aber: wenig selektiv ∙ Lösung: trägerfixierte Au-Nanopartikel - hohe Effizienz und Selektivität für Oxidation von Alkoholen und Diolen - Voraussetzung: Vorhandensein einer Base - Katalysatoren: Au/C - auch Oxidation von Zuckern möglich Abbildung 1: Oxidation unterschiedlicher Alkohole mit verschiedenen Katalysatoren
∙ Au/Graphit katalyisiert Oxidation von Glycerin zu Glycerinsäure: - O2 als Ox, milde Bedingungen, NaOH → Selektivität bis zu 100%, Ausbeute 60 % - Selektivität abhängig vom Verhältnis NaOH/Glycerin - mit Pd/C bzw. Pt/C viele Nebenprodukte ∙ „nackte“ Au-Kolloidpartikel katalysieren: - Oxidation von Glucose zu Gluconsäure - Oxidation von 1,2-Diolen Schema 1: Mechanistisches Modell für die Glucose-Oxidation
∙ Au/CeO2: - Oxidationen: Alkohol → Aldehyd, bzw. Keton; Aldehyd → Carbonsäure - O2 als Ox, lösungsmittelfrei, milde Bedingungen → hohe Selektivität ∙ Legierung von Pd mit Au aus Au/TiO2-Kat: - effiziente Oxidation von primären Alkoholen und Diolen ∙ Goldkomplexe: - selektive Oxidation von Alkoholen zu Aldehyden und Ketonen - „grüne“ Chemie: Reaktion mit Luft, Umsatz bis 100%, Selektivität 99 % für Benzaldehyd
4. C-H-Aktivierung ∙ besonderes Interesse: aerobe Oxidation von Cyclohexan ∙ industrieller Prozess: 70-85% Ausbeute, Umsatz 4% ∙ Au-Katalysatoren: - Au/ZSM-5 → 90 % Selektivität für Cyclohexanon - Au/MCM-41 → > 90 % Selektivität für Cyclohexanon - Wiederverwendung der Katalysatoren problematisch → hohe Selektivitäten, allerdings bei hohen Temperaturen (140-160°C)
∙ Au/C-Katalysatoren: - Oxidation von Cyclohexan bei < 100°C - sehr hohe Selektivität bei niedrigem Umsatz - Tendenz identisch zu Pt/C und Pd/C: Selektivität nur vom Umsatz an Cyclohexan abhängig
5. Direkte Wasserstoffperoxidsynthese ∙ Industrie: Anthrachinonverfahren - problematisch für kleine Mengen ∙ optimal: Synthese aus den Elementen (wird seit 90 Jahren angestrebt) ∙ Au/Al2O3: - katalysiert direkte Reaktion von H2 und O2 - bei Au-Pd/Al2O3 Reaktion noch schneller, aber: Selektivitätsproblem → auch Hydrierung zu H2O und Zersetzung in H20 und O2 werden katalysiert Abbildung 2: Auswirkung von Additiven auf die H2O2 – Menge bei der direkten Oxidation von H2
∙ Au/SiO2 bzw. Au-Pd/SiO2: - selbst bei 10°C noch aktiv ∙ Fe2O3 bzw. TiO2 als Trägermaterial: - Selektivitäten von bis zu > 95% (bei kurzen Reaktionszeiten) Tabelle 2: Einfluss der Reaktionszeit auf den H2-Umsatz und die Selektivität der H2O2-Synthese
Gold-Komplexe aktivieren für einen nucleophilen Angriff: • C-C-Doppel- und C-C-Dreifachbindungen in • Isolierten Systemen • Kumulierten Systemen • Konjugierten Systemen • C-O Doppelbindungen in Carbonylgruppen
Einfache Nucleophile ohne konjugierte Mehrfachbindungen Diastereoselektive anti-Addition des Gold-Substituenten und des Nukleophils WW mit dem p-System Nucleophile Addition Protodemetallierung
A) Alkine 1976: Alkine mit Tetrachloridogoldsäure (Thomas et al.) 1985: Hydrochlorierung von Ethin (Hutchings)
A) Alkine Effiziente Synthese von Furanen durch (Z)-3-Ethinylallylalkoholen Spezifische Reaktion mit dem Alkin in Gegenwart des aktivierten Alkens
B) Allene • Anspruchsvollste Substrate für Additionsreaktionen • Chemoselektivität, Diastereoselektivität und Regioselektivität sind relevant Cycloisomerisierung von Allenylcarbinolen zu 2,5-Dihydrofuranen Addition von Anilinen an chirale Allene
C) Alkene Zwei denkbare Reaktionswege: Aktivierung des Alkens und Friedel-Crafts-artige elektrophile Substitution Direkte Aurierung Protodesaurierung
C) Alkene Reaktion von Bis(m-oxo)-Gold(III)-Komplexe mit Norbornen • Gold-Komplex katalysiert die Addition von Wasser an ein Alken • liefert das Epoxid in einer stöchiometrischen Reaktion
C) Alkene Erstes und bislang einziges isoliertes metallorganisches Analogon einer Zwischenstufe einer Gold-katalysierten Reaktion (Cinellu et al.) Auraoxetan Konnte vom Alken-Komplex abgetrennt werden und mittels Röntgenkristallstrukturanalyse zweifelsfrei charakterisiert werden
Cycloisomerisierung von Allenylketonen • 2000: Hashmi et. al. • Wheland Zwischenstufe • Aromatisierung • Protodesaurierung
Bildung von Furanen aus Alkinylketonen • Katalysator koordiniert an Dreifachbindung • Bildung eines Furanlykations • Addition von Methanol
Bildung von Naphthalinen • Bildung einer Pyrylium Zwischenstufe • [4+2] Cycloaddition mit Alkinen oder Alkenen und Ringöffung • Mechanismus wurde durch Rechnung bestätigt
Cyclisierung von Alkinphenolen od. -anilinen • Bildung aus ortho substituierten Aromaten • X=O: AuCl3 • X=NH: Na[AuCl4]∙H2O
Epoxidringerweiterung • Liefert interessantes Substitutionsmuster der Furane • R1: -Me, -Et-OH • R2: -Pr-OH, -Bu-OH, -Ph • Nuc. Angriff des Epoxids schneller als der der Hydroxygruppe
Gold Katalyse Nukleophile Additionen an π -Systeme
Gliederung: • Reaktionen von ambidenten nukleophilen Gruppen in Propargyl – Position • 1.1 Reaktionen über Vinylcarbenoide • 1.2 Reaktionen über Allenylester • 1.3 Reaktionen über Vinylgold-Spezies
1. Gold-katalysierte Reaktionen ambidenter Gruppen in Propargyl-Position Zwei unterschiedliche Reaktionswege: 5-exo-dig – und 6-endo-dig Modus
Reaktionsmodi 5-exo-dig 6-endo-dig Allen Vinylcarbenoid
Reaktionen über Vinylcarbenoide + Alkenylester 26% 2 Diastereomere 63%
Anwendung • Synthese von Caren – Terpenoiden durch Abfangen der Vinylcarbenoide durch Doppelbindung in passender Entfernung Vinylcarbenoid 95%
gute Diastereoselektivität • nur marginale Mengen an isomeren Allenylacetats