Materia
Cetonas. Amonio. Materia. Alma de Raudales. Que es Materia ?. Sustancia por la que estan hechas todas las cosas Masa : medida de la cantidad de materia Peso: accion de la fuerza de gravedad sobre un objeto en particular. Diferencia entre masa y peso.

Materia
E N D
Presentation Transcript
Cetonas Amonio Materia Alma de Raudales
QueesMateria? • Sustanciapor la queestanhechastodaslascosas • Masa: medida de la cantidad de materia • Peso: accion de la fuerza de gravedadsobre un objeto en particular
Diferencia entre masa y peso El peso depende de la fuerza de la gravedadque se ejercesobre el cuepo. • Gravedad de la luna = 0.17 veces de la tierra • Marte: = 0.38 veces de la tierra Ej: Su masa en la luna, esigual a su peso en la tierra Su peso en la lunaes = 0.17 X su peso
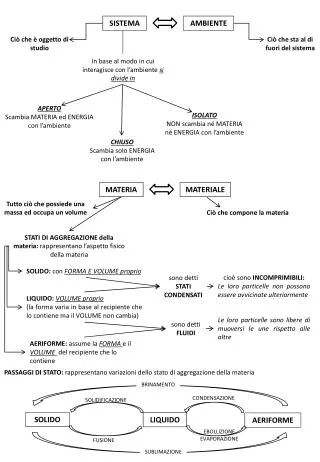
Estados de la Materia solido gas liquido
Cambios de estado Ubicaestoscambios de estado en el cuadro anterior • licuefaccion • Evaporacion • Condensacion • Solidificacion • Sublimacion • depositacion
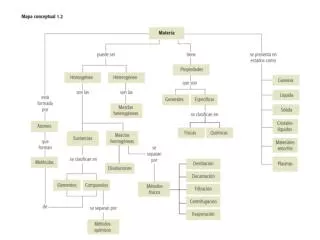
Clasificacion de la Materia M. Heterogeneas
Sustanciaspuras y mezclas Bronce Bario
Propiedades de lasMezclas QueMetodos de Separacion de Mezclasconoce?
Propiedades de la materia Las propiedades, permitenidentificarunasustancia y distinguirla de otras. • PropiedadesFisicas: identifican la sustancia sin alterarsucomposicion ( color, olor D, Pf, PE,dureza, lustre, maleabilidad, ductibilidad . • PropiedadesQuimicas: Ej (arde, se descompone, reacciona, forma otroscompuestos)
Cambios • CambioFisico: sucomposicion no se altera, solo su forma o tamaňo • CambioQuimico:Seconsumenunassustancias y se formanotrassustanciasnuevas:
Elementos Concepto: sustanciapuraque no puede ser descompuesta en sustanciasmas simples pormediosquimicosordinarios. Composicion: Estancompuestosporatomos Ejemplos de Elementos:
Propiedades de los metales • 1. Mayor lustre • Conducenbien la electricidad • Maleables ( se le puededar forma) • Ductiles (se estiran) • Densidadalta • Punto de fusion alto • Duros • No esfacilcombinarlos entre si
No Metales • Lo contrario de metales • PropiedadQuimica: Se combinan entre si • Y formanlasmoleculas • Ej: N₂, Cl₂, Br₂ O₂ etc. • Metaloides: B. Si, Ge, As, Sb, Te, Po, Astato.
compuestos • Sustanciapuraformadapor dos o maselementos en proporcionesdefinidas. • Puededescomponersepormetodosquimicos en dos o massustancias simples (elementos) • Ejemplo de compuestos: • H₂O • CaCl₂ • C₁₂H₂₂O₁₁ • (NH₂)₂CO
Ley de lasProporcionesDefinidas • Todos los compuestostienen un numeroespecifico de elementos en su formula queguardanunaproporciondefinida de combinacion; de acuerdo a la ley de lasproporcionesdefinidas: • Un determinadocompuestopuro, contienesiempre, los mismoselementosexactamente en lasmismasproporcionespormasa.
Tipos de Energia • EnergiaPotencialEj:(gas natural y gasolina) • Energiacalorica (combustion) • Energiamecanica ( cuando el auto funciona) • Energiaquimica (energiaproveniente del acumulador al encender el vehiculo) • Energiaelectrica (produce corrienteelectrica) • Energiamecanica ( estransmitida al motor de arranque) • Energiacinetica: el carro se mueve.
Energia y fotosintesis • Energiaradiante o luminosa: (luz solar) • EnergiaQuimica: iniciaprocesosquimicos = Carbohidratos Medida de la Energia 1. Caloria: Calornecesarioparaelevar la oT de 14.5 – 15.5 oC 2. Joule (SI) 1cal = 4.184 J 3. Caloriagrande o Kcal = 1000 cal